名校
解题方法
1 . 下列由实验现象所得结论正确的是
| A.向H2S气体中通入SO2气体,瓶壁上产生淡黄色固体,证明SO2具有氧化性 |
| B.压缩二氧化氮气体时,气体颜色加深,证明加压时N2O4与NO2的混合气体中NO2的含量增大 |
| C.向Fe(NO3)2溶液中滴加稀硫酸,溶液变为黄色,证明稀硫酸可将Fe2+氧化为Fe3+ |
| D.常温下,向铁质容器中注入浓硫酸,无明显现象,证明铁在常温下不与浓硫酸反应 |
您最近一年使用:0次
2021-12-25更新
|
300次组卷
|
5卷引用:重庆市2021-2022学年高三12月联考化学试题
重庆市2021-2022学年高三12月联考化学试题河北省保定市2021-2022学年高三上学期期末考试化学试题(已下线)卷04 元素及其化合物-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)河北省唐山市开滦第一中学2022-2023学年高三上学期期末考试化学试题课时3影响化学平衡的因素随堂练习
名校
2 . 2021年6月17日,搭载神舟十二号载人飞般的长征二号F遥十二运载火箭,在酒泉卫星发射中
心发射。该运载火箭推进物分为偏二甲基肼( )、四氧化二氮和液氢、液氧。
)、四氧化二氮和液氢、液氧。
(1)3.0g液态偏二甲基肼与足量液态四氧化二氮完全反应生成 、
、 和
和 ,放出112.5kJ的热量,写出上述反应的热化学方程式
,放出112.5kJ的热量,写出上述反应的热化学方程式___________ 。
(2)对 和
和 反应的说法正确的是___________。
反应的说法正确的是___________。
(3)飞船在发射前,运载火箭要加注燃料,火箭的周围常常会看到淡淡的黄色烟雾。这是由于燃料推进时,需要减压排出部分 。无色的
。无色的 可分解为红棕色的
可分解为红棕色的 。
。
①已知 和
和 的结构式分别是
的结构式分别是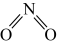 和
和 ,实验测得N-N的键能为167kJ/mol,
,实验测得N-N的键能为167kJ/mol, 中氮氧键(
中氮氧键( )的键能为466kJ/mol,
)的键能为466kJ/mol, 中氮氧键(
中氮氧键( )的键能为438.5kJ/mol;
)的键能为438.5kJ/mol; 转化为
转化为 的
的
___________ 。
②将一定量的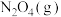 充入注射器中后封口,如图是在拉伸或压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小)。下列说法确的是
充入注射器中后封口,如图是在拉伸或压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小)。下列说法确的是___________ 。
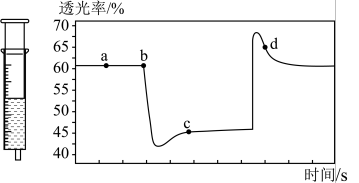
A.d点:
B.b点的操作是压缩注射器
C.c点与a点相比, 增大,
增大,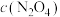 减小
减小
D.若不忽略体系温度变化,且没有能量损失,则b、c两点的平衡常数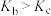
③反应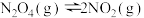 ,一定条件下
,一定条件下 与
与 的消耗速率与自身压强间存在:
的消耗速率与自身压强间存在: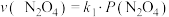 ,
,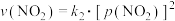 。其中
。其中 、
、 是与反应及温度有关的常数。一定温度下,
是与反应及温度有关的常数。一定温度下, 、
、 与平衡常数
与平衡常数 的关系是
的关系是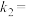
___________ 。(对于气相反应,用某组分B的平衡压强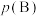 代替物质的量浓度
代替物质的量浓度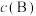 也可表示平衡常数,记作
也可表示平衡常数,记作 )
)
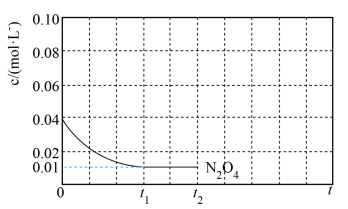
④反应温度 时,
时,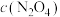 随t(时间)变化曲线如图1,画出
随t(时间)变化曲线如图1,画出 时段,
时段, 随t变化曲线。保持其它条件不变,改变反应温度为
随t变化曲线。保持其它条件不变,改变反应温度为 (
( ),再次画出
),再次画出 时段,
时段, 随t变化趋势的曲线。
随t变化趋势的曲线。_________
心发射。该运载火箭推进物分为偏二甲基肼(
 )、四氧化二氮和液氢、液氧。
)、四氧化二氮和液氢、液氧。(1)3.0g液态偏二甲基肼与足量液态四氧化二氮完全反应生成
 、
、 和
和 ,放出112.5kJ的热量,写出上述反应的热化学方程式
,放出112.5kJ的热量,写出上述反应的热化学方程式(2)对
 和
和 反应的说法正确的是___________。
反应的说法正确的是___________。| A.偏二甲肼是比液氢更环保的燃料 | B. 既是氧化产物,又是还原产物 既是氧化产物,又是还原产物 |
| C.偏二甲基肼的燃烧热为2250kJ/mol | D.该反应是一个熵增的自发反应 |
 。无色的
。无色的 可分解为红棕色的
可分解为红棕色的 。
。①已知
 和
和 的结构式分别是
的结构式分别是 和
和 ,实验测得N-N的键能为167kJ/mol,
,实验测得N-N的键能为167kJ/mol, 中氮氧键(
中氮氧键( )的键能为466kJ/mol,
)的键能为466kJ/mol, 中氮氧键(
中氮氧键( )的键能为438.5kJ/mol;
)的键能为438.5kJ/mol; 转化为
转化为 的
的
②将一定量的
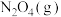 充入注射器中后封口,如图是在拉伸或压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小)。下列说法确的是
充入注射器中后封口,如图是在拉伸或压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小)。下列说法确的是
A.d点:

B.b点的操作是压缩注射器
C.c点与a点相比,
 增大,
增大,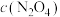 减小
减小D.若不忽略体系温度变化,且没有能量损失,则b、c两点的平衡常数
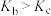
③反应
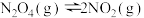 ,一定条件下
,一定条件下 与
与 的消耗速率与自身压强间存在:
的消耗速率与自身压强间存在: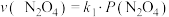 ,
,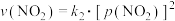 。其中
。其中 、
、 是与反应及温度有关的常数。一定温度下,
是与反应及温度有关的常数。一定温度下, 、
、 与平衡常数
与平衡常数 的关系是
的关系是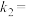
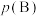 代替物质的量浓度
代替物质的量浓度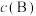 也可表示平衡常数,记作
也可表示平衡常数,记作 )
)④反应温度
 时,
时,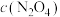 随t(时间)变化曲线如图1,画出
随t(时间)变化曲线如图1,画出 时段,
时段, 随t变化曲线。保持其它条件不变,改变反应温度为
随t变化曲线。保持其它条件不变,改变反应温度为 (
( ),再次画出
),再次画出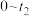 时段,
时段, 随t变化趋势的曲线。
随t变化趋势的曲线。
您最近一年使用:0次
3 . 利用合成气(主要成分为CO、CO2和H2)制备甲醇的主要反应有
①CO(g) +2H2(g) CH3OH(g) ΔH1 =-116 kJ/mol
CH3OH(g) ΔH1 =-116 kJ/mol
②CO2(g)+ H2(g) CO(g)+ H2O(g) ΔH2=+41.2 kJ/mol
CO(g)+ H2O(g) ΔH2=+41.2 kJ/mol
向一固定体积的容器中充入合成气,已知起始时c(CO)=0.1 mol/L、c(H2)=0.3 mol/L,平衡时c(CO)=0.05 mol/L,c(H2O)=0.02 mol/L,则下列说法错误的是
①CO(g) +2H2(g)
 CH3OH(g) ΔH1 =-116 kJ/mol
CH3OH(g) ΔH1 =-116 kJ/mol②CO2(g)+ H2(g)
 CO(g)+ H2O(g) ΔH2=+41.2 kJ/mol
CO(g)+ H2O(g) ΔH2=+41.2 kJ/mol向一固定体积的容器中充入合成气,已知起始时c(CO)=0.1 mol/L、c(H2)=0.3 mol/L,平衡时c(CO)=0.05 mol/L,c(H2O)=0.02 mol/L,则下列说法错误的是
| A.增大CO2的浓度,有利于提高甲醇的产量 |
| B.升高温度,①和②反应速率都加快 |
| C.压缩体积,反应②平衡不移动 |
| D.平衡时c(CH3OH)为0.07 mol/L |
您最近一年使用:0次
2021-12-03更新
|
175次组卷
|
2卷引用:河北省百师联盟2022届高三上学期一轮复习联考(三)化学试题
名校
4 . 利用 CO2与丙烷反应生成丙烯和水蒸气的反应机理如图所示。下列说法错误的是


| A.C3H8是还原剂 | B.CrO3作催化剂 |
| C.Cr2O3是反应的中间体 | D.增大压强有利于提高 CO2的转化率 |
您最近一年使用:0次
2021-10-11更新
|
491次组卷
|
4卷引用:广东省深圳市第七高级中学2022届高三上学期9月月考化学试题
广东省深圳市第七高级中学2022届高三上学期9月月考化学试题广东省深圳市第七高级中学2022届高三第二次月考化学试题山西省长治市上党区一中2021-2022学年高二上学期10月月考化学试题(已下线)专题09 反应机理—2022年高考化学二轮复习讲练测(全国版)-讲义
名校
5 . 工业上利用C和H2O(g)来制造水煤气,可以进一步制造重要的工业原料甲醇。现有10molC(s)和5molH2O(g)在一定条件下发生反应:C(s)+H2O(g) CO(g)+H2(g)。已知反应容器容积为1L,经过10s后测得生成2molH2(g),则下列说法不正确的是
CO(g)+H2(g)。已知反应容器容积为1L,经过10s后测得生成2molH2(g),则下列说法不正确的是
 CO(g)+H2(g)。已知反应容器容积为1L,经过10s后测得生成2molH2(g),则下列说法不正确的是
CO(g)+H2(g)。已知反应容器容积为1L,经过10s后测得生成2molH2(g),则下列说法不正确的是| A.再加入1molH2O(g),平衡时H2O(g)的转化率减小 |
| B.v[C(s)]=0.2mol·L-1·s-1 |
| C.水蒸气的转化率为40% |
| D.反应生成了2molCO |
您最近一年使用:0次
名校
6 . NO2与N2O4能相互转化,热化学方程式为N2O4(g)⇌2NO2(g)ΔH=57kJ·mol-1,下列有关说法正确的是
| A.升高体系温度正反应速率增大,逆反应速率也增大 |
| B.若容器体积不变,气体密度不变时说明该反应建立化学平衡 |
C.其它条件不变,向平衡后的容器中再加入少量N2O4, 的值变大 的值变大 |
| D.增大体系的压强能提高N2O4的反应速率和转化率 |
您最近一年使用:0次
名校
7 . T1时,在1L恒容密闭容器中充入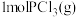 和
和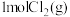 ,发生反应:
,发生反应: ,
, ,达平衡时升温至T2,实验测得:
,达平衡时升温至T2,实验测得: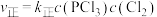 、
、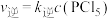 ,
, ,
, 为速率常数,只与温度有关。下列说法不正确的是
为速率常数,只与温度有关。下列说法不正确的是
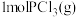 和
和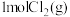 ,发生反应:
,发生反应: ,
, ,达平衡时升温至T2,实验测得:
,达平衡时升温至T2,实验测得: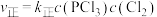 、
、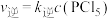 ,
, ,
, 为速率常数,只与温度有关。下列说法不正确的是
为速率常数,只与温度有关。下列说法不正确的是A.当 且不变时,该反应达到平衡状态 且不变时,该反应达到平衡状态 |
B.该反应的平衡常数可表示为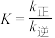 , ,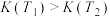 |
C.向T1温度下的平衡体系再充入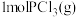 ,平衡正向移动,产物 ,平衡正向移动,产物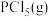 的体积分数变大 的体积分数变大 |
D.T1时,在一恒压密闭容器中充入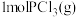 和 和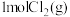 ,发生上述反应, ,发生上述反应, 的转化率变大 的转化率变大 |
您最近一年使用:0次
2023-08-23更新
|
468次组卷
|
4卷引用:云南省保山市2020-2021学年高二下学期期末考试化学试题
名校
解题方法
8 . 一定条件下恒温恒容的装置中,固体A和气体B可以反应生成气体C,反应过程中各物质的物质的量随时间的变化如图所示。下列关于该反应的说法正确的是
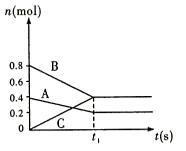

| A.若t1时刻是40s,用B表示该反应的0~t1时段的速率为0.01mol/(L·s) |
| B.t1时刻后,压缩该容器的体积增大压强,C的物质的量增多 |
| C.t1时刻后,再加入1molB,再次达到平衡后C的物质的量为0.9mol |
D.t1时刻后,升高体系的温度,容器内气体的密度减小,该反应的 |
您最近一年使用:0次
2021-11-06更新
|
144次组卷
|
3卷引用:湘豫名校2021-2022学年高三上学期联考(11月)化学试题
名校
9 . 可逆反应2SO2+O2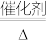 2SO3 △H<0,开始把2molSO2和1molO2充入容积为2L的恒容密闭容器中,在500℃条件下达化学平衡,下列说法中正确的是
2SO3 △H<0,开始把2molSO2和1molO2充入容积为2L的恒容密闭容器中,在500℃条件下达化学平衡,下列说法中正确的是
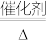 2SO3 △H<0,开始把2molSO2和1molO2充入容积为2L的恒容密闭容器中,在500℃条件下达化学平衡,下列说法中正确的是
2SO3 △H<0,开始把2molSO2和1molO2充入容积为2L的恒容密闭容器中,在500℃条件下达化学平衡,下列说法中正确的是| A.升高温度平衡向正反应方向移动 |
| B.增大压强SO2的转化率增大 |
| C.加入催化剂平衡不发生移动,但反应速率加快 |
| D.只增大SO2浓度平衡不移动 |
您最近一年使用:0次
名校
解题方法
10 . 通过下列反应合成CO和CH4,可实现CO2的再转化:
①CO2(g)+4H2(g) CH4(g)+2H2O(g) △H<0
CH4(g)+2H2O(g) △H<0
②CO2(g)+H2(g) CO(g)+H2O(g) △H>0
CO(g)+H2O(g) △H>0
在密闭容器中通入3 mol的H2和1 mol的CO2,分别在压强为1 MPa 和10 MPa下进行反应。实验中对平衡体系的三种物质(CO2、CO、CH4)进行分析,其中温度对CO和CH4在三种物质中的体积分数影响如图所示。
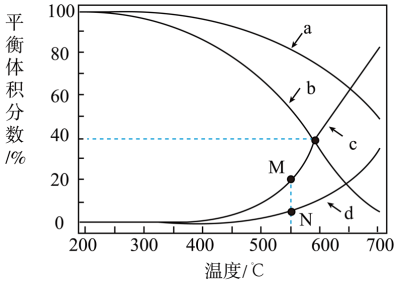
下列说法不正确的是
①CO2(g)+4H2(g)
 CH4(g)+2H2O(g) △H<0
CH4(g)+2H2O(g) △H<0②CO2(g)+H2(g)
 CO(g)+H2O(g) △H>0
CO(g)+H2O(g) △H>0在密闭容器中通入3 mol的H2和1 mol的CO2,分别在压强为1 MPa 和10 MPa下进行反应。实验中对平衡体系的三种物质(CO2、CO、CH4)进行分析,其中温度对CO和CH4在三种物质中的体积分数影响如图所示。

下列说法不正确的是
| A.曲线a表示10 MPa条件下CH4的体积分数随温度的变化 |
| B.曲线a、d交点纵坐标可能为40% |
| C.550°C时M点位于N点上方是由于压强降低时,平衡①逆向移动导致平衡②正向移动 |
| D.由曲线b、c的交点可计算该温度下反应②的平衡常数为2.4 |
您最近一年使用:0次
2022-09-02更新
|
211次组卷
|
2卷引用:江苏省南师附中、天一中学、海安中学、海门中学四校2021-2022学年高三12月联考化学试题



