名校
1 . γ-丁内酯(BL)广泛应用于医药、染料等领域。
Ⅰ.γ-羟基丁酸发生酯化反应合成BL。_______ 。
(2)已知:②
 。平衡常数K与ΔG关系为
。平衡常数K与ΔG关系为 (R为气体常数,T为温度),ΔH1和ΔH2近似相等,但是在相同条件下,反应①的限度显著大于反应②,其原因是
(R为气体常数,T为温度),ΔH1和ΔH2近似相等,但是在相同条件下,反应①的限度显著大于反应②,其原因是_______ 。
(3)298K下,水溶液中物质浓度随时间变化如图所示。_______ ,为了提高平衡转化率,除改变温度外,还可以采取的措施有_______ 。
②298K时,该反应的平衡常数K为_______ 。
Ⅱ.1,4-丁二醇(BD)脱氢法合成BL。有关反应如下: 。
。
(4)在493K,3.0×103kPa的高压H2氛围下,分别以0.01mol BD或BL为初始原料,在密闭容器中进行反应。达到平衡时,以BD为原料,体系从环境吸收a kJ热量;以BL为原料,体系向环境放出b kJ热量。忽略ⅱ、ⅲ反应的热效应。在此条件下,ⅰ反应的ΔH(493K,3.0×103kPa)=_______ kJ·mol-1。
(5)在标准大气压下,选择CuO/ZnO/Al2O3作催化剂,氢醇比 为5,分别探究温度和流速(BD和H2通过催化剂表面的速率)对三种产物选择性的影响,所得关系曲线如图2和图3所示。
为5,分别探究温度和流速(BD和H2通过催化剂表面的速率)对三种产物选择性的影响,所得关系曲线如图2和图3所示。
(6)在体积固定的刚性容器中充入5.0×10-3mol BL,在493K、3.0×103kPa条件下,在高压H2氛围中反应生成BD(伴随反应ⅱ和ⅲ)。已知:物质的量分数(xa)表示体系中物质a的物质的量与除H2外所有物质的物质的量总和之比。该条件下达到平衡时, ,
,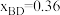 ,则
,则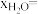
_______ 。
Ⅰ.γ-羟基丁酸发生酯化反应合成BL。
①
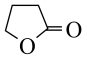

 ΔH1。
ΔH1。
(2)已知:②

 。平衡常数K与ΔG关系为
。平衡常数K与ΔG关系为 (R为气体常数,T为温度),ΔH1和ΔH2近似相等,但是在相同条件下,反应①的限度显著大于反应②,其原因是
(R为气体常数,T为温度),ΔH1和ΔH2近似相等,但是在相同条件下,反应①的限度显著大于反应②,其原因是(3)298K下,水溶液中物质浓度随时间变化如图所示。

②298K时,该反应的平衡常数K为
Ⅱ.1,4-丁二醇(BD)脱氢法合成BL。有关反应如下:
ⅰ.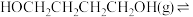

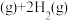 ;
;
ⅱ.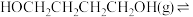
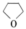
 ;
;
 。
。(4)在493K,3.0×103kPa的高压H2氛围下,分别以0.01mol BD或BL为初始原料,在密闭容器中进行反应。达到平衡时,以BD为原料,体系从环境吸收a kJ热量;以BL为原料,体系向环境放出b kJ热量。忽略ⅱ、ⅲ反应的热效应。在此条件下,ⅰ反应的ΔH(493K,3.0×103kPa)=
(5)在标准大气压下,选择CuO/ZnO/Al2O3作催化剂,氢醇比
 为5,分别探究温度和流速(BD和H2通过催化剂表面的速率)对三种产物选择性的影响,所得关系曲线如图2和图3所示。
为5,分别探究温度和流速(BD和H2通过催化剂表面的速率)对三种产物选择性的影响,所得关系曲线如图2和图3所示。
| A.题给条件下,制备BL反应的最优温度为320℃,最优流速为1.6 L·min-1 |
| B.流速较小时,发生副反应导致BL选择性不高 |
| C.280℃后,温度升高,BL的选择性降低的原因可能是催化剂活性降低 |
| D.实际工业生产时流速选择2.0 L·min-1的原因是所得BL产品杂质含量少 |
(6)在体积固定的刚性容器中充入5.0×10-3mol BL,在493K、3.0×103kPa条件下,在高压H2氛围中反应生成BD(伴随反应ⅱ和ⅲ)。已知:物质的量分数(xa)表示体系中物质a的物质的量与除H2外所有物质的物质的量总和之比。该条件下达到平衡时,
 ,
,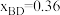 ,则
,则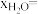
您最近一年使用:0次
2 . 1,2-二甲基环丙烷的顺反异构体可相互转化:
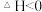 。该反应的速率方程为:
。该反应的速率方程为: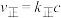 (顺式),
(顺式), (反式),
(反式), 和
和 分别为正、逆反应速率常数。
分别为正、逆反应速率常数。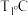 时,加入顺式异构体发生反应,两种异构体的质量分数
时,加入顺式异构体发生反应,两种异构体的质量分数 随时间
随时间 的变化如图所示。下列说法正确的是
的变化如图所示。下列说法正确的是

A.反应速率: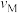 (正) (正)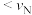 (逆) (逆) |
B.反应在 点达到平衡 点达到平衡 |
| C.升高温度,k正减小,k逆增大,所以k正<k逆 |
D. 时发生反应,测得 时发生反应,测得 ,则 ,则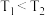 |
您最近一年使用:0次
名校
3 . 丙烯是重要的有机原料之一,可通过多种途径制备。回答下列问题:
Ⅰ.由丙烷直接脱氢法制备: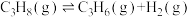

(1)已知键能: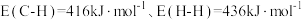 ;生成
;生成 碳碳
碳碳 键放出的能量为
键放出的能量为 ,则
,则
________  。
。
(2)在一定温度下,保持总压为 ,将
,将 和
和 的混合气体分别按
的混合气体分别按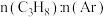 为
为 和
和 向密闭容器中投料,发生脱氢反应,测得
向密闭容器中投料,发生脱氢反应,测得 的转化率与时间的关系如图1所示(已知
的转化率与时间的关系如图1所示(已知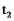 时反应处于平衡状态)。m点对应的投料方式为
时反应处于平衡状态)。m点对应的投料方式为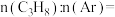
____ ,原因是_______________ 。 内,曲线
内,曲线_________ (填“ ”“
”“ ”)对应的平均反应速率最快。n点对应的平衡常数
”)对应的平均反应速率最快。n点对应的平衡常数
_____  (以分压表示,分压=总压×物质的量分数,保留一位小数)。
(以分压表示,分压=总压×物质的量分数,保留一位小数)。 ;
;
(3)在一定条件下,将物质的量之比为 的
的 和
和 匀速通入体积可变的反应容器中发生上述反应,使总压强恒定为
匀速通入体积可变的反应容器中发生上述反应,使总压强恒定为 。在不同温度下反应相同时间,测得丙烷和氧气的转化率与温度倒数
。在不同温度下反应相同时间,测得丙烷和氧气的转化率与温度倒数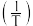 的关系如图2所示。
的关系如图2所示。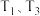 对应的点均处于平衡状态,保持其他条件不变,仅将容器更换为恒容的刚性容器,则图示点
对应的点均处于平衡状态,保持其他条件不变,仅将容器更换为恒容的刚性容器,则图示点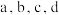 中,
中, 与
与 新的转化率点可能依次是
新的转化率点可能依次是________ (填代号);M点丙烷的分压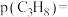
________  (保留两位有效数字)。
(保留两位有效数字)。
Ⅰ.由丙烷直接脱氢法制备:
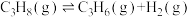

(1)已知键能:
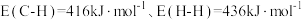 ;生成
;生成 碳碳
碳碳 键放出的能量为
键放出的能量为 ,则
,则
 。
。(2)在一定温度下,保持总压为
 ,将
,将 和
和 的混合气体分别按
的混合气体分别按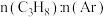 为
为 和
和 向密闭容器中投料,发生脱氢反应,测得
向密闭容器中投料,发生脱氢反应,测得 的转化率与时间的关系如图1所示(已知
的转化率与时间的关系如图1所示(已知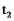 时反应处于平衡状态)。m点对应的投料方式为
时反应处于平衡状态)。m点对应的投料方式为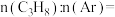
 内,曲线
内,曲线 ”“
”“ ”)对应的平均反应速率最快。n点对应的平衡常数
”)对应的平均反应速率最快。n点对应的平衡常数
 (以分压表示,分压=总压×物质的量分数,保留一位小数)。
(以分压表示,分压=总压×物质的量分数,保留一位小数)。
 ;
;
(3)在一定条件下,将物质的量之比为
 的
的 和
和 匀速通入体积可变的反应容器中发生上述反应,使总压强恒定为
匀速通入体积可变的反应容器中发生上述反应,使总压强恒定为 。在不同温度下反应相同时间,测得丙烷和氧气的转化率与温度倒数
。在不同温度下反应相同时间,测得丙烷和氧气的转化率与温度倒数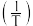 的关系如图2所示。
的关系如图2所示。
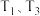 对应的点均处于平衡状态,保持其他条件不变,仅将容器更换为恒容的刚性容器,则图示点
对应的点均处于平衡状态,保持其他条件不变,仅将容器更换为恒容的刚性容器,则图示点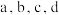 中,
中, 与
与 新的转化率点可能依次是
新的转化率点可能依次是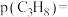
 (保留两位有效数字)。
(保留两位有效数字)。
您最近一年使用:0次
名校
4 . 烯烃是一种应用广泛的化学原料。烯烃之间存在下列三个反应:
反应Ⅰ:

反应Ⅱ:
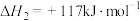
反应Ⅲ: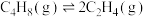

在压强为pkPa的恒压密闭容器中,反应达到平衡时,三种组分的物质的量分数x随温度T的变化关系如图所示。
反应Ⅰ:


反应Ⅱ:

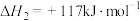
反应Ⅲ:

在压强为pkPa的恒压密闭容器中,反应达到平衡时,三种组分的物质的量分数x随温度T的变化关系如图所示。
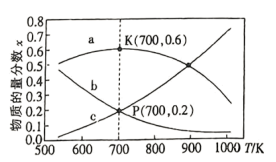
A.反应Ⅲ的 |
B.700K时反应Ⅱ的平衡常数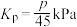 |
C.欲提高 的物质的量分数,需研发低温条件下活性好且耐高压的催化剂 的物质的量分数,需研发低温条件下活性好且耐高压的催化剂 |
| D.超过700K后曲线a下降的原因可能是随着温度升高反应Ⅰ逆向移动,反应Ⅱ正向移动 |
您最近一年使用:0次
2024-06-02更新
|
131次组卷
|
2卷引用:江西省九校联考2023-2024学年高三下学期3月月考化学试题
名校
解题方法
5 . T℃时,向2L的恒容密闭容器中加入 和
和 共5mol发生反应
共5mol发生反应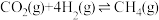
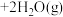 ,下图为
,下图为 和
和 按不同投料比反应达平衡时的相关数据,其中曲线a、b表示反应物转化率,曲线c表示
按不同投料比反应达平衡时的相关数据,其中曲线a、b表示反应物转化率,曲线c表示 的体积分数,下列分析
的体积分数,下列分析不正确 的是
 和
和 共5mol发生反应
共5mol发生反应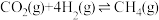
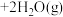 ,下图为
,下图为 和
和 按不同投料比反应达平衡时的相关数据,其中曲线a、b表示反应物转化率,曲线c表示
按不同投料比反应达平衡时的相关数据,其中曲线a、b表示反应物转化率,曲线c表示 的体积分数,下列分析
的体积分数,下列分析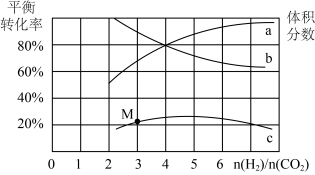
A.曲线a表示 的平衡转化率 的平衡转化率 | B.当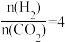 ,平衡时 ,平衡时 体积分数最大 体积分数最大 |
| C.T℃时,该反应的平衡常数为25 | D.M点对应的 的体积分数小于23.5% 的体积分数小于23.5% |
您最近一年使用:0次
6 . 丙烷脱氢制备丙烯已成为制备丙烯的重要方法之一。
已知:一定温度下,由元素的最稳定的单质生成1mol纯物质的热效应称为该物质的摩尔生成焓。
回答下列问题:
(1)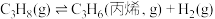 的
的
___________  ,该反应在
,该反应在___________ (填“高温”“低温”或“任意温度”)下能自发。
(2)维持体系总压强恒定为0.1MPa,加入1mol 时,再加入nmol水蒸气作为稀释剂,测得丙烷平衡转化率与温度的关系如图所示,已知:水烃比是指投料中水蒸气和丙烷的物质的量之比。
时,再加入nmol水蒸气作为稀释剂,测得丙烷平衡转化率与温度的关系如图所示,已知:水烃比是指投料中水蒸气和丙烷的物质的量之比。

①温度为800K,反应经tmin后达到平衡,0~tmin内, 的分压平均变化率为
的分压平均变化率为___________  。
。
②800K下反应的平衡常数
___________ MPa。(用气体分压计算平衡常数,气体分压 气体总压
气体总压 气体的物质的量分数)
气体的物质的量分数)
③0.1MPa下,在图中画出水烃比为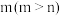 时的曲线
时的曲线___________ 。
④若其他条件不变,将nmol水蒸气改为nmol [此时有副反应
[此时有副反应 ],则丙烷的平衡转化率将大大增加,请解释原因:
],则丙烷的平衡转化率将大大增加,请解释原因:___________ 。
(3)恒温、体积可变的密闭容器中投入丙烷发生反应,某压强下反应一定时间,测量丙烷的转化率。然后保持其他初始实验条件不变,分别在不同压强下,重复上述实验,经过相同时间测得丙烷的转化率随压强变化的趋势图不可能是___________(填标号)。
已知:一定温度下,由元素的最稳定的单质生成1mol纯物质的热效应称为该物质的摩尔生成焓。
| 气态物质 |  |  (丙烯) (丙烯) |  |
摩尔生成焓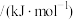 | 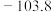 | 20.4 | 0 |
(1)
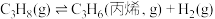 的
的
 ,该反应在
,该反应在(2)维持体系总压强恒定为0.1MPa,加入1mol
 时,再加入nmol水蒸气作为稀释剂,测得丙烷平衡转化率与温度的关系如图所示,已知:水烃比是指投料中水蒸气和丙烷的物质的量之比。
时,再加入nmol水蒸气作为稀释剂,测得丙烷平衡转化率与温度的关系如图所示,已知:水烃比是指投料中水蒸气和丙烷的物质的量之比。
①温度为800K,反应经tmin后达到平衡,0~tmin内,
 的分压平均变化率为
的分压平均变化率为 。
。②800K下反应的平衡常数

 气体总压
气体总压 气体的物质的量分数)
气体的物质的量分数)③0.1MPa下,在图中画出水烃比为
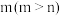 时的曲线
时的曲线④若其他条件不变,将nmol水蒸气改为nmol
 [此时有副反应
[此时有副反应 ],则丙烷的平衡转化率将大大增加,请解释原因:
],则丙烷的平衡转化率将大大增加,请解释原因:(3)恒温、体积可变的密闭容器中投入丙烷发生反应,某压强下反应一定时间,测量丙烷的转化率。然后保持其他初始实验条件不变,分别在不同压强下,重复上述实验,经过相同时间测得丙烷的转化率随压强变化的趋势图不可能是___________(填标号)。
A.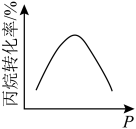 | B. 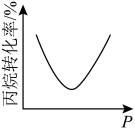 |
C. 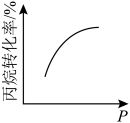 | D. |
您最近一年使用:0次
解题方法
7 . 碘单质及其化合物在生产、生活中有广泛应用。回答下列问题:
(1)已知几种共价键键能数据如图所示。

__________  。
。
(2)NH4I分解温度为235℃,HI分解温度为300℃。
①卤化铵分解与产物稳定性有关,产物越稳定,卤化铵(NH4X)越容易分解。NH4I、NH4Br、NH4Cl、NH4F的热分解温度由高到低排序为_____________ 。
②某温度下,在恒容密闭容器中加入适量的NH4I(s),仅发生下列反应:反应Ⅰ: ;反应Ⅱ:
;反应Ⅱ: 。随着反应的进行,产物物质的量随时间的变化曲线如图所示。
。随着反应的进行,产物物质的量随时间的变化曲线如图所示。__________ (填“甲”“乙”或“丙”)代表 物质的量随时间变化曲线;该温度下,反应Ⅱ的平衡常数
物质的量随时间变化曲线;该温度下,反应Ⅱ的平衡常数
__________ 。
ⅱ.进一步研究发现,其他条件不变,升高温度时甲曲线平台下移,其可能的原因是_____________ (写出化学方程式)。
(3)1925年VanArkn和DeBoer发明了碘化钛热分解法制备高纯钛。装置如图所示:
 ;
;
副反应: ,
, 。
。
①主反应中
__________ 0(填“>”“<”或“=”),简述提纯钛的原理:_____________ 。
②钛沉积速率与钛丝温度关系如图所示。温度高1500℃时,钛沉积速率降低的主要原因可能是______________ 。
(1)已知几种共价键键能数据如图所示。

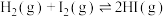

 。
。(2)NH4I分解温度为235℃,HI分解温度为300℃。
①卤化铵分解与产物稳定性有关,产物越稳定,卤化铵(NH4X)越容易分解。NH4I、NH4Br、NH4Cl、NH4F的热分解温度由高到低排序为
②某温度下,在恒容密闭容器中加入适量的NH4I(s),仅发生下列反应:反应Ⅰ:
 ;反应Ⅱ:
;反应Ⅱ: 。随着反应的进行,产物物质的量随时间的变化曲线如图所示。
。随着反应的进行,产物物质的量随时间的变化曲线如图所示。
 物质的量随时间变化曲线;该温度下,反应Ⅱ的平衡常数
物质的量随时间变化曲线;该温度下,反应Ⅱ的平衡常数
ⅱ.进一步研究发现,其他条件不变,升高温度时甲曲线平台下移,其可能的原因是
(3)1925年VanArkn和DeBoer发明了碘化钛热分解法制备高纯钛。装置如图所示:


 ;
;副反应:
 ,
, 。
。①主反应中

②钛沉积速率与钛丝温度关系如图所示。温度高1500℃时,钛沉积速率降低的主要原因可能是

您最近一年使用:0次
8 . 在容积为1L的密闭容器中,以Ag-ZSM为催化剂,相同时间测得0.1mol NO转化为 的转化率随温度变化如图所示[有CO时反应为
的转化率随温度变化如图所示[有CO时反应为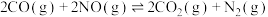 ;无CO时反应为
;无CO时反应为
 ](忽略温度对催化剂活性的影响)。下列说法正确的是
](忽略温度对催化剂活性的影响)。下列说法正确的是
 的转化率随温度变化如图所示[有CO时反应为
的转化率随温度变化如图所示[有CO时反应为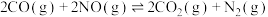 ;无CO时反应为
;无CO时反应为
 ](忽略温度对催化剂活性的影响)。下列说法正确的是
](忽略温度对催化剂活性的影响)。下列说法正确的是
| A.X点若更换高效催化剂NO转化率不变 |
B.Y点再通入CO、 各0.01mol,此时 各0.01mol,此时 |
C.反应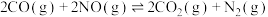 的△H>0 的△H>0 |
D.达平衡后,其他条件不变,使 ,NO转化率增大 ,NO转化率增大 |
您最近一年使用:0次
名校
9 . 甲烷水蒸气重整制合成气[
 ]是利用甲烷资源的途径之一、其他条件相同时,在不同催化剂(
]是利用甲烷资源的途径之一、其他条件相同时,在不同催化剂( 、
、 、
、 )作用下,反应相同时间后,
)作用下,反应相同时间后, 的转化率随反应温度的变化如下图所示。下列说法错误的是
的转化率随反应温度的变化如下图所示。下列说法错误的是

 ]是利用甲烷资源的途径之一、其他条件相同时,在不同催化剂(
]是利用甲烷资源的途径之一、其他条件相同时,在不同催化剂( 、
、 、
、 )作用下,反应相同时间后,
)作用下,反应相同时间后, 的转化率随反应温度的变化如下图所示。下列说法错误的是
的转化率随反应温度的变化如下图所示。下列说法错误的是
A.该反应 | B.平衡常数: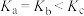 |
C.催化剂催化效率: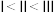 | D.增大压强, 增大倍数小于 增大倍数小于 增大倍数 增大倍数 |
您最近一年使用:0次
名校
10 . 将 转化为
转化为 的反应有:I.无
的反应有:I.无 时,
时, ;
;
Ⅱ.有 时,
时, 。
。
向 密闭容器甲中通入
密闭容器甲中通入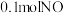 ,向
,向 密闭容器乙中通入
密闭容器乙中通入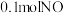 和
和 ,相同时间内测得
,相同时间内测得 的转化率随温度变化如图所示。下列说法正确的是
的转化率随温度变化如图所示。下列说法正确的是
 转化为
转化为 的反应有:I.无
的反应有:I.无 时,
时, ;
;Ⅱ.有
 时,
时, 。
。向
 密闭容器甲中通入
密闭容器甲中通入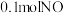 ,向
,向 密闭容器乙中通入
密闭容器乙中通入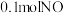 和
和 ,相同时间内测得
,相同时间内测得 的转化率随温度变化如图所示。下列说法正确的是
的转化率随温度变化如图所示。下列说法正确的是
A.相同条件下,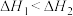 |
B.Y点处,反应I在此温度下, ( ( 为压强平衡常数,分压=总压 为压强平衡常数,分压=总压 物质的量分数) 物质的量分数) |
| C.X点处,反应I、Ⅱ的正反应速率一定相等 |
D.容器甲中反应达平衡后,再通入 的平衡转化率增大 的平衡转化率增大 |
您最近一年使用:0次



