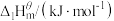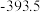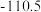解题方法
1 .  和
和 是两种常见的温室气体,利用
是两种常见的温室气体,利用 和
和 生成高附加值合成气CO和
生成高附加值合成气CO和 ,以及甲烷部分催化裂解制备乙烯是目前研究的热点之一。回答下列问题:
,以及甲烷部分催化裂解制备乙烯是目前研究的热点之一。回答下列问题:
(1)已知: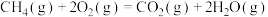
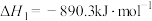 ;
;
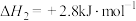 ;
;

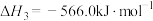 。
。
反应 的
的
________  ;对于该反应,有利于提高
;对于该反应,有利于提高 平衡转化率的条件是
平衡转化率的条件是________ (填字母)。
A.高温高压 B.高温低压 C.低温高压 D.低温低压
(2)CO常用于工业冶炼金属,如图是在不同温度下CO还原三种金属氧化物达平衡后气体中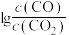 与温度(T)的关系曲线图。下列说法正确的是________(填字母)。
与温度(T)的关系曲线图。下列说法正确的是________(填字母)。
(3)甲烷部分催化裂解制备乙烯的反应原理为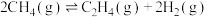
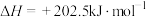 。温度为T℃,压强为100kPa时,向体积可变的密闭容器中加入
。温度为T℃,压强为100kPa时,向体积可变的密闭容器中加入 ,平衡时
,平衡时 转化率为40%,若温度、压强和
转化率为40%,若温度、压强和 初始量不变,充入
初始量不变,充入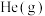 作为稀释气,平衡时
作为稀释气,平衡时 转化率为50%,则充入He的物质的量为
转化率为50%,则充入He的物质的量为________ mol。
(4)一定温度下,将 充入2L的固定容积容器中发生反应
充入2L的固定容积容器中发生反应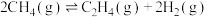
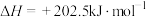 。实验测得容器内各气体分压与时间的关系如图所示。
。实验测得容器内各气体分压与时间的关系如图所示。 的平衡转化率为
的平衡转化率为________ 。
②反应的平衡常数
________ 。
③若在该温度下,向容器中再充入 ,达到平衡时,平衡混合物中
,达到平衡时,平衡混合物中 的物质的量分数
的物质的量分数________ (填“增大”“减小”或“不变”)。
 和
和 是两种常见的温室气体,利用
是两种常见的温室气体,利用 和
和 生成高附加值合成气CO和
生成高附加值合成气CO和 ,以及甲烷部分催化裂解制备乙烯是目前研究的热点之一。回答下列问题:
,以及甲烷部分催化裂解制备乙烯是目前研究的热点之一。回答下列问题:(1)已知:
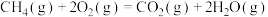
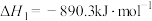 ;
;
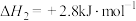 ;
;
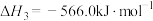 。
。反应
 的
的
 ;对于该反应,有利于提高
;对于该反应,有利于提高 平衡转化率的条件是
平衡转化率的条件是A.高温高压 B.高温低压 C.低温高压 D.低温低压
(2)CO常用于工业冶炼金属,如图是在不同温度下CO还原三种金属氧化物达平衡后气体中
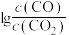 与温度(T)的关系曲线图。下列说法正确的是________(填字母)。
与温度(T)的关系曲线图。下列说法正确的是________(填字母)。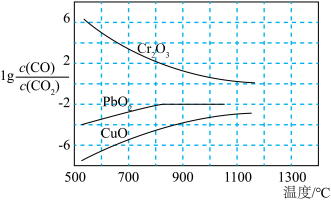
A.CO还原 的反应 的反应 |
| B.CO不适宜用于工业冶炼金属铬(Cr) |
| C.工业冶炼金属铜时较低的温度有利于提高CO的利用率 |
| D.工业上可以通过增高反应装置来延长矿石和CO接触的时间,减少尾气中CO的含量 |
(3)甲烷部分催化裂解制备乙烯的反应原理为
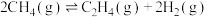
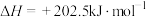 。温度为T℃,压强为100kPa时,向体积可变的密闭容器中加入
。温度为T℃,压强为100kPa时,向体积可变的密闭容器中加入 ,平衡时
,平衡时 转化率为40%,若温度、压强和
转化率为40%,若温度、压强和 初始量不变,充入
初始量不变,充入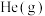 作为稀释气,平衡时
作为稀释气,平衡时 转化率为50%,则充入He的物质的量为
转化率为50%,则充入He的物质的量为(4)一定温度下,将
 充入2L的固定容积容器中发生反应
充入2L的固定容积容器中发生反应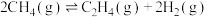
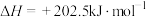 。实验测得容器内各气体分压与时间的关系如图所示。
。实验测得容器内各气体分压与时间的关系如图所示。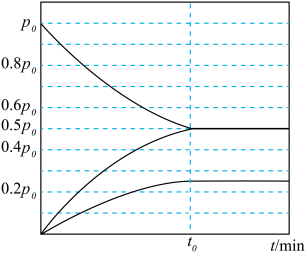
 的平衡转化率为
的平衡转化率为②反应的平衡常数

③若在该温度下,向容器中再充入
 ,达到平衡时,平衡混合物中
,达到平衡时,平衡混合物中 的物质的量分数
的物质的量分数
您最近一年使用:0次
2 . 利用 CO2 合成甲醇、二甲醚技术是有效利用 CO2 资源,实现“碳中和”目标的重要途径。
(1)开发 CO2 直接催化加氢合成二甲醚技术是很好的一个研究方向。
主反应:2CO2(g)+6H2(g) CH3OCH3(g)+3H2O(g)
CH3OCH3(g)+3H2O(g)  1=-122.54kJ•mol-1
1=-122.54kJ•mol-1
副反应:CO2(g)+H2(g) CO(g)+H2O(g)
CO(g)+H2O(g)  2
2
①已知 25℃和 101kPa 下,H2 (g)、CO(g)的燃烧热 H 分别为-285.8kJ•mol-1、-283.0kJ•mol-1,H2O(l)=H2O(g)
H 分别为-285.8kJ•mol-1、-283.0kJ•mol-1,H2O(l)=H2O(g)  H=+44kJ•mol-1,则
H=+44kJ•mol-1,则 H2=
H2=___________ kJ/mol。
②在催化剂作用下,向恒温恒压(250℃、3.0MPa)的密闭容器中充入反应气,n(CO):(CO2):n(H2)= 1:5:20,反应平衡时测得 CO2 的转化率为 20%,二甲醚的选择性为 80%(已知二甲醚的选择性=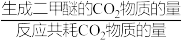 ×100%),则副反应CO2(g)+H2(g)
×100%),则副反应CO2(g)+H2(g) CO(g)+H2O(g)的Kp=
CO(g)+H2O(g)的Kp=___________ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(2)利用 CO2 合成甲醇也是有效利用 CO2 资源的重要途径。将原料气(CO2):n(H2)=1:3 充入某一恒容密闭容器中,只发生 CO2(g)+3H2(g) CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)  H3<0,在不同催化剂作用下,反应 t min 时 CO2 的转化率随温度的变化如图所示。
H3<0,在不同催化剂作用下,反应 t min 时 CO2 的转化率随温度的变化如图所示。___________ 。
A.使用催化剂 I 时,d 点已达到平衡
B.T3 K 的平衡常数大于 T4 K 的平衡常数
C.若 a 点时,v(H2)正 = 3v(CH3OH)逆,则此条件下反应已达到最大限度
D.c 点转化率比 a 点低的原因一定是催化剂活性降低
②若图中 a 点时反应已达平衡,现原料气按(CO2):n(H2)=1:2.8 充入同一恒容密闭容器中,在催化剂 I 的作用下发生反应。请在图中用实线画出了 T3K~T5K 之间 CO2 的平衡转化率变化曲线___________ 。
(3)水煤气变换反应的机理被广泛研究,其中有一种为羧基机理,某催化剂催化CO*+H2O* CO2*+H2(g) (*表示吸附态、Ea 表示活化能)步骤如下:
CO2*+H2(g) (*表示吸附态、Ea 表示活化能)步骤如下:
I.H2O*→OH*+H* Ea1=141.7kJ/mol
II.___________ Ea2=39.5kJ/mol
III.COOH*→CO2*+H* Ea3=132.1kJ/mol
IV.___________ Ea4=97.4kJ/mol
①请补充其中的一个反应式:II___________ 。
②反应CO*+H2O* CO2*+H2(g)的决速步骤是
CO2*+H2(g)的决速步骤是___________ (填序号)。
(4)一种新型 Zn-CO2 水介质电池,为解决环境和能源问题提供了一种新途径,其工作示意图如图所示,酸性条件下,正极电极反应式为___________ ;充电时阴极的电极反应式为___________ 。
(1)开发 CO2 直接催化加氢合成二甲醚技术是很好的一个研究方向。
主反应:2CO2(g)+6H2(g)
 CH3OCH3(g)+3H2O(g)
CH3OCH3(g)+3H2O(g)  1=-122.54kJ•mol-1
1=-122.54kJ•mol-1 副反应:CO2(g)+H2(g)
 CO(g)+H2O(g)
CO(g)+H2O(g)  2
2①已知 25℃和 101kPa 下,H2 (g)、CO(g)的燃烧热
 H 分别为-285.8kJ•mol-1、-283.0kJ•mol-1,H2O(l)=H2O(g)
H 分别为-285.8kJ•mol-1、-283.0kJ•mol-1,H2O(l)=H2O(g)  H=+44kJ•mol-1,则
H=+44kJ•mol-1,则 H2=
H2=②在催化剂作用下,向恒温恒压(250℃、3.0MPa)的密闭容器中充入反应气,n(CO):(CO2):n(H2)= 1:5:20,反应平衡时测得 CO2 的转化率为 20%,二甲醚的选择性为 80%(已知二甲醚的选择性=
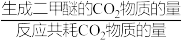 ×100%),则副反应CO2(g)+H2(g)
×100%),则副反应CO2(g)+H2(g) CO(g)+H2O(g)的Kp=
CO(g)+H2O(g)的Kp=(2)利用 CO2 合成甲醇也是有效利用 CO2 资源的重要途径。将原料气(CO2):n(H2)=1:3 充入某一恒容密闭容器中,只发生 CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)  H3<0,在不同催化剂作用下,反应 t min 时 CO2 的转化率随温度的变化如图所示。
H3<0,在不同催化剂作用下,反应 t min 时 CO2 的转化率随温度的变化如图所示。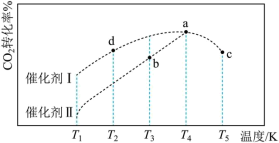
A.使用催化剂 I 时,d 点已达到平衡
B.T3 K 的平衡常数大于 T4 K 的平衡常数
C.若 a 点时,v(H2)正 = 3v(CH3OH)逆,则此条件下反应已达到最大限度
D.c 点转化率比 a 点低的原因一定是催化剂活性降低
②若图中 a 点时反应已达平衡,现原料气按(CO2):n(H2)=1:2.8 充入同一恒容密闭容器中,在催化剂 I 的作用下发生反应。请在图中用实线画出了 T3K~T5K 之间 CO2 的平衡转化率变化曲线
(3)水煤气变换反应的机理被广泛研究,其中有一种为羧基机理,某催化剂催化CO*+H2O*
 CO2*+H2(g) (*表示吸附态、Ea 表示活化能)步骤如下:
CO2*+H2(g) (*表示吸附态、Ea 表示活化能)步骤如下:I.H2O*→OH*+H* Ea1=141.7kJ/mol
II.___________ Ea2=39.5kJ/mol
III.COOH*→CO2*+H* Ea3=132.1kJ/mol
IV.___________ Ea4=97.4kJ/mol
①请补充其中的一个反应式:II
②反应CO*+H2O*
 CO2*+H2(g)的决速步骤是
CO2*+H2(g)的决速步骤是(4)一种新型 Zn-CO2 水介质电池,为解决环境和能源问题提供了一种新途径,其工作示意图如图所示,酸性条件下,正极电极反应式为

您最近一年使用:0次
3 . 氢能新质生产力正加速发展。工业上利用天然气制备氢气,还能得到乙烯、乙炔等化工产品,有关反应原理如下:
反应①:2CH4(g) C2H2(g)+3H2(g) ∆H1=+376.3kJ/mol K1;
C2H2(g)+3H2(g) ∆H1=+376.3kJ/mol K1;
反应②:2CH4(g) C2H4(g)+2H2(g) ∆H2=+202.0kJ/mol K2;
C2H4(g)+2H2(g) ∆H2=+202.0kJ/mol K2;
回答下列问题:
(1)反应③:C2H2(g)+2H2(g) C2H4(g) ∆H3=
C2H4(g) ∆H3=___________ kJ/mol,K3=___________ (用含K1、K2的代数式表示)。
(2)若用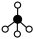 、
、 、
、 和
和 表示CH4、C2H2、H2和固体催化剂,如图在催化剂表面进行反应①,从吸附到解吸的过程中,能量状态最高的是
表示CH4、C2H2、H2和固体催化剂,如图在催化剂表面进行反应①,从吸附到解吸的过程中,能量状态最高的是___________ (填字母)。___________ T2(填“>”“<”或“=”)。
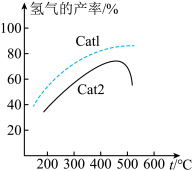
(4)向恒温恒容密闭容器中充入适量CH4,同时发生上述反应①和反应②,在不同催化剂Cat1、Cat2作用下,测得单位时间内H2的产率与温度的关系如图所示。在其他条件相同时,催化效率较高的是___________ (填“Cat1”或“Cat2”)。在Cat2作用下,温度高于500℃时,H2的产率迅速降低的原因是___________ 。 C2H2(g)+H2(g)制备氢气。
C2H2(g)+H2(g)制备氢气。
①实际操作中,往往向反应器中充入一定量的水蒸气,其目的是___________ 。
②忽略其他副反应,若向反应器中充入5mol水蒸气,平衡时(C2H4的转化率为75%,则该反应的Kp=___________ 。
反应①:2CH4(g)
 C2H2(g)+3H2(g) ∆H1=+376.3kJ/mol K1;
C2H2(g)+3H2(g) ∆H1=+376.3kJ/mol K1;反应②:2CH4(g)
 C2H4(g)+2H2(g) ∆H2=+202.0kJ/mol K2;
C2H4(g)+2H2(g) ∆H2=+202.0kJ/mol K2;回答下列问题:
(1)反应③:C2H2(g)+2H2(g)
 C2H4(g) ∆H3=
C2H4(g) ∆H3=(2)若用
 、
、 、
、 和
和 表示CH4、C2H2、H2和固体催化剂,如图在催化剂表面进行反应①,从吸附到解吸的过程中,能量状态最高的是
表示CH4、C2H2、H2和固体催化剂,如图在催化剂表面进行反应①,从吸附到解吸的过程中,能量状态最高的是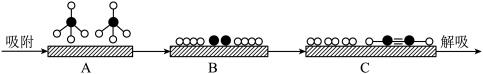
(4)向恒温恒容密闭容器中充入适量CH4,同时发生上述反应①和反应②,在不同催化剂Cat1、Cat2作用下,测得单位时间内H2的产率与温度的关系如图所示。在其他条件相同时,催化效率较高的是
 C2H2(g)+H2(g)制备氢气。
C2H2(g)+H2(g)制备氢气。①实际操作中,往往向反应器中充入一定量的水蒸气,其目的是
②忽略其他副反应,若向反应器中充入5mol水蒸气,平衡时(C2H4的转化率为75%,则该反应的Kp=
您最近一年使用:0次
2024-05-08更新
|
174次组卷
|
2卷引用:2024届内蒙古自治区赤峰市高三下学期三模理科综合试题-高中化学
4 . 将 还原转化为有用的化学产品是目前研究的热点之一、回答下列问题:
还原转化为有用的化学产品是目前研究的热点之一、回答下列问题:
Ⅰ.用铜铝催化剂可将 加氢合成甲醇,已知过程中发生的反应如下:
加氢合成甲醇,已知过程中发生的反应如下:
ⅰ.


ⅱ.


ⅲ.


(1)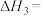
_____ (用含 、
、 的代数式表示),
的代数式表示),
_____ (用含 、
、 的代数式表示)。
的代数式表示)。
(2)查阅资料可知, ,则
,则_____ (填“低温"“商温”或“任意温度”)条件下有利于反应ⅲ自发进行。
Ⅱ. 和
和 以1:3的物质的量之比通入某密闭容器中,仅发生反应
以1:3的物质的量之比通入某密闭容器中,仅发生反应 ,
, 的平衡转化率与温度、气体的总压强的关系如图所示:
的平衡转化率与温度、气体的总压强的关系如图所示: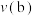
______ (填“>”“<”或“=”)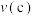 。
。
(4)平衡常数: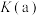
____ (填“>”“<”或“=”)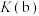 。
。
(5)压强:
______ (填“>”“<”或“=”) 。
。
(6)b点时,该反应的平衡常数
______ (分压=总压×物质的量分数,用含x、 的代数式表示)。
的代数式表示)。
Ⅲ.常温下,CH4和CO2都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如图所示: 和
和 的体积比为
的体积比为______ 。
 还原转化为有用的化学产品是目前研究的热点之一、回答下列问题:
还原转化为有用的化学产品是目前研究的热点之一、回答下列问题:Ⅰ.用铜铝催化剂可将
 加氢合成甲醇,已知过程中发生的反应如下:
加氢合成甲醇,已知过程中发生的反应如下:ⅰ.



ⅱ.



ⅲ.



(1)
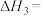
 、
、 的代数式表示),
的代数式表示),
 、
、 的代数式表示)。
的代数式表示)。(2)查阅资料可知,
 ,则
,则Ⅱ.
 和
和 以1:3的物质的量之比通入某密闭容器中,仅发生反应
以1:3的物质的量之比通入某密闭容器中,仅发生反应 ,
, 的平衡转化率与温度、气体的总压强的关系如图所示:
的平衡转化率与温度、气体的总压强的关系如图所示:
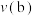
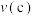 。
。(4)平衡常数:
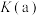
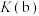 。
。(5)压强:

 。
。(6)b点时,该反应的平衡常数

 的代数式表示)。
的代数式表示)。Ⅲ.常温下,CH4和CO2都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如图所示:
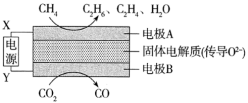
 和
和 的体积比为
的体积比为
您最近一年使用:0次
解题方法
5 . 氮氧化物是大气的主要污染物,为防治环境污染,科研人员做了大量研究。
I.汽油燃油车上安装三元催化转化器,可以使 和
和 两种尾气反应生成
两种尾气反应生成 ,可有效降低汽车尾气污染,反应为
,可有效降低汽车尾气污染,反应为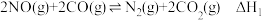 。
。
(1)下表中数据是该反应中的相关物质的标准摩尔生成焓(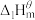 )(标准摩尔生成焓是指在
)(标准摩尔生成焓是指在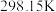 、
、 条件下,由稳定态单质生成
条件下,由稳定态单质生成 化合物时的焓变)数据。
化合物时的焓变)数据。
则
__________  。
。
(2)将 和
和 按物质的量之比
按物质的量之比 以一定的流速分别通过两种催化剂(
以一定的流速分别通过两种催化剂(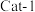 和
和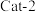 )进行反应,相同时间内测定逸出气体中
)进行反应,相同时间内测定逸出气体中 的含量,从而确定尾气脱氮率(
的含量,从而确定尾气脱氮率( 的转化率),结果如图所示。
的转化率),结果如图所示。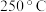 下脱氮率较高的催化剂是
下脱氮率较高的催化剂是__________ (填“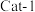 ”或“
”或“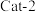 ”)。
”)。
②催化剂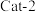 催化条件下,
催化条件下,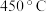 后,脱氮率随温度升高而下降的原因是
后,脱氮率随温度升高而下降的原因是_______________ 。
Ⅱ.一定条件下 与
与 可发生反应:
可发生反应: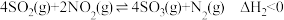 。
。
(3)将 与
与 按物质的量之比
按物质的量之比 置于恒温恒容密闭容器中反应。下列能说明反应达到平衡状态的是__________(填标号)。
置于恒温恒容密闭容器中反应。下列能说明反应达到平衡状态的是__________(填标号)。
(4)将一定量的 与
与 置于密闭容器中发生反应,在相同时间内测得
置于密闭容器中发生反应,在相同时间内测得 的物质的量分数与温度的变化曲线如图1所示(虚线为平衡时的曲线)。
的物质的量分数与温度的变化曲线如图1所示(虚线为平衡时的曲线)。 的平衡转化率与压强、温度及氮硫比
的平衡转化率与压强、温度及氮硫比 的关系如图2所示。
的关系如图2所示。_______________ 。
②图2中压强:
__________ (填“>”“<”或“=”,下同) ,氮硫比:
,氮硫比:
__________  。
。
③温度为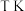 ,压强恒定为
,压强恒定为 时,反应平衡常数
时,反应平衡常数
__________ 。
I.汽油燃油车上安装三元催化转化器,可以使
 和
和 两种尾气反应生成
两种尾气反应生成 ,可有效降低汽车尾气污染,反应为
,可有效降低汽车尾气污染,反应为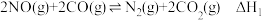 。
。(1)下表中数据是该反应中的相关物质的标准摩尔生成焓(
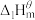 )(标准摩尔生成焓是指在
)(标准摩尔生成焓是指在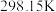 、
、 条件下,由稳定态单质生成
条件下,由稳定态单质生成 化合物时的焓变)数据。
化合物时的焓变)数据。物质 |
|
|
|
|
| 0 |
|
| 90 |

 。
。(2)将
 和
和 按物质的量之比
按物质的量之比 以一定的流速分别通过两种催化剂(
以一定的流速分别通过两种催化剂(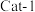 和
和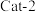 )进行反应,相同时间内测定逸出气体中
)进行反应,相同时间内测定逸出气体中 的含量,从而确定尾气脱氮率(
的含量,从而确定尾气脱氮率( 的转化率),结果如图所示。
的转化率),结果如图所示。
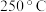 下脱氮率较高的催化剂是
下脱氮率较高的催化剂是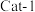 ”或“
”或“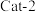 ”)。
”)。②催化剂
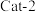 催化条件下,
催化条件下,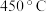 后,脱氮率随温度升高而下降的原因是
后,脱氮率随温度升高而下降的原因是Ⅱ.一定条件下
 与
与 可发生反应:
可发生反应: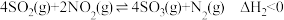 。
。(3)将
 与
与 按物质的量之比
按物质的量之比 置于恒温恒容密闭容器中反应。下列能说明反应达到平衡状态的是__________(填标号)。
置于恒温恒容密闭容器中反应。下列能说明反应达到平衡状态的是__________(填标号)。| A.体系压强保持不变 | B. 与 与 的物质的量之比保持不变 的物质的量之比保持不变 |
C. | D.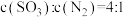 |
(4)将一定量的
 与
与 置于密闭容器中发生反应,在相同时间内测得
置于密闭容器中发生反应,在相同时间内测得 的物质的量分数与温度的变化曲线如图1所示(虚线为平衡时的曲线)。
的物质的量分数与温度的变化曲线如图1所示(虚线为平衡时的曲线)。 的平衡转化率与压强、温度及氮硫比
的平衡转化率与压强、温度及氮硫比 的关系如图2所示。
的关系如图2所示。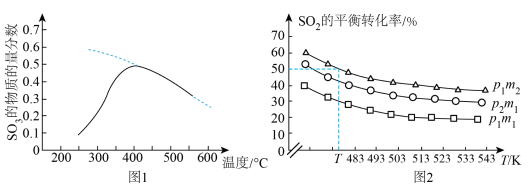
②图2中压强:

 ,氮硫比:
,氮硫比:
 。
。③温度为
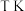 ,压强恒定为
,压强恒定为 时,反应平衡常数
时,反应平衡常数
您最近一年使用:0次
2024-04-11更新
|
587次组卷
|
6卷引用:2024届内蒙古锡林郭勒盟高三第三次模拟考试理综试卷-高中化学
2024届内蒙古锡林郭勒盟高三第三次模拟考试理综试卷-高中化学广东省湛江市2024届高三下学期第二次模拟测试化学试题(已下线)化学(福建卷01)-2024年高考押题预测卷(已下线)T13-原理综合题四川省雅安市2023-2024学年高三下学期4月月考理综试题-高中化学2024届河南省中原名校高三下学期考前全真模拟考试理科综合试题-高中化学
6 . 建设“美丽中国”首先要做好环境保护与治理。氮氧化物 是严重的大气污染物,其主要来源有汽车尾气和硝酸工厂等。氮氧化物
是严重的大气污染物,其主要来源有汽车尾气和硝酸工厂等。氮氧化物 能引起雾霾、光化学烟雾、酸雨等环境问题。某科研机构设计了如下转化氮氧化物的几种方案。请回答下列问题:
能引起雾霾、光化学烟雾、酸雨等环境问题。某科研机构设计了如下转化氮氧化物的几种方案。请回答下列问题:
方案Ⅰ:利用甲烷在催化剂条件下还原 ,相关反应如下:
,相关反应如下:
①
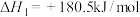
②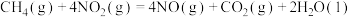
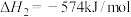
③
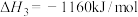
(1)表示甲烷燃烧热的热化学方程式为______ 。
(2)反应③自发进行的条件是______ (填“高温自发”、“低温自发”或“任何温度下都自发”),该反应中活化能 (逆)
(逆)______ (填“>”或“<”) (正)。
(正)。
方案Ⅱ:利用CO在催化剂条件下还原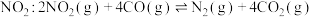 。向容积均为2L的甲(温度为)、乙(温度为
。向容积均为2L的甲(温度为)、乙(温度为 )两个恒容密闭容器中分别充入2mol
)两个恒容密闭容器中分别充入2mol 和3mol
和3mol 。反应过程中两容器内
。反应过程中两容器内 的物质的量浓度随时间的变化关系如图所示:
的物质的量浓度随时间的变化关系如图所示:

(3)由图像可得:甲容器中, 的平衡转化率为
的平衡转化率为______ ;
______  (填“>”或“<”);
(填“>”或“<”);
______ 0(填“>”或“<”),判断的依据是______ 。
(4) 温度时,该反应的平衡常数
温度时,该反应的平衡常数
______ 。
[对于反应 ,
,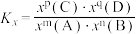 ,
, 为物质的量分数]
为物质的量分数]
方案Ⅲ:可以利用原电池原理处理氮氧化物,如下图所示:
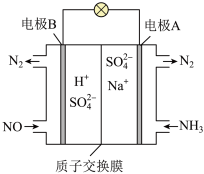
(5)该原电池的正极反应式为______ 。
 是严重的大气污染物,其主要来源有汽车尾气和硝酸工厂等。氮氧化物
是严重的大气污染物,其主要来源有汽车尾气和硝酸工厂等。氮氧化物 能引起雾霾、光化学烟雾、酸雨等环境问题。某科研机构设计了如下转化氮氧化物的几种方案。请回答下列问题:
能引起雾霾、光化学烟雾、酸雨等环境问题。某科研机构设计了如下转化氮氧化物的几种方案。请回答下列问题:方案Ⅰ:利用甲烷在催化剂条件下还原
 ,相关反应如下:
,相关反应如下:①

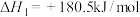
②
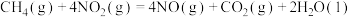
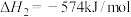
③

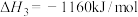
(1)表示甲烷燃烧热的热化学方程式为
(2)反应③自发进行的条件是
 (逆)
(逆) (正)。
(正)。方案Ⅱ:利用CO在催化剂条件下还原
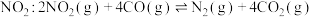 。向容积均为2L的甲(温度为)、乙(温度为
。向容积均为2L的甲(温度为)、乙(温度为 )两个恒容密闭容器中分别充入2mol
)两个恒容密闭容器中分别充入2mol 和3mol
和3mol 。反应过程中两容器内
。反应过程中两容器内 的物质的量浓度随时间的变化关系如图所示:
的物质的量浓度随时间的变化关系如图所示:
(3)由图像可得:甲容器中,
 的平衡转化率为
的平衡转化率为
 (填“>”或“<”);
(填“>”或“<”);
(4)
 温度时,该反应的平衡常数
温度时,该反应的平衡常数
[对于反应
 ,
,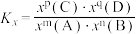 ,
, 为物质的量分数]
为物质的量分数] 方案Ⅲ:可以利用原电池原理处理氮氧化物,如下图所示:

(5)该原电池的正极反应式为
您最近一年使用:0次
7 . 党的二十大报告中强调“实现碳达峰、碳中和是一场广泛而深刻的经济社会系统性变革”。利用CO2合成淀粉的研究成果已经被我国科学家发表在《Nature》杂志上,其涉及的关键反应如下:
I.CO2(g)+3H2(g)=CH3OH(g)+H2O(g) △H1=-49.0kJ•mol-1
Ⅱ.CO2(g)+H2(g)=CO(g)+H2O(g) △H2=+41.2kJ•mol-1
Ⅲ.CO(g)+2H2(g)=CH3OH(g) △H3=
(1)反应Ⅲ的△H3=_______ ,该反应自发进行的条件是______ (填“高温自发”、“低温自发”或“任何温度下都自发”)。
(2)在该反应体系中,下列有关说法错误的是______ 。
(3)反应Ⅱ的反应速率v=v正- v逆=k正c(CO2)c(H2)-k逆c(CO)c(H2O),其中k正、k逆分别为正、逆反应速率常数,影响速率常数k的因素有温度和催化剂等。该反应的平衡常数K= ,升高温度时,k正-k逆是
,升高温度时,k正-k逆是_______ (填“增大”、“减小”或“不变”)。
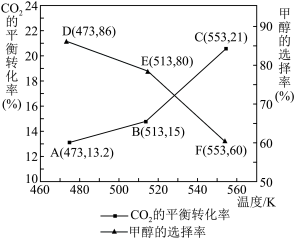
(4)在催化剂作用下,向某恒容密闭容器中通入1molCO2和3molH2,只发生I、Ⅱ两个反应。测得不同温度下CO2的平衡转化率和甲醇的选择率随温度的变化趋势如图所示。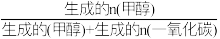 ×100%
×100%
①根据图中数据,温度选择_______ K达到平衡时,反应体系内甲醇的产量最高。随着温度的升高,CO2的平衡转化率增加,但甲醇的选择率降低,请分析其原因:________ 。
②513K时,平衡体系的压强为p0MPa,体系中n(H2O)=_______ mol,反应Ⅱ的Kp=_______ (列出计算式即可)。
I.CO2(g)+3H2(g)=CH3OH(g)+H2O(g) △H1=-49.0kJ•mol-1
Ⅱ.CO2(g)+H2(g)=CO(g)+H2O(g) △H2=+41.2kJ•mol-1
Ⅲ.CO(g)+2H2(g)=CH3OH(g) △H3=
(1)反应Ⅲ的△H3=
(2)在该反应体系中,下列有关说法错误的是
| A.增大H2的浓度有利于提高CO2的转化率 |
| B.升高温度,反应Ⅱ的速率加快,反应I的速率减慢 |
| C.选用合适的催化剂可以提高甲醇在单位时间内的产量 |
| D.达到平衡后,若压缩体积,反应I平衡正向移动,反应Ⅱ平衡不移动 |
(3)反应Ⅱ的反应速率v=v正- v逆=k正c(CO2)c(H2)-k逆c(CO)c(H2O),其中k正、k逆分别为正、逆反应速率常数,影响速率常数k的因素有温度和催化剂等。该反应的平衡常数K=
 ,升高温度时,k正-k逆是
,升高温度时,k正-k逆是(4)在催化剂作用下,向某恒容密闭容器中通入1molCO2和3molH2,只发生I、Ⅱ两个反应。测得不同温度下CO2的平衡转化率和甲醇的选择率随温度的变化趋势如图所示。
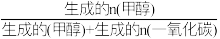 ×100%
×100%①根据图中数据,温度选择
②513K时,平衡体系的压强为p0MPa,体系中n(H2O)=
您最近一年使用:0次
2024-03-20更新
|
676次组卷
|
5卷引用:内蒙古赤峰市2024届高三一模理科综合-化学试题
内蒙古赤峰市2024届高三一模理科综合-化学试题(已下线)题型11 反应原理综合题(25题)-2024年高考化学常考点必杀300题(新高考通用)(已下线)化学(山东卷03)-2024年高考押题预测卷湖南省衡阳县第四中学2023-2024学年高三下学期4月月考化学试题2024届山东省邹城市北大新世纪高级中学高三下学期第三次模拟考试化学试题
名校
8 . 杭州亚运会主火炬燃料是“零碳甲醇”,这是一种利用焦炉气中的 和工业废气捕获的
和工业废气捕获的 生产的绿色燃料。两者在适宜的过渡金属及其氧化物催化下发生反应:
生产的绿色燃料。两者在适宜的过渡金属及其氧化物催化下发生反应:
Ⅰ.

Ⅱ.

Ⅲ.

回答下列问题:
(1)
_______ 。
(2)在密闭容器中充有2molCO和 ,在催化剂作用下发生反应Ⅱ,改变条件,测得CO的平衡转化率与温度(T)、压强(p)的关系如图所示。
,在催化剂作用下发生反应Ⅱ,改变条件,测得CO的平衡转化率与温度(T)、压强(p)的关系如图所示。
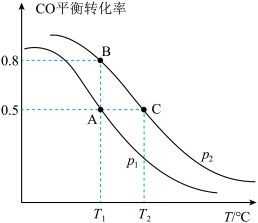
若达到平衡状态A时,容器的体积为2L,则在平衡状态B时容器的体积_______ (填“大于”、“=”或“小于”)2L。若反应进行1min达到平衡状态C,用CO的分压变化表示的平均反应速率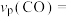
_______  ,此时的化学平衡常数
,此时的化学平衡常数
_______ [ 是用分压表示的平衡常数,某气体的分压=气体总压强×该气体的体积分数(或物质的量分数)]。
是用分压表示的平衡常数,某气体的分压=气体总压强×该气体的体积分数(或物质的量分数)]。
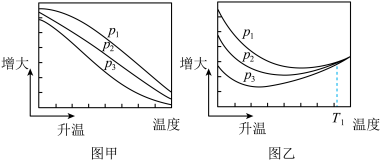
(3)不同压强下,按照 投料,实验测定
投料,实验测定 的平衡转化率和
的平衡转化率和 的平衡产率随温度的变化关系如下图所示。
的平衡产率随温度的变化关系如下图所示。
已知: 的平衡转化率
的平衡转化率
 的平衡产率
的平衡产率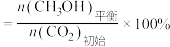
其中纵坐标表示 平衡转化率的是图
平衡转化率的是图_______ (填“甲”或“乙”);压强 、
、 、
、 由大到小的顺序为
由大到小的顺序为_______ ;图乙中 温度时,三条曲线几乎交于一点的原因是
温度时,三条曲线几乎交于一点的原因是_______ 。
(4)催化还原法
① 与丙烯通过金属杂多酸盐
与丙烯通过金属杂多酸盐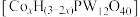 催化合成甲基丙烯酸。研究发现金属杂多酸盐中x对
催化合成甲基丙烯酸。研究发现金属杂多酸盐中x对 转化率的影响如图1所示,由图1得出催化效果最好的金属杂多酸盐化学式是
转化率的影响如图1所示,由图1得出催化效果最好的金属杂多酸盐化学式是_______ 。
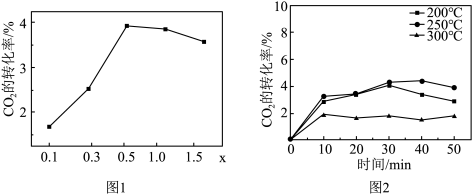
②催化剂在温度不同时对 转化率的影响如图2所示,300℃催化效果远不如200℃和250℃的原因
转化率的影响如图2所示,300℃催化效果远不如200℃和250℃的原因_______ 。
 和工业废气捕获的
和工业废气捕获的 生产的绿色燃料。两者在适宜的过渡金属及其氧化物催化下发生反应:
生产的绿色燃料。两者在适宜的过渡金属及其氧化物催化下发生反应:Ⅰ.


Ⅱ.


Ⅲ.


回答下列问题:
(1)

(2)在密闭容器中充有2molCO和
 ,在催化剂作用下发生反应Ⅱ,改变条件,测得CO的平衡转化率与温度(T)、压强(p)的关系如图所示。
,在催化剂作用下发生反应Ⅱ,改变条件,测得CO的平衡转化率与温度(T)、压强(p)的关系如图所示。
若达到平衡状态A时,容器的体积为2L,则在平衡状态B时容器的体积
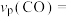
 ,此时的化学平衡常数
,此时的化学平衡常数
 是用分压表示的平衡常数,某气体的分压=气体总压强×该气体的体积分数(或物质的量分数)]。
是用分压表示的平衡常数,某气体的分压=气体总压强×该气体的体积分数(或物质的量分数)]。(3)不同压强下,按照
 投料,实验测定
投料,实验测定 的平衡转化率和
的平衡转化率和 的平衡产率随温度的变化关系如下图所示。
的平衡产率随温度的变化关系如下图所示。
已知:
 的平衡转化率
的平衡转化率
 的平衡产率
的平衡产率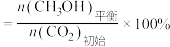
其中纵坐标表示
 平衡转化率的是图
平衡转化率的是图 、
、 、
、 由大到小的顺序为
由大到小的顺序为 温度时,三条曲线几乎交于一点的原因是
温度时,三条曲线几乎交于一点的原因是(4)催化还原法
①
 与丙烯通过金属杂多酸盐
与丙烯通过金属杂多酸盐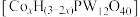 催化合成甲基丙烯酸。研究发现金属杂多酸盐中x对
催化合成甲基丙烯酸。研究发现金属杂多酸盐中x对 转化率的影响如图1所示,由图1得出催化效果最好的金属杂多酸盐化学式是
转化率的影响如图1所示,由图1得出催化效果最好的金属杂多酸盐化学式是
②催化剂在温度不同时对
 转化率的影响如图2所示,300℃催化效果远不如200℃和250℃的原因
转化率的影响如图2所示,300℃催化效果远不如200℃和250℃的原因
您最近一年使用:0次
名校
解题方法
9 . 已知下列反应的平衡常数: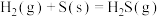 ,
, ;
; ,
, ;则反应
;则反应 的平衡常数是
的平衡常数是
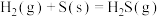 ,
, ;
; ,
, ;则反应
;则反应 的平衡常数是
的平衡常数是A. | B. | C. | D.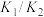 |
您最近一年使用:0次
2024-03-05更新
|
156次组卷
|
65卷引用:2015-2016学年内蒙古巴彦淖尔高二上10月月考化学试卷
2015-2016学年内蒙古巴彦淖尔高二上10月月考化学试卷【全国百强校】内蒙古自治区杭锦后旗奋斗中学2018-2019学年高二上学期期末考试化学试题2016届湖南省衡阳县第四中学高三9月月考试化学试卷2015-2016学年重庆市第一中学高二上期中测试化学试卷2015-2016学年吉林省松原市油田高中高一下期末化学试卷2016-2017学年四川省成都外国语学校高二上10月月考化学试卷辽宁省庄河市高级中学2016-2017学年高一下学期期末考试化学试题陕西省渭南市尚德中学2017-2018学年高二第一次教学质量检测化学试题甘肃省兰州第一中学2017-2018学年高二上学期期中考试化学(理)试题湖南省娄底市第四中学2018-2019学年高二上学期10月月考化学试题江西省九江市同文中学2018-2019学年高二上学期期中考试化学试题四川省遂宁市2018-2019学年高二下学期期末考试化学试题(已下线)2019年9月16日《每日一题》选修4—— 化学平衡常数甘肃省甘谷第一中学2019-2020学年高二上学期第一次月考化学试题山东省日照市第一中学2019-2020学年高二10月月考化学试题吉林省吉化第一高级中学校2019-2020学年高二9月月考化学试题新疆乌鲁木齐市第四中学2019-2020学年高二上学期期中考试化学试题广东省梅州市水寨中学2019-2020学年高二上学期期中考试化学试题湖南省长沙市长郡中学2019-2020学年高二上学期期中考试化学试题安徽省黄山市“八校联盟”2019-2020学年高二上学期期中考试化学试题四川省自贡市田家炳中学2019-2020学年高二下学期开学考试化学试题(已下线)【南昌新东方】江西省九江市同文中学2018-2019学年高二上学期期中考试化学试题安徽省亳州市涡阳县第九中学2019-2020学年高一7月月考化学试题广东省广州大学附属中学2019-2020学年高一下学期期末考试化学试题广东省广州大学附属中学等三校2019~2020学年高一下学期期末联考化学试题福建省泰宁第一中学2019-2020学年高二上学期第一阶段考试化学(选考)试题(已下线)2.3.3+化学平衡常数-2020-2021学年高二化学同步课堂帮帮帮(人教版选修4)(已下线)2.3.3化学平衡常数(重点练)-2020-2021学年高二化学上学期十分钟同步课堂专练(人教版选修4)安徽省舒城中学2020-2021学年高二上学期第二次月考化学试题河北省鸡泽县第一中学2020-2021学年高二上学期第一次月考化学试题河北省张家口市宣化区宣化第一中学2020-2021学年高二上学期10月月考化学试题黑龙江省伊春市伊美区第二中学2020-2021学年高二上学期第一次月考化学试题辽宁省大连市一〇三中学2020-2021学年高二10月月考化学试题鲁科版(2019)高二选择性必修第一册第2章 化学反应的方向、限度与速率 第2节 化学反应的限度课时1 化学平衡常数 平衡转化率人教版(2019)高二化学选择性必修1第二章 化学反应速率与化学平衡 第二节 化学平衡 课时2 化学平衡常数及相关计算(已下线)【浙江新东方】绍兴qw122选择性必修1(SJ)专题2第二单元课时3 化学平衡常数平衡转化率(已下线)第20讲 化学平衡常数及转化率的计算(练) — 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)考向23 化学平衡常数及其应用-备战2022年高考化学一轮复习考点微专题湖南省武冈市第二中学2021-2022学年高二上学期开学摸底考试化学试题天津市武清区梅厂中学2021-2022学年高二上学期阶段性练习化学试题黑龙江省绥化市望奎县第一中学2021-2022学年高二上学期第一次月考化学试题江苏省盐城市实验高级中学(新洋高级中学)2020-2021学年高二下学期期中考试化学试题(已下线)2.2.3 化学平衡常数(备作业)-【上好课】2021-2022学年高二化学同步备课系列(苏教版2019选择性必修1)重庆市清华中学校2021—2022学年上学期高二10月月考化学试题福建省福州黎明中学2021-2022学年高二上学期期中考试化学试题(已下线)第27练 化学平衡-2023年高考化学一轮复习小题多维练(全国通用)广东省揭阳华侨高级中学2021-2022学年高二上学期第一次阶段考试化学试题(已下线)2.2.1 化学平衡状态 化学平衡常数 -2022-2023学年高二化学上学期课后培优分级练(人教版2019选择性必修1)山东省济宁市泗水县2021-2022学年高二上学期期中考试化学试题广西柳州市第三中学2022-2023学年高二上学期10月月考化学试题陕西省宝鸡市千阳县中学2022-2023学年高二上学期第一次月考(理)化学试题福建省建瓯市芝华中学2021-2022学年高二上学期期中考试化学试题福建省建瓯市芝华中学2022-2023学年高二上学期期中考试化学试题福建省福州第十五中学2022-2023学年高二上学期11月线上限时训练化学试题2.2.3化学平衡常数 课中第二章 化学反应速率与化学平衡 第二节 化学平衡 第2课时 化学平衡常数河北省石家庄市第四十二中学2023-2024学年高二上学期第一次月考化学试题(已下线)第3讲 化学平衡计算 平衡常数河南省焦作市博爱县第一中学2023-2024学年高三上学期9月月考化学试题甘肃省兰州市教育局第四片区联考2023-2024学年高二上学期期中考试化学试题黑龙江省佳木斯市四校联考2023-2024学年高二上学期11月期中化学考试试题广东省台山市某校2023-2024学年高二上学期期中考试化学试题甘肃省武威市民勤县第一中学2023-2024学高二下学期开学考试化学试题湖南省衡阳县第四中学2023-2024学年高二上学期11月期中化学试题
名校
10 . 正丁烷除可直接用作燃料外,还可用作亚临界生物技术提取溶剂、制冷剂和有机合成原料。已知:
反应1:
反应2:
反应3:
回答下列问题:
(1)①
______  ,反应2正反应的活化能
,反应2正反应的活化能______ (填“大于”“等于”或“小于”,下同)逆反应的活化能;稳定性:顺-2-丁烯(g)______ 反-2-丁烯(g)。
②随着温度的升高,反应1的平衡常数 与反应2的平衡常数
与反应2的平衡常数 的比值
的比值
______ (填“增大”或“减小”)。[反应 的物质的量分数平衡常数
的物质的量分数平衡常数 ,其中x(D)、x(E)、x(G)、x(H)为各组分的物质的量分数]
,其中x(D)、x(E)、x(G)、x(H)为各组分的物质的量分数]
(2)恒温恒压下,向某反应容器中加入一定量顺-2-丁烯(g)、反-2-丁烯(g)和2molH2,同时发生反应1和反应2,顺-2-丁烯(g)的物质的量分数x(A)和反-2-丁烯(g)的物质的量分数x(B)随反应时间的变化如图。______ (填“m”或“n”)。
②设反应体系中气体总压强为pkPa,反应tmin后达到平衡,此时,体系中顺-2-丁烯(g)的物质的量为______ mol;0~tmin内,H2的分压平均变化率为______  ;该条件下,反应3的平衡常数
;该条件下,反应3的平衡常数
______ 。
③恒温恒压下,再向该容器中充入一定量惰性气体He,反应1的化学平衡将______ (填“正向移动”“逆向移动”或“不移动”)。
反应1:

反应2:

反应3:

回答下列问题:
(1)①

 ,反应2正反应的活化能
,反应2正反应的活化能②随着温度的升高,反应1的平衡常数
 与反应2的平衡常数
与反应2的平衡常数 的比值
的比值
 的物质的量分数平衡常数
的物质的量分数平衡常数 ,其中x(D)、x(E)、x(G)、x(H)为各组分的物质的量分数]
,其中x(D)、x(E)、x(G)、x(H)为各组分的物质的量分数](2)恒温恒压下,向某反应容器中加入一定量顺-2-丁烯(g)、反-2-丁烯(g)和2molH2,同时发生反应1和反应2,顺-2-丁烯(g)的物质的量分数x(A)和反-2-丁烯(g)的物质的量分数x(B)随反应时间的变化如图。

②设反应体系中气体总压强为pkPa,反应tmin后达到平衡,此时,体系中顺-2-丁烯(g)的物质的量为
 ;该条件下,反应3的平衡常数
;该条件下,反应3的平衡常数
③恒温恒压下,再向该容器中充入一定量惰性气体He,反应1的化学平衡将
您最近一年使用:0次
2024-02-23更新
|
67次组卷
|
2卷引用:内蒙古自治区赤峰第四中学2023-2024学年高三下学期开学考试理综试题-高中化学