解题方法
1 . 在一定条件下,生产化工产品C的反应如下: A(g)+B(g) 2C(g) ∆H < 0 T ℃时,向1 L密闭容器中充入1.0 mol A(g)、1.0 mol B(g),反应过程中C(g)的浓度随时间变化如图所示。
2C(g) ∆H < 0 T ℃时,向1 L密闭容器中充入1.0 mol A(g)、1.0 mol B(g),反应过程中C(g)的浓度随时间变化如图所示。

(1)0 ~10 min内,υ(C) =_____ mol/(L·min)。
(2)仅升高温度,平衡向______ (填“正”或“逆”)反应方向移动。
(3)平衡时,A的转化率是______ 。
(4)该温度下,此反应的化学平衡常数数值为______ 。
 2C(g) ∆H < 0 T ℃时,向1 L密闭容器中充入1.0 mol A(g)、1.0 mol B(g),反应过程中C(g)的浓度随时间变化如图所示。
2C(g) ∆H < 0 T ℃时,向1 L密闭容器中充入1.0 mol A(g)、1.0 mol B(g),反应过程中C(g)的浓度随时间变化如图所示。
(1)0 ~10 min内,υ(C) =
(2)仅升高温度,平衡向
(3)平衡时,A的转化率是
(4)该温度下,此反应的化学平衡常数数值为
您最近一年使用:0次
名校
2 . (1)乙基叔丁基醚(以ETBE表示)是一种性能优良的高辛烷值汽油调和剂。用乙醇与异丁烯(以IB表示)在催化剂HZSM-5催化下合成ETBE,反应的化学方程式为:C2H5OH(g)+IB(g)=ETBE(g) △H。回答下列问题:
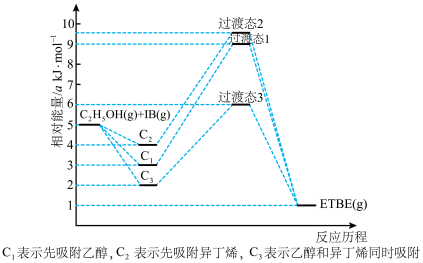
反应物被催化剂HZSM-5吸附的顺序与反应历程的关系如图所示,该反应的△H=__________ kJ·mol-1。反应历程的最优途径是________ (填C1、C2或C3)。
(2)开发清洁能源是当今化工研究的一个热点问题。二甲醚(CH3OCH3)在未来可能替代柴油和液化气作为洁净液体燃料使用,工业上以CO和H2为原料生产CH3OCH3。工业制备二甲醚在催化反应室中(压力2.0~10.0Mpa,温度230~280℃)进行下列反应:
反应ⅰ:CO(g)+2H2(g)⇌CH3OH(g) ΔH1=-99kJ·mol−1
反应ⅱ:2CH3OH(g)⇌CH3OCH3(g)+H2O(g) ΔH2=-23.5kJ·mol−1
反应ⅲ:CO(g)+H2O(g)⇌CO2(g)+H2(g) ΔH3=-41.2kJ·mol−1
①在该条件下,若反应1的起始浓度分别为:c(CO)=0.6mol·L−1,c(H2)=1.4mol·L−1,8min后达到平衡,CO的转化率为50%,则8min内H2的平均反应速率为__________ 。
②在t℃时,反应2的平衡常数为400,此温度下,在1L的密闭容器中加入一定的甲醇,反应到某时刻测得各组分的物质的量浓度如下:
此时刻v正___ v逆(填“>”“<”或“=”),平衡时c(CH3OCH3)的物质的量浓度是___ 。
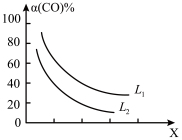
③催化反应室的总反应3CO(g)+3H2(g)⇌CH3OCH3(g)+CO2(g),CO的平衡转化率α(CO)与温度、压强的关系如图所示,图中X代表___ (填“温度”或“压强”),且L1___ L2(填“>”“<”或“=”)。
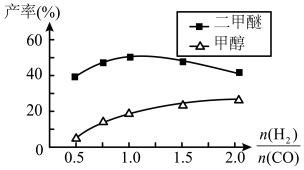
④在催化剂的作用下同时进行三个反应,发现随着起始投料比 的改变,二甲醚和甲醇的产率(产物中的碳原子占起始CO中碳原子的百分率)呈现如图的变化趋势。试解释投料比大于1.0之后二甲醚产率和甲醇产率变化的原因:
的改变,二甲醚和甲醇的产率(产物中的碳原子占起始CO中碳原子的百分率)呈现如图的变化趋势。试解释投料比大于1.0之后二甲醚产率和甲醇产率变化的原因:______________ 。

反应物被催化剂HZSM-5吸附的顺序与反应历程的关系如图所示,该反应的△H=
(2)开发清洁能源是当今化工研究的一个热点问题。二甲醚(CH3OCH3)在未来可能替代柴油和液化气作为洁净液体燃料使用,工业上以CO和H2为原料生产CH3OCH3。工业制备二甲醚在催化反应室中(压力2.0~10.0Mpa,温度230~280℃)进行下列反应:
反应ⅰ:CO(g)+2H2(g)⇌CH3OH(g) ΔH1=-99kJ·mol−1
反应ⅱ:2CH3OH(g)⇌CH3OCH3(g)+H2O(g) ΔH2=-23.5kJ·mol−1
反应ⅲ:CO(g)+H2O(g)⇌CO2(g)+H2(g) ΔH3=-41.2kJ·mol−1
①在该条件下,若反应1的起始浓度分别为:c(CO)=0.6mol·L−1,c(H2)=1.4mol·L−1,8min后达到平衡,CO的转化率为50%,则8min内H2的平均反应速率为
②在t℃时,反应2的平衡常数为400,此温度下,在1L的密闭容器中加入一定的甲醇,反应到某时刻测得各组分的物质的量浓度如下:
| 物质 | CH3OH | CH3OCH3 | H2O |
| c(mol·L−1) | 0.46 | 1.0 | 1.0 |
③催化反应室的总反应3CO(g)+3H2(g)⇌CH3OCH3(g)+CO2(g),CO的平衡转化率α(CO)与温度、压强的关系如图所示,图中X代表

④在催化剂的作用下同时进行三个反应,发现随着起始投料比
 的改变,二甲醚和甲醇的产率(产物中的碳原子占起始CO中碳原子的百分率)呈现如图的变化趋势。试解释投料比大于1.0之后二甲醚产率和甲醇产率变化的原因:
的改变,二甲醚和甲醇的产率(产物中的碳原子占起始CO中碳原子的百分率)呈现如图的变化趋势。试解释投料比大于1.0之后二甲醚产率和甲醇产率变化的原因:
您最近一年使用:0次
2020-05-13更新
|
229次组卷
|
3卷引用:山东省2022-2023学年高二上学期学业水平测试化学试题
名校
解题方法
3 . 聚乙烯醇生产过程中会产生大量副产物乙酸甲酯,其催化醇解反应可用于制备甲醇和乙酸己酯,该反应的化学方程式为:CH3COOCH3(l)+C6H13OH(l)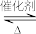 CH3COOC6H13(l)+CH3OH(l)
CH3COOC6H13(l)+CH3OH(l)
已知v正=k正x(CH3COOCH3)·x(C6H13OH),v逆=k逆x(CH3COOC6H13)·x(CH3OH),其中v正、v逆为正、逆反应速率,k正、k逆为速率常数,x为各组分的物质的量分数。
(1)反应开始时,己醇和乙酸甲酯按物质的量之比1:1投料,测得348K、343K、338K三个温度下乙酸甲酯转化率(α)随时间(t)的变化关系如图所示。

该醇解反应的ΔH____ 0(填>或<)。348K时,以物质的量分数表示的化学平衡常数Kx=____ (保留2位有效数字)。在曲线①、②、③中,k正-k逆值最大的曲线是____ ;A、B、C、D四点中,v正最大的是___ ,v逆最大的是____ 。
(2)343K时,己醇和乙酸甲酯按物质的量之比1:1、1:2和2:1进行初始投料。则达到平衡后,初始投料比____ 时,乙酸甲酯转化率最大;与按1:2投料相比,按2:1投料时化学平衡常数Kx___ (填增大、减小或不变)。
(3)该醇解反应使用离子交换树脂作催化剂,下列关于该催化剂的说法正确的是____ 。
a.参与了醇解反应,但并不改变反应历程 b.使k正和k逆增大相同倍数
c.降低了醇解反应的活化能 d.提高乙酸甲酯的平衡转化率
 CH3COOC6H13(l)+CH3OH(l)
CH3COOC6H13(l)+CH3OH(l)已知v正=k正x(CH3COOCH3)·x(C6H13OH),v逆=k逆x(CH3COOC6H13)·x(CH3OH),其中v正、v逆为正、逆反应速率,k正、k逆为速率常数,x为各组分的物质的量分数。
(1)反应开始时,己醇和乙酸甲酯按物质的量之比1:1投料,测得348K、343K、338K三个温度下乙酸甲酯转化率(α)随时间(t)的变化关系如图所示。

该醇解反应的ΔH
(2)343K时,己醇和乙酸甲酯按物质的量之比1:1、1:2和2:1进行初始投料。则达到平衡后,初始投料比
(3)该醇解反应使用离子交换树脂作催化剂,下列关于该催化剂的说法正确的是
a.参与了醇解反应,但并不改变反应历程 b.使k正和k逆增大相同倍数
c.降低了醇解反应的活化能 d.提高乙酸甲酯的平衡转化率
您最近一年使用:0次
2020-02-11更新
|
890次组卷
|
7卷引用:山东省2020年普通高中学业水平等级考试模拟试题
山东省2020年普通高中学业水平等级考试模拟试题【省级联考】山东省2020届新高考模拟统考化学试题河南省洛阳市2020届高三上学期期末模拟考试化学试题(已下线)第24讲 化学平衡常数及转化率的计算(精练)-2021年高考化学一轮复习讲练测(已下线)小题29 化学平衡的相关计算——备战2021年高考化学经典小题考前必刷(全国通用)湖北省沙市中学2021-2022学年高二上学期期末考试化学试题广东省广州大学附属中学2022-2023学年高二上学期期中考试化学试题
名校
解题方法
4 . 一定温度下,在三个体积均为2.0 L的恒容密闭容器中发生反应:PCl5(g)⇌PCl3(g)+Cl2(g)。
下列说法正确的是
| 编号 | 温度 /℃ | 起始物质 的量/mol | 平衡物质 的量/mol | 达到平衡 所需时间/s | |
| PCl5(g) | PCl3(g) | Cl2(g) | |||
| Ⅰ | 320 | 0.40 | 0.10 | 0.10 | t |
| Ⅱ | 320 | 0.80 | t1 | ||
| Ⅲ | 410 | 0.40 | 0.15 | 0.15 | t2 |
| A.平衡常数K:容器Ⅱ>容器Ⅲ |
| B.反应到达平衡时,PCl5的转化率:容器Ⅱ>容器Ⅰ |
C.反应到达平衡时,容器Ⅰ中的平均速率为v(PCl5)=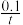 mol·L-1·s-1 mol·L-1·s-1 |
| D.起始时向容器Ⅲ中充入PCl5 0.30 mol、PCl3 0.45 mol和Cl2 0.10 mol,则反应将向逆反应方向进行 |
您最近一年使用:0次
2019-12-05更新
|
438次组卷
|
20卷引用:2018届高三一轮复习化学:微考点57-全面破解平衡常数
2018届高三一轮复习化学:微考点57-全面破解平衡常数2015届江苏省南通市高三第一次模拟化学试卷2016届江苏省无锡市青山高级中学高三上学期10月月考化学试卷2016届江苏省清江中学高三第四次(12月)月考化学试卷2016届福建省上杭县第一中学高三上12月月考化学试卷2016届福建省龙岩市上杭一中高三上学期12月月考化学试卷2017届江苏省苏州市高三上学期期初调研化学试卷2017届陕西省黄陵中学高三上学期第三次质检化学试卷安徽师范大学附属中学2017-2018学年高二上学期10月月考化学试题安徽省江淮名校2017-2018学年高二期中考试化学试题湖南省师范大学附属中学2016-2017学年高二(理科)上学期期末考试化学试题安徽省师范大学附中2019-2020学年高二上学期期中考试化学试题黑龙江省哈尔滨师范大学附属中学2020届高三上学期期中考试化学试题黑龙江省顶级名校2020届高三上学期期中考试化学试题黑龙江省安达市第七中学2020届高三上学期第二次模拟考试化学试题河北省承德第一中学2020届高三上学期第三次月考化学试题2019年秋高三化学复习强化练习—— 等效平衡(已下线)考点10 化学平衡常数及其图象分析-2020年高考化学命题预测与模拟试题分类精编黑龙江省哈尔滨市师大附中2020-2021学年高二上学期期末考试化学试题河南省新蔡县第一高级中学2021-2022学年高二上学期9月月考化学试题
名校
5 . Ⅰ.工业上可用CO或CO2来生产燃料甲醇。已知甲醇制备的有关化学反应以及在不同温度下的化学反应平衡常数如下表所示:

(1)据反应①与②可推导出K1、K2与K3之间的关系,则K3=________ (用K1、K2表示)。500 ℃时测得反应③在某时刻,H2(g)、CO2(g)、CH3OH(g)、H2O(g)的浓度(mol·L-1)分别为0.8、0.1、0.3、0.15,则此时v正________ (填“>”、“=”或“<”)v逆。
(2)在3 L容积可变的密闭容器中发生反应②,已知c(CO)—反应时间t变化曲线Ⅰ如图所示,若在t0时刻分别改变一个条件,曲线Ⅰ变为曲线Ⅱ和曲线Ⅲ。当曲线Ⅰ变为曲线Ⅱ时,改变的条件是______________ 。当曲线Ⅰ变为曲线Ⅲ时,改变的条件是______________ 。

Ⅱ.利用CO和H2可以合成甲醇,反应原理为CO(g)+2H2(g) CH3OH(g)。一定条件下,在容积为V L的密闭容器中充入a mol CO与2a mol H2合成甲醇,平衡转化率与温度、压强的关系如下图所示。
CH3OH(g)。一定条件下,在容积为V L的密闭容器中充入a mol CO与2a mol H2合成甲醇,平衡转化率与温度、压强的关系如下图所示。

(1)p1________ (填“>”、“<”或“=”)p2,理由是_____________________________ 。
(2)该甲醇合成反应在A点的平衡常数K=______________ (用a和V表示)。
(3)该反应达到平衡时,反应物转化率的关系是CO________ (填“>”、“<”或“=”)H2。
(4)下列措施中能够同时满足增大反应速率和提高CO转化率的是________ (填字母)。
A.使用高效催化剂
B.降低反应温度
C.增大体系压强
D.不断将CH3OH从反应混合物中分离出来

(1)据反应①与②可推导出K1、K2与K3之间的关系,则K3=
(2)在3 L容积可变的密闭容器中发生反应②,已知c(CO)—反应时间t变化曲线Ⅰ如图所示,若在t0时刻分别改变一个条件,曲线Ⅰ变为曲线Ⅱ和曲线Ⅲ。当曲线Ⅰ变为曲线Ⅱ时,改变的条件是

Ⅱ.利用CO和H2可以合成甲醇,反应原理为CO(g)+2H2(g)
 CH3OH(g)。一定条件下,在容积为V L的密闭容器中充入a mol CO与2a mol H2合成甲醇,平衡转化率与温度、压强的关系如下图所示。
CH3OH(g)。一定条件下,在容积为V L的密闭容器中充入a mol CO与2a mol H2合成甲醇,平衡转化率与温度、压强的关系如下图所示。
(1)p1
(2)该甲醇合成反应在A点的平衡常数K=
(3)该反应达到平衡时,反应物转化率的关系是CO
(4)下列措施中能够同时满足增大反应速率和提高CO转化率的是
A.使用高效催化剂
B.降低反应温度
C.增大体系压强
D.不断将CH3OH从反应混合物中分离出来
您最近一年使用:0次
2017-09-21更新
|
628次组卷
|
6卷引用:2018届高三一轮复习化学:微考点57-全面破解平衡常数
名校
6 . (1)CH3COOH是最常见的有机弱酸。
①CH3COOH的电离方程式为_____________ 。
②CH3COONa溶液呈碱性,原因是__________ (填“CH3COO-”或“Na+”)水解引起的。
③在CH3COONa溶液中,c(Na+)_______ c(CH3COO-)(填“>”“=”或“<”)。
(2)已知:反应C(s)+H2O(g) CO(g)+H2(g)的△H=131.3kJ/mol。
CO(g)+H2(g)的△H=131.3kJ/mol。
①该反应是反应__________ (填“吸热”或“放热”)。
②若反应消耗24g C(s),则反应的热效应为__________ 。
(3)在一定温度下,将CO(g)和H2O(g)各0.16mol通入容积为2.0L的恒容密闭容器中,发生以下反应:CO(g)+H2O(g) CO2(g)+H2(g),得到如下数据:
CO2(g)+H2(g),得到如下数据:
① 2min内,v(CO)=__________ 。
②该温度下,此反应的平衡常数表达式K=_________ 。
③其他条件不变,再充入0.1mol CO和0.1mol H2O(g),达到平衡时CO的体积分数_____ (填“增大”、“减小”或“不变”)。
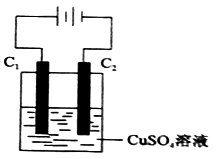
(4)下图为直流电源电解CuSO4溶液的装置,C1和C2都为石墨电极,请回答下列问题:
① C1作_________ (填“阳极”或”阴极”)。
② C2极电极反应式为____________ 。
①CH3COOH的电离方程式为
②CH3COONa溶液呈碱性,原因是
③在CH3COONa溶液中,c(Na+)
(2)已知:反应C(s)+H2O(g)
 CO(g)+H2(g)的△H=131.3kJ/mol。
CO(g)+H2(g)的△H=131.3kJ/mol。①该反应是反应
②若反应消耗24g C(s),则反应的热效应为
(3)在一定温度下,将CO(g)和H2O(g)各0.16mol通入容积为2.0L的恒容密闭容器中,发生以下反应:CO(g)+H2O(g)
 CO2(g)+H2(g),得到如下数据:
CO2(g)+H2(g),得到如下数据:t/min | 2 | 4 | 7 | 9 |
n(H2O)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
① 2min内,v(CO)=
②该温度下,此反应的平衡常数表达式K=
③其他条件不变,再充入0.1mol CO和0.1mol H2O(g),达到平衡时CO的体积分数
(4)下图为直流电源电解CuSO4溶液的装置,C1和C2都为石墨电极,请回答下列问题:
① C1作
② C2极电极反应式为
您最近一年使用:0次
2017-04-27更新
|
238次组卷
|
2卷引用:湖南省2016-2017学年高二学业水平模拟(一)化学试题



