真题
名校
1 . 下列说法正确的是
A.反应N2 (g) +3H2 (g)  2NH3 (g)的ΔH < 0,ΔS >0 2NH3 (g)的ΔH < 0,ΔS >0 |
| B.地下钢铁管道用导线连接锌块可以减缓管道的腐蚀 |
| C.常温下,Ksp[Mg(OH)2]=5.6×10-12,pH=10的含Mg2+溶液中,c(Mg2+ )≤5.6×10-4 mol·L-1 |
| D.常温常压下,锌与稀H2SO4反应生成11.2 L H2,反应中转移的电子数为6.02×1023 |
您最近一年使用:0次
2017-08-08更新
|
2995次组卷
|
7卷引用:吉林省延边第二中学2019-2020学年高二12月月考化学试题
吉林省延边第二中学2019-2020学年高二12月月考化学试题2017年全国普通高等学校招生统一考试化学(江苏卷精编版)(已下线)2019高考备考二轮复习精品资料-专题10 电化学及其应用(教学案)【全国百强校】江苏省启东中学2018-2019学年高一(创新班)下学期3月月考化学试题百所名校联考-化学反应与能量(已下线)专题十 化学能与电能(真题汇编)-2020年高考二轮模块化复习之《化学基本原理》名师讲案与提分特训重庆市渝北区、合川区、江北区等七区2019-2020学年高一下学期期末联考化学试题
名校
2 . 将一定量的氨基甲酸铵置于恒容的密闭真空容器中(固体体积忽略不计),使其达到化学平衡:H2NCOONH4(s) 2NH3(g)+CO2(g)。实验测得不同温度下的平衡数据列于下表
2NH3(g)+CO2(g)。实验测得不同温度下的平衡数据列于下表
下列有关叙述正确的是
 2NH3(g)+CO2(g)。实验测得不同温度下的平衡数据列于下表
2NH3(g)+CO2(g)。实验测得不同温度下的平衡数据列于下表| 温度/℃ | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
| 平衡总压强/kPa | 5.7 | 8.3 | 12.0 | 17.1 | 24.0 |
| 平衡气体总浓度/10-3mol/L | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
下列有关叙述正确的是
| A.在低温下该反应能自发进行 |
| B.15℃时,该反应的化学平衡常数约为2.0 |
| C.当混合气体平均相对分子质量不变时,该反应达到化学反应限度 |
| D.恒温条件下,向原平衡体系中再充入2molNH3和1molCO2,达平衡后CO2浓度不变 |
您最近一年使用:0次
2017-03-09更新
|
1161次组卷
|
5卷引用:安徽省六安市舒城中学2019-2020学年高二上学期期末考试化学试题
名校
3 . 下列说法正确的是
| A.在相同条件下PH=5的CH3COOH溶液和PH=5的NH4Cl溶液中,水的电离程度前者比后者大 |
B.反应NH3(g)+HCl(g)  NH4Cl(s)能自发进行,则该反应ΔH>0 NH4Cl(s)能自发进行,则该反应ΔH>0 |
| C.锌与稀硫酸反应时加入少量硫酸铜,反应加快的主要原因是Cu2+水解增大了c(H+) |
D.一定条件下,反应2SO2(g)+O2(g)  2SO3(g) ΔH<0达到平衡后,升高体系温度,反应重新达到平衡前,有2v正(O2)<v逆(SO3) 2SO3(g) ΔH<0达到平衡后,升高体系温度,反应重新达到平衡前,有2v正(O2)<v逆(SO3) |
您最近一年使用:0次
2017-03-08更新
|
634次组卷
|
2卷引用:四川省成都市阳安中学2020-2021学年高二下学期3月月考化学试题
13-14高二上·甘肃兰州·期末
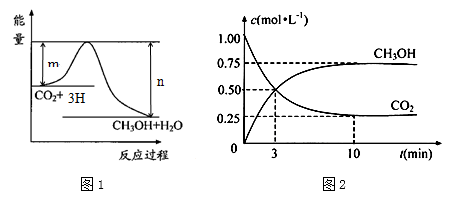
4 . 由于温室效应和资源短缺等问题,如何降低大气中的CO2含量并加以开发利用,引起了各国的普遍重视。目前工业上有一种方法是用CO2生产燃料甲醇。一定条件下发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g),图1表示该反应进行过程中能量(单位为kJ·mol—1)的变化。
CH3OH(g)+H2O(g),图1表示该反应进行过程中能量(单位为kJ·mol—1)的变化。
(1)写出该反应的热化学方程式__________________________ 。
(2)关于该反应的下列说法中,正确的是___________ 。
A.△H>0,△S>0 B.△H>0,△S<0
C.△H<0,△S<0 D.△H<0,△S>0
(3)该反应的平衡常数K的表达式为:________________ 。
(4)温度降低,平衡常数K____________ (填“增大”、 “不变”或“减小”)。
(5)为探究反应原理,现进行如下实验:在体积为1 L的密闭容器中,充入1 molCO2和3 molH2,测得CO2和CH3OH(g)的浓度随时间变化如图2所示。从反应开始到平衡,用氢气浓度变化表示的平均反应速率v (H2)=______________________ 。
(6)下列措施中能使n(CH3OH)/n(CO2)增大的有____________ 。
A.升高温度 B.加入催化剂
C.将H2O(g)从体系中分离 D.充入He(g),使体系总压强增大
 CH3OH(g)+H2O(g),图1表示该反应进行过程中能量(单位为kJ·mol—1)的变化。
CH3OH(g)+H2O(g),图1表示该反应进行过程中能量(单位为kJ·mol—1)的变化。
(1)写出该反应的热化学方程式
(2)关于该反应的下列说法中,正确的是
A.△H>0,△S>0 B.△H>0,△S<0
C.△H<0,△S<0 D.△H<0,△S>0
(3)该反应的平衡常数K的表达式为:
(4)温度降低,平衡常数K
(5)为探究反应原理,现进行如下实验:在体积为1 L的密闭容器中,充入1 molCO2和3 molH2,测得CO2和CH3OH(g)的浓度随时间变化如图2所示。从反应开始到平衡,用氢气浓度变化表示的平均反应速率v (H2)=
(6)下列措施中能使n(CH3OH)/n(CO2)增大的有
A.升高温度 B.加入催化剂
C.将H2O(g)从体系中分离 D.充入He(g),使体系总压强增大
您最近一年使用:0次
2017-02-27更新
|
216次组卷
|
3卷引用:2012-2013学年甘肃省兰州一中高二上学期期末考试化学试卷
(已下线)2012-2013学年甘肃省兰州一中高二上学期期末考试化学试卷2016-2017学年甘肃省嘉峪关市酒钢三中高二上学期期末考试化学试卷黑龙江省牡丹江市海林市朝鲜族中学2022-2023学年高二上学期第一次月考化学试题
名校
5 . 下列依据热化学方程式得出的结论正确的是
| A.已知C(石墨,s)=C(金刚石,s) ΔH>0,则金刚石比石墨稳定 |
| B.已知C(s)+O2(g)=CO2(g) ΔH1 C(s)+1/2O2(g)=CO(g) ΔH2;则ΔH2>ΔH1 |
| C.已知2H2(g)+O2(g)=2H2O(g) ΔH=-483.6 kJ/mol,则氢气的燃烧热为241.8 kJ/mol |
| D.放热过程(ΔH<0)或熵增加(ΔS> 0)的过程一定是自发的 |
您最近一年使用:0次
2017-02-26更新
|
1409次组卷
|
4卷引用:2016-2017学年新疆兵团第二师华山中学高二上学期期末考试化学试卷
名校
6 . (1)煤是一种重要的化工原料,人们将利用煤制取的水煤气、焦炭、甲醚等广泛用于工农业生产中。(1)已知:①C(s)+H2O(g)═CO(g)+H2(g) △H=+131.3kJ·mol-1
②CO2(g)+H2(g)═CO(g)+H2O(g) △H=+41.3kJ·mol-1
则碳与水蒸气反应生成二氧化碳和氢气的热化学方程式为____________ 。该反应在____________ (填“高温”、“低温”或“任何温度”)下有利于正向自发进行。
(2)有人利用炭还原法处理氮氧化物,发生反应C(s)+2NO(g) N2(g)+CO2(g)。向某密闭容器中加入一定量的活性炭和NO,在T1℃时,不同时间测得各物质的浓度如下表所示:
N2(g)+CO2(g)。向某密闭容器中加入一定量的活性炭和NO,在T1℃时,不同时间测得各物质的浓度如下表所示:
①10~20min内,N2的平均反应速率v(N2)=____________ 。
②30min后,只改变某一条件,反应重新达到平衡,根据上表中的数据判断改变的条件可能是_________ 填字母序号)。
A.通入一定量的NO B.加入一定量的活性炭
C.加入合适的催化剂 D.适当缩小容器的体积
(3)研究表明:反应CO(g)+H2O(g) H2(g)+CO2(g)平衡常数随温度的变化如下表所示:
H2(g)+CO2(g)平衡常数随温度的变化如下表所示:
若反应在500℃时进行,设起始时CO和H2O的浓度均为0.020mol·L-1,在该条件下达到平衡时,CO的转化率为____________ 。
②CO2(g)+H2(g)═CO(g)+H2O(g) △H=+41.3kJ·mol-1
则碳与水蒸气反应生成二氧化碳和氢气的热化学方程式为
(2)有人利用炭还原法处理氮氧化物,发生反应C(s)+2NO(g)
 N2(g)+CO2(g)。向某密闭容器中加入一定量的活性炭和NO,在T1℃时,不同时间测得各物质的浓度如下表所示:
N2(g)+CO2(g)。向某密闭容器中加入一定量的活性炭和NO,在T1℃时,不同时间测得各物质的浓度如下表所示:| 时间(min) 浓度(mol·L-1) | 0 | 10 | 20 | 30 | 40 | 50 |
| NO | 1.00 | 0.68 | 0.50 | 0.50 | 0.60 | 0.60 |
| N2 | 0 | 0.16 | 0.25 | 0.25 | 0.30 | 0.30 |
| CO2 | 0 | 0.16 | 0.25 | 0.25 | 0.30 | 0.30 |
①10~20min内,N2的平均反应速率v(N2)=
②30min后,只改变某一条件,反应重新达到平衡,根据上表中的数据判断改变的条件可能是
A.通入一定量的NO B.加入一定量的活性炭
C.加入合适的催化剂 D.适当缩小容器的体积
(3)研究表明:反应CO(g)+H2O(g)
 H2(g)+CO2(g)平衡常数随温度的变化如下表所示:
H2(g)+CO2(g)平衡常数随温度的变化如下表所示:| 温度/℃ | 400 | 500 | 800 |
| 平衡常数K | 9.94 | 9 | 1 |
若反应在500℃时进行,设起始时CO和H2O的浓度均为0.020mol·L-1,在该条件下达到平衡时,CO的转化率为
您最近一年使用:0次
2017-02-23更新
|
637次组卷
|
2卷引用:安徽省六安市第一中学2016-2017学年高二下学期开学考试化学试题
名校
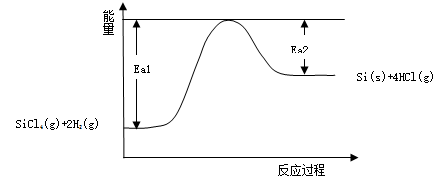
7 . 工业上制备纯硅反应的化学方程式如下:SiCl4(g)+2H2(g) = Si(s)+4HCl(g),将一定量反应物通入密闭容器进行以上反应(此条件下为可逆反应),下列叙述正确的是

| A.反应过程中,若通过缩小体积增大压强,则活化分子百分数变大,反应速率加快 |
| B.若Si-Cl、H-H、Si-Si、H-Cl的键能分别为Ea、Eb、 Ec、Ed(单位:kJ/mol),则△H=(4Ea+2Eb-Ec-4Ed )kJ/mol |
| C.该反应能量变化如下图所示,则Ea1、Ea2分别代表该反应正向和逆向的活化能,使用催化剂Ea1、Ea2都减小,△H也变小 |
| D.由下图和题目信息可知该反应△H>0,△S>0,所以在较高温度下可自发进行 |
您最近一年使用:0次
2016-12-09更新
|
608次组卷
|
3卷引用:江苏省扬州市高邮市临泽中学2021-2022学年高二9月阶段测试化学试卷
8 . (1)在与外界隔离的体系中,自发过程将导致体系的熵_________ ,(填“增大”、“减小”、“不变”);对于同一种物质,__________ 时熵值最大。(填“固态”、“液态”、“气态”)
(2)某工厂实验室用CO和H2制备CH3OH,其原理为:CO(g)+2H2(g) CH3OH(g) △H < 0该温度下的化学平衡常数表达式
CH3OH(g) △H < 0该温度下的化学平衡常数表达式_____________ ;若在298K、398K时化学平衡常数分别为K1、K2,则K1__________ K2(填“>”、“<”、“=”)
(3)M与N是同素异形体,由M=N;△H=+119KJ/mol可知,M比N________ (填稳定、不稳定)
(4)一定温度下,反应3Fe(s)+4H2O(g)⇌Fe3O4(s)+4H2(g),在一密闭容器中进行达平衡后, 保持压强不变,充入Ar,其正反应速率__________ (A.变快 B.不变 C变慢,填字母代号);该反应向__________ (填正移、逆移或不移)。
(2)某工厂实验室用CO和H2制备CH3OH,其原理为:CO(g)+2H2(g)
 CH3OH(g) △H < 0该温度下的化学平衡常数表达式
CH3OH(g) △H < 0该温度下的化学平衡常数表达式(3)M与N是同素异形体,由M=N;△H=+119KJ/mol可知,M比N
(4)一定温度下,反应3Fe(s)+4H2O(g)⇌Fe3O4(s)+4H2(g),在一密闭容器中进行达平衡后, 保持压强不变,充入Ar,其正反应速率
您最近一年使用:0次
12-13高二上·四川绵阳·阶段练习
名校
9 . 下列关于热化学反应的描述中正确的是
| A.已知:H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3kJ/mol,则H2SO4和Ba(OH)2反应H2SO4 (aq)+Ba(OH)2(aq)=BaSO4(s)+2H2O(l) ΔH=-114.6kJ/mol |
| B.CO的燃烧热是283.0kJ/mol,则:2CO2(g)=2CO(g)+O2(g) ΔH=2×(-283.0)kJ/mol |
C.两个体积相同的容器中充入等量的NO2发生反应:2NO2(g) N2O4(g) ΔH<0,绝热容器中气体的颜色比铁制容器中颜色深 N2O4(g) ΔH<0,绝热容器中气体的颜色比铁制容器中颜色深 |
| D.ΔH>0的化学反应一定不能自发进行 |
您最近一年使用:0次
12-13高二上·云南红河·期中
10 . 某化学科研小组研究在其他条件不变时,改变某一条件对反应[可用aA(g)+bB(g)⇌cC(g)表示]化学平衡的影响,得到如图所示图像(图中p表示压强,T表示温度,n表示物质的量,α表示平衡转化率):
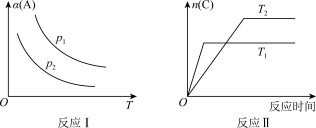
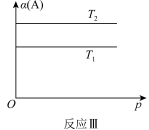
分析图像,回答下列问题:
(1)在图像反应Ⅰ中,若P1<P2(填“>”、“<”或“=”),则此正反应为是一个气体分子数_______ (填“减少”或“增大”)的反应,该正反应为_______ (填“吸热”或“放热”)反应。由此判断,此反应自发进行的温度是_______ 。(填“低温”“高温”“任何温度”)
(2)在图像反应Ⅱ中,T1_______ T2(填“>”、“<”或“=”),该正反应为_______ (填“吸热”或“放热”)反应。
(3)在图像反应Ⅲ中,若T1>T2,该反应能否自发进行_______ 。


分析图像,回答下列问题:
(1)在图像反应Ⅰ中,若P1<P2(填“>”、“<”或“=”),则此正反应为是一个气体分子数
(2)在图像反应Ⅱ中,T1
(3)在图像反应Ⅲ中,若T1>T2,该反应能否自发进行
您最近一年使用:0次



