解题方法
1 . 常温下,将等浓度的 溶液分别滴加到等
溶液分别滴加到等 、等体积的
、等体积的 、
、 两种弱酸溶液中,溶液的
两种弱酸溶液中,溶液的 与粒子浓度比值的对数关系如图所示。下列叙述错误的是
与粒子浓度比值的对数关系如图所示。下列叙述错误的是
 溶液分别滴加到等
溶液分别滴加到等 、等体积的
、等体积的 、
、 两种弱酸溶液中,溶液的
两种弱酸溶液中,溶液的 与粒子浓度比值的对数关系如图所示。下列叙述错误的是
与粒子浓度比值的对数关系如图所示。下列叙述错误的是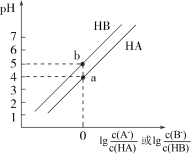
A. 的浓度大于 的浓度大于 的浓度 的浓度 |
| B.a点水的电离程度小于b点水的电离程度 |
C.常温下 的电离常数是 的电离常数是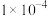 |
D.向 溶液中滴加 溶液中滴加 溶液至 溶液至 时, 时,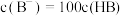 |
您最近一年使用:0次
2 . 下列对溶液平衡体系的说法不正确的是
| A.常温下,NaCN溶液呈碱性,说明HCN是弱电解质 |
| B.将KCl溶液从常温加热至80℃,溶液的pH变小但仍保持中性 |
C. 醋酸溶液在加水稀释过程中,溶液中所有离子的浓度均减小 醋酸溶液在加水稀释过程中,溶液中所有离子的浓度均减小 |
D.可用pH试纸鉴别浓度均为 的 的 、 、 溶液 溶液 |
您最近一年使用:0次
解题方法
3 . 在 时,下列有关电解质溶液的说法正确的是
时,下列有关电解质溶液的说法正确的是
 时,下列有关电解质溶液的说法正确的是
时,下列有关电解质溶液的说法正确的是A. 的盐酸与 的盐酸与 的氨水等体积混合后,溶液中: 的氨水等体积混合后,溶液中: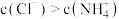 |
B.等浓度的盐酸和醋酸溶液,分别中和等量的 ,消耗醋酸的体积多 ,消耗醋酸的体积多 |
C. 的 的 溶液与 溶液与 的 的 溶液,水的电离程度相同 溶液,水的电离程度相同 |
D. 溶液加水稀释, 溶液加水稀释,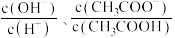 都增大 都增大 |
您最近一年使用:0次
解题方法
4 . 室温下,用0.1mol•L-1的一水合二甲胺[(CH3)2NH•H2O]溶液(一水合二甲胺在水中的电离与一水合氨相似)滴定10.00mL0.1mol•L-1盐酸溶液。溶液pH随加入一水合二甲胺溶液体积变化曲线如图所示(忽略溶液混合时的体积变化)。下列说法正确的是
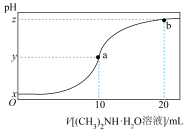
| A.本实验应该选择酚酞作指示剂 |
| B.x>1,y<7 |
| C.a、b两点的溶液中,Kw不相等 |
D.b点溶液中存在:2c(Cl-)=c[(CH3)2NH ]+c[(CH3)2NH•H2O] ]+c[(CH3)2NH•H2O] |
您最近一年使用:0次
2024-09-19更新
|
65次组卷
|
2卷引用:广东省深圳市2025届高三上学期9月联考化学试题
5 . 常温下,用 的
的 溶液滴定
溶液滴定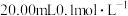 的
的 溶液,混合液的
溶液,混合液的 与
与 溶液体积的变化关系如图(不考虑溶液混合时体积和温度的变化)。下列说法正确的是
溶液体积的变化关系如图(不考虑溶液混合时体积和温度的变化)。下列说法正确的是
 的
的 溶液滴定
溶液滴定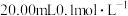 的
的 溶液,混合液的
溶液,混合液的 与
与 溶液体积的变化关系如图(不考虑溶液混合时体积和温度的变化)。下列说法正确的是
溶液体积的变化关系如图(不考虑溶液混合时体积和温度的变化)。下列说法正确的是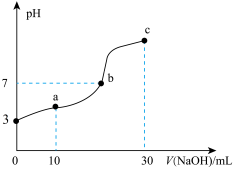
A.该温度下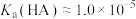 |
B.a点溶液中,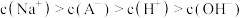 |
C.b点溶液中,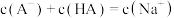 |
| D.从a到c的过程中水的电离程度先减小后增大 |
您最近一年使用:0次
6 . 常温下将NaOH溶液滴加到20mL H2A溶液中,混合溶液的pH与离子浓度变化的关系如图所示[纵坐标为 或
或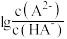 ]。下列叙述错误的是
]。下列叙述错误的是
 或
或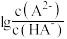 ]。下列叙述错误的是
]。下列叙述错误的是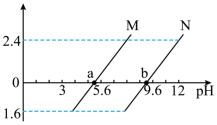
A.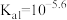 |
B.图中a点对应溶液中: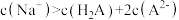 |
C.溶液中NaHA和H2A 1∶1时: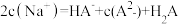 |
| D.溶液pH从5.6到9.6的过程中,水的电离程度逐渐增大 |
您最近一年使用:0次
2024-09-17更新
|
93次组卷
|
2卷引用:湖南省衡阳县四中2024届高三下学期高考猜题卷化学试题
7 . 缓冲溶液在一定程度上维持酸碱稳定。常温下,用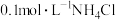 和
和 氨水配制
氨水配制 不同缓冲比下的缓冲溶液,如下表所示,再分别往缓冲溶液中滴加
不同缓冲比下的缓冲溶液,如下表所示,再分别往缓冲溶液中滴加 溶液,用
溶液,用 传感器测得不同缓冲比下溶液的
传感器测得不同缓冲比下溶液的 随滴加盐酸体积的变化曲线如图。下列说法不正确的是
随滴加盐酸体积的变化曲线如图。下列说法不正确的是
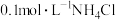 和
和 氨水配制
氨水配制 不同缓冲比下的缓冲溶液,如下表所示,再分别往缓冲溶液中滴加
不同缓冲比下的缓冲溶液,如下表所示,再分别往缓冲溶液中滴加 溶液,用
溶液,用 传感器测得不同缓冲比下溶液的
传感器测得不同缓冲比下溶液的 随滴加盐酸体积的变化曲线如图。下列说法不正确的是
随滴加盐酸体积的变化曲线如图。下列说法不正确的是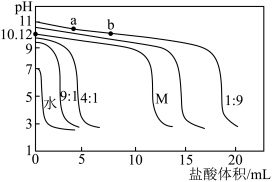
| 缓冲比 |  |  氨水 氨水 |
 | 1.5 | 13.5 |
 | 3.0 | 12.0 |
 | 7.5 | 7.5 |
 | 12.0 | 3.0 |
 | 13.5 | 1.5 |
A.水的电离程度: |
B.由图可知,缓冲比为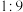 的缓冲溶液抗酸能力最强 的缓冲溶液抗酸能力最强 |
C.该温度下,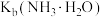 近似等于 近似等于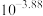 |
D.曲线M的缓冲比为 ,且该曲线上任意一点均存在: ,且该曲线上任意一点均存在: |
您最近一年使用:0次
2024-09-16更新
|
33次组卷
|
2卷引用:广东省茂名市2023-2024学年高三上学期第一次综合测试化学试题
8 . 常温下,用 盐酸滴定
盐酸滴定 溶液,滴定曲线如图所示。下列说法错误的是
溶液,滴定曲线如图所示。下列说法错误的是 ;
;
②不考虑溶液体积和温度的变化。
 盐酸滴定
盐酸滴定 溶液,滴定曲线如图所示。下列说法错误的是
溶液,滴定曲线如图所示。下列说法错误的是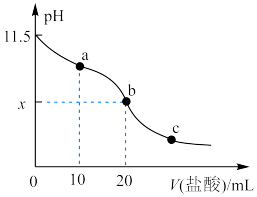
 ;
;②不考虑溶液体积和温度的变化。
A. |
B.常温下, |
C.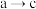 的过程中,水的电离程度先减小后增大 的过程中,水的电离程度先减小后增大 |
D.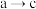 的过程中,一定存在 的过程中,一定存在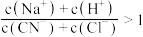 |
您最近一年使用:0次
2024-09-16更新
|
116次组卷
|
3卷引用:河北省保定市定州市2023-2024学年高二上学期1月期末化学试题
名校
解题方法
9 . 电位滴定法是根据滴定过程中指示电极电位的变化来确定滴定终点的一种滴定分析方法。在化学计量点附近,被测离子浓度发生突跃,指示电极电位也产生了突跃,进而确定滴定终点的位置,已知:某二元酸 电离常数
电离常数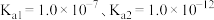 。某化学小组采用电位滴定法,用盐酸滴定某溶液中
。某化学小组采用电位滴定法,用盐酸滴定某溶液中 的浓度,滴定过程中,溶液电位U、电极电压随盐酸体积V的变化曲线如图所示,下列说法中正确的是
的浓度,滴定过程中,溶液电位U、电极电压随盐酸体积V的变化曲线如图所示,下列说法中正确的是
 电离常数
电离常数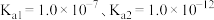 。某化学小组采用电位滴定法,用盐酸滴定某溶液中
。某化学小组采用电位滴定法,用盐酸滴定某溶液中 的浓度,滴定过程中,溶液电位U、电极电压随盐酸体积V的变化曲线如图所示,下列说法中正确的是
的浓度,滴定过程中,溶液电位U、电极电压随盐酸体积V的变化曲线如图所示,下列说法中正确的是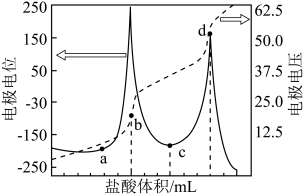
| A.b点溶液显碱性 |
B.水电离出的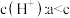 |
C.d点溶液中: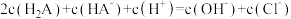 |
D.实验过程中小组发现所用 溶液混有少量 溶液混有少量 ,将b点消耗的盐酸体积记为 ,将b点消耗的盐酸体积记为 ,d点消耗的盐酸体积为 ,d点消耗的盐酸体积为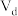 ,则 ,则 的含量可表示为 的含量可表示为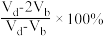 |
您最近一年使用:0次
10 . 亚砷酸( )作为一种化疗药物,常用于白血病的治疗,其在水溶液中存在多种微粒形态。常温下,用
)作为一种化疗药物,常用于白血病的治疗,其在水溶液中存在多种微粒形态。常温下,用 溶液滴定
溶液滴定 时,各种含砷微粒的物质的量分数随
时,各种含砷微粒的物质的量分数随 的变化如图所示。下列说法不正确的是
的变化如图所示。下列说法不正确的是
 )作为一种化疗药物,常用于白血病的治疗,其在水溶液中存在多种微粒形态。常温下,用
)作为一种化疗药物,常用于白血病的治疗,其在水溶液中存在多种微粒形态。常温下,用 溶液滴定
溶液滴定 时,各种含砷微粒的物质的量分数随
时,各种含砷微粒的物质的量分数随 的变化如图所示。下列说法不正确的是
的变化如图所示。下列说法不正确的是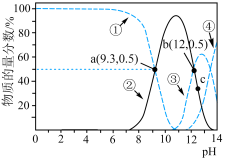
A.②代表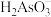 ,③代表 ,③代表 |
B.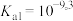 , ,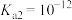 |
C.等浓度的 与 与 等体积混合,所得溶液中水的电离受到抑制 等体积混合,所得溶液中水的电离受到抑制 |
D. 点溶液中 点溶液中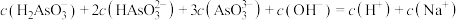 |
您最近一年使用:0次



