名校
解题方法
1 . 某温度下,0.100mol/LNaOH滴定50.0mL0.0500mol/LHCl溶液的滴定曲线如图所示。设该温度下水的离子积为Kw。下列说法错误的是
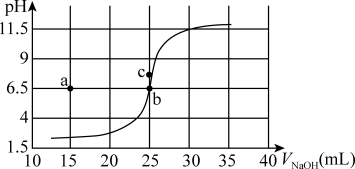

| A.根据曲线数据计算可知该温度下Kw为10-13 |
| B.曲线上各点的溶液满足关系式c(H+)·c(OH—)=Kw |
| C.其它条件相同,若降温,反应终点b向c方向移动 |
| D.相同实验条件下,若改为滴定0.0200mol·L-1H2SO4,反应终点b移到a |
您最近一年使用:0次
2021-06-01更新
|
1983次组卷
|
12卷引用:广西玉林市博白县中学2023-2024学年高三上学期10月月考化学试题
广西玉林市博白县中学2023-2024学年高三上学期10月月考化学试题广东省广州市华南师范大学附属中学2021届高三下学期三模化学试题(已下线)第24讲 水的电离和溶液的pH(精练)-2022年高考化学一轮复习讲练测黑龙江省密山市第一中学2021-2022学年高二上学期期中考试化学试题黑龙江省大庆实验中学2021-2022学年高二上学期期中考试化学试题黑龙江省鹤岗市第三中学2021-2022学年高二下学期开学考试化学试题湖北省襄阳市第五中学2022届高三适应性考试(一)化学试题天津市第一中学2022-2023学年高二上学期月考化学试题广东省广州市华南师范大学附属中学2022届高三上学期综合测试(一)化学试题江西省宜春市宜丰中学2022-2023学年高三上学期1月期末考试化学试题重庆市育才中学2023-2024学年高二上学期10月月考化学试题【定心卷】3.2.3 酸碱中和滴定随堂练习-人教版2023-2024学年选择性必修1
2 . 花椒油是从花椒籽中提取的一种香精油,具有挥发性,溶于乙醇、乙醚等有机溶剂。利用如图所示装置处理花椒籽粉,经分离提纯得到花椒油。
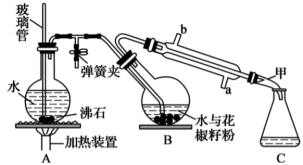
实验步骤:
i.在装置A中的圆底烧瓶中装入 容积的水,加2~3粒沸石。同时在装置B中的圆底烧瓶中加入20g花椒籽粉和50mL水。
容积的水,加2~3粒沸石。同时在装置B中的圆底烧瓶中加入20g花椒籽粉和50mL水。
ii.加热装置A中的圆底烧瓶,当有大量水蒸气产生时关闭弹簧夹,进行蒸馏。
iii.向馏出液中加入食盐至饱和,再用15mL乙醚萃取2次,将两次萃取的醚层合并,加入少量无水Na2SO4;将液体注入蒸馏烧瓶,蒸馏得花椒油。
回答下列问题:
(1)装置A中玻璃管的作用是___ ;装置B中圆底烧瓶倾斜的目的是___ 。
(2)步骤ii中,当观察到_____________ 现象时,可停止蒸馏。蒸馏结束时,下列操作的顺序为___ (填标号)。
a.停止加热 b.打开弹簧夹 c.关闭冷凝水
(3)在馏出液中加入食盐的作用是___ ;加入无水Na2SO4的作用是___ 。
(4)实验结束后,用稀NaOH溶液清洗冷凝管(冷凝管中的残留物以 表示),反应的化学方程式为
表示),反应的化学方程式为___ 。
(5)为测定花椒油中油脂的含量,取20.00mL花椒油溶于乙醇中,加入92.00mL0.5000mol•L-1NaOH的乙醇溶液,搅拌,充分反应;加水配成200.0mL溶液,从中取出25.00mL溶液于锥形瓶中,滴入几滴酚酞试液,用0.1000mol•L-1HCl溶液进行滴定,滴定终点消耗HCl溶液20.00mL。则该花椒油中含有油脂___ g•L-1(油脂用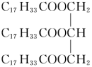 表示,它的相对分子质量为884)。
表示,它的相对分子质量为884)。

实验步骤:
i.在装置A中的圆底烧瓶中装入
 容积的水,加2~3粒沸石。同时在装置B中的圆底烧瓶中加入20g花椒籽粉和50mL水。
容积的水,加2~3粒沸石。同时在装置B中的圆底烧瓶中加入20g花椒籽粉和50mL水。ii.加热装置A中的圆底烧瓶,当有大量水蒸气产生时关闭弹簧夹,进行蒸馏。
iii.向馏出液中加入食盐至饱和,再用15mL乙醚萃取2次,将两次萃取的醚层合并,加入少量无水Na2SO4;将液体注入蒸馏烧瓶,蒸馏得花椒油。
回答下列问题:
(1)装置A中玻璃管的作用是
(2)步骤ii中,当观察到
a.停止加热 b.打开弹簧夹 c.关闭冷凝水
(3)在馏出液中加入食盐的作用是
(4)实验结束后,用稀NaOH溶液清洗冷凝管(冷凝管中的残留物以
 表示),反应的化学方程式为
表示),反应的化学方程式为(5)为测定花椒油中油脂的含量,取20.00mL花椒油溶于乙醇中,加入92.00mL0.5000mol•L-1NaOH的乙醇溶液,搅拌,充分反应;加水配成200.0mL溶液,从中取出25.00mL溶液于锥形瓶中,滴入几滴酚酞试液,用0.1000mol•L-1HCl溶液进行滴定,滴定终点消耗HCl溶液20.00mL。则该花椒油中含有油脂
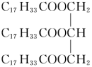 表示,它的相对分子质量为884)。
表示,它的相对分子质量为884)。
您最近一年使用:0次
2021-03-09更新
|
1005次组卷
|
6卷引用:广西南宁市2020-2021学年高二上学期期末考试化学试题
广西南宁市2020-2021学年高二上学期期末考试化学试题(已下线)专题七 羧酸 羧酸衍生物-2020-2021学年高二《新题速递·化学》(人教版2019选择性必修3)3月刊 (同步课堂必刷题)(已下线)3.4 羧酸 羧酸衍生物(B级能力练)-2020-2021学年高二化学章节分层检测ABC(人教版2019选择性必修3)(已下线)专题一 油脂-2020-2021学年高二《新题速递·化学》(人教版选修5)4月刊 (同步课堂必刷题)(已下线)第3章 水溶液中的离子反应与平衡(基础过关卷)-【高效检测】2021-2022学年高二化学章末测试卷(人教版2019选择性必修1)专题6 生命活动的物质基础——糖类、油脂、蛋白质 本专题达标检测
名校
3 . 某兴趣小组同学向一定体积的Ba(OH)2溶液中逐滴滴加稀H2SO4,不断搅拌并测定溶液导电能力的变化(装置如下图所示)。
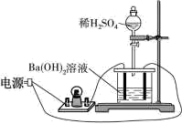
I.实验测得混合溶液的导电能力随时间变化的曲线如图所示。
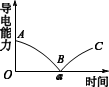
(1)写出Ba(OH)2溶液与稀H2SO4反应的离子方程式_________________ 。
(2)实验现象:烧杯中有白色沉淀产生,小灯泡__________________ 。
(3)下列说法正确的是__________________ (填“序号”)
a.AB段溶液的导电能力不断减弱,说明生成的BaSO4不是电解质
b.B处溶液的导电能力约为0,说明溶液中几乎没有自由移动的离子
c.a时刻Ba(OH)2溶液与稀H2SO4恰好中和
d.BC段溶液的导电能力不断增大,主要是由于过量的Ba(OH)2电离出的离子导电
II.配制250mL1.0mol/LH2SO4溶液。
(1)计算:需要18mol/LH2SO4溶液__________ mL(计算结果精确到小数点后一位)。
(2)配制过程中,不需要使用的仪器有_________________ (填“序号”)。
①量筒 ②托盘天平 ③烧瓶 ④250ml容量瓶 ⑤烧杯 ⑥玻璃棒 ⑦胶头滴管
(3)配制过程中的正确操作顺序是:b、d、____________ 、e(填“字母”)。
a.用少量蒸馏水洗涤烧杯和玻璃棒2~3次,洗涤液均注入容量瓶。
b.用量筒量取所需体积的18mol/LH2SO4溶液注入盛有约50ml蒸馏水的烧杯。
c.用胶头滴管滴加蒸馏水,至溶液的凹液面与刻度线相切。
d.用玻璃棒慢慢搅动,混合均匀。
e.盖好容量瓶瓶塞,反复上下颠倒,摇匀
f.将稀释后的H2SO4溶液沿玻璃棒注入250ml容量瓶。
g.往容量瓶中加入蒸馏水,直到液面在容量瓶刻度线下1~2cm处。
(4)下列操作将导致所配制的H2SO4溶液浓度偏大的是________________ (填“字母”)。
a.移液过程有H2SO4溶液溅出瓶外 b.移液后未洗涤烧杯和玻璃棒
c.定容时俯视容量瓶刻度线 d.加水超过刻度线,用胶头滴管吸出多余液体

I.实验测得混合溶液的导电能力随时间变化的曲线如图所示。

(1)写出Ba(OH)2溶液与稀H2SO4反应的离子方程式
(2)实验现象:烧杯中有白色沉淀产生,小灯泡
(3)下列说法正确的是
a.AB段溶液的导电能力不断减弱,说明生成的BaSO4不是电解质
b.B处溶液的导电能力约为0,说明溶液中几乎没有自由移动的离子
c.a时刻Ba(OH)2溶液与稀H2SO4恰好中和
d.BC段溶液的导电能力不断增大,主要是由于过量的Ba(OH)2电离出的离子导电
II.配制250mL1.0mol/LH2SO4溶液。
(1)计算:需要18mol/LH2SO4溶液
(2)配制过程中,不需要使用的仪器有
①量筒 ②托盘天平 ③烧瓶 ④250ml容量瓶 ⑤烧杯 ⑥玻璃棒 ⑦胶头滴管
(3)配制过程中的正确操作顺序是:b、d、
a.用少量蒸馏水洗涤烧杯和玻璃棒2~3次,洗涤液均注入容量瓶。
b.用量筒量取所需体积的18mol/LH2SO4溶液注入盛有约50ml蒸馏水的烧杯。
c.用胶头滴管滴加蒸馏水,至溶液的凹液面与刻度线相切。
d.用玻璃棒慢慢搅动,混合均匀。
e.盖好容量瓶瓶塞,反复上下颠倒,摇匀
f.将稀释后的H2SO4溶液沿玻璃棒注入250ml容量瓶。
g.往容量瓶中加入蒸馏水,直到液面在容量瓶刻度线下1~2cm处。
(4)下列操作将导致所配制的H2SO4溶液浓度偏大的是
a.移液过程有H2SO4溶液溅出瓶外 b.移液后未洗涤烧杯和玻璃棒
c.定容时俯视容量瓶刻度线 d.加水超过刻度线,用胶头滴管吸出多余液体
您最近一年使用:0次
2021-02-21更新
|
297次组卷
|
3卷引用:广西壮族自治区柳州市鹿寨县鹿寨中学2021-2022学年高一上学期12月月考化学试题
名校
4 . 已知:ICl的熔点为13.9℃,沸点为97.4℃,易水解,ICl3的熔点为111℃,并且已知:ICl(l)+Cl2(g)=ICl3(s)。用下图(中夹持装置略去)的装置制取ICl。
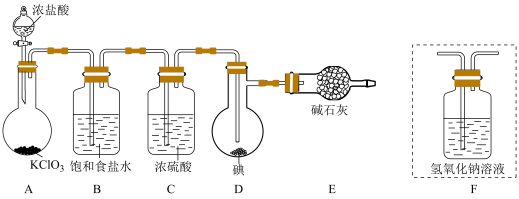
(1)装置A中发生反应的化学方程式是_____________________ 。
(2)装置B的作用是_________ ,不能用装置F代替装置E,理由____________ 。
(3)所制得的ICl中溶有少量ICl3杂质,提纯的方法是____________ (填标号)。
A.过滤 B.蒸发结晶 C.蒸馏 D.分液
(4)用ICl的冰醋酸溶液测定某油脂的不饱和度。进行如下两个实验,实验过程中有关反应为:
①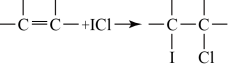
②ICl+KI=I2+KCl
③I2+2Na2S2O3=2NaI+Na2S4O6
实验1:将5.00 g该油脂样品溶于四氯化碳后形成100 mL溶液,从中取出十分之一,加入20 mL某ICl的冰醋酸溶液(过量),充分反应后,加入足量KI溶液,生成的碘单质用a mol/L的Na2S2O3标准溶液滴定。经平行实验,测得消耗的Na2S2O3溶液的平均体积为V1 mL。
实验2(空白实验):不加油脂样品,其它操作步骤、所用试剂及用量与实验I完全相同,测得消耗的Na2S2O3溶液的平均体积为V2 mL。
①滴定过程需要的指示剂是___________________ 。
②5.00 g该油脂样品所消耗的ICl的物质的量为________ mol。由此数据经换算即可求得该油脂的不饱和度。

(1)装置A中发生反应的化学方程式是
(2)装置B的作用是
(3)所制得的ICl中溶有少量ICl3杂质,提纯的方法是
A.过滤 B.蒸发结晶 C.蒸馏 D.分液
(4)用ICl的冰醋酸溶液测定某油脂的不饱和度。进行如下两个实验,实验过程中有关反应为:
①
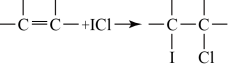
②ICl+KI=I2+KCl
③I2+2Na2S2O3=2NaI+Na2S4O6
实验1:将5.00 g该油脂样品溶于四氯化碳后形成100 mL溶液,从中取出十分之一,加入20 mL某ICl的冰醋酸溶液(过量),充分反应后,加入足量KI溶液,生成的碘单质用a mol/L的Na2S2O3标准溶液滴定。经平行实验,测得消耗的Na2S2O3溶液的平均体积为V1 mL。
实验2(空白实验):不加油脂样品,其它操作步骤、所用试剂及用量与实验I完全相同,测得消耗的Na2S2O3溶液的平均体积为V2 mL。
①滴定过程需要的指示剂是
②5.00 g该油脂样品所消耗的ICl的物质的量为
您最近一年使用:0次
2020-09-05更新
|
346次组卷
|
4卷引用:广西南宁市第二中学2022-2023学年高二上学期12月月考化学试卷
5 . 84消毒液、酒精、过氧乙酸等消毒剂在抗击新型冠状病毒肺炎疫情中起到重要作用。回答下列问题:
Ⅰ.84消毒液是北京第一传染病医院(现北京地坛医院)于1984年研制的一种消毒液,主要成分为受热易分解的次氯酸钠(NaClO)。某实验小组用如图装置制备84消毒液。
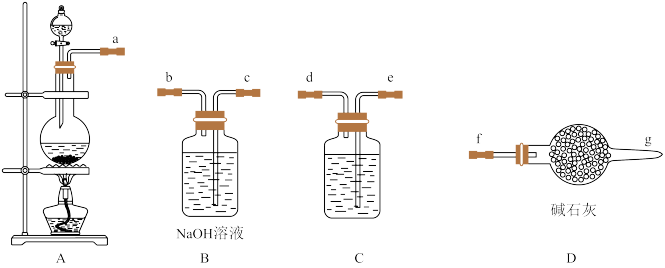
(1)A中发生反应的离子方程式为___ 。
(2)C中盛装试剂为__ ,仪器的连接顺序为a→__ 。
(3)制备84消毒液时,若Cl2与NaOH溶液反应温度过高,NaClO的产率将__ (填“增大”“减小”或“不变”)。
Ⅱ.过氧乙酸(CH3COOOH)是无色液体,易溶于水,有强烈刺激性气味,有腐蚀性,对人的眼睛、皮肤、黏膜、上呼吸道等有强烈刺激作用,易分解,易爆炸。
(4)贮存和运输CH3COOOH时要注意的事项是__ 。
(5)消毒过程中需将200mL20%的过氧乙酸(密度为1.02g·cm-3)稀释为0.5%的过氧乙酸,则需加入水的体积为__  。
。
(6)CH3COOOH可用H2O2和CH3COOH制备,其化学方程式为___ 。
(7)制备CH3COOOH过程中总会残留少量H2O2,因此CH3COOOH在使用过程中需要准确标定原液的浓度。取CH3COOOH样品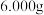 ,标定步骤如下:
,标定步骤如下:
a.用KMnO4标准溶液滴定H2O2;
b.当达到终点时加入足量KI溶液,发生反应:2KI+H2SO4+CH3COOOH=2KHSO4+CH3COOH+H2O+I2;
c.用1.500mol·L-1Na2S2O3标准溶液滴定生成的I2,发生反应:I2+2Na2S2O3=2NaI+Na2S4O6,消耗Na2S2O3溶液20.00mL。
测得样品中CH3COOOH的质量分数为___ 。
Ⅰ.84消毒液是北京第一传染病医院(现北京地坛医院)于1984年研制的一种消毒液,主要成分为受热易分解的次氯酸钠(NaClO)。某实验小组用如图装置制备84消毒液。

(1)A中发生反应的离子方程式为
(2)C中盛装试剂为
(3)制备84消毒液时,若Cl2与NaOH溶液反应温度过高,NaClO的产率将
Ⅱ.过氧乙酸(CH3COOOH)是无色液体,易溶于水,有强烈刺激性气味,有腐蚀性,对人的眼睛、皮肤、黏膜、上呼吸道等有强烈刺激作用,易分解,易爆炸。
(4)贮存和运输CH3COOOH时要注意的事项是
(5)消毒过程中需将200mL20%的过氧乙酸(密度为1.02g·cm-3)稀释为0.5%的过氧乙酸,则需加入水的体积为
 。
。(6)CH3COOOH可用H2O2和CH3COOH制备,其化学方程式为
(7)制备CH3COOOH过程中总会残留少量H2O2,因此CH3COOOH在使用过程中需要准确标定原液的浓度。取CH3COOOH样品
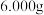 ,标定步骤如下:
,标定步骤如下:a.用KMnO4标准溶液滴定H2O2;
b.当达到终点时加入足量KI溶液,发生反应:2KI+H2SO4+CH3COOOH=2KHSO4+CH3COOH+H2O+I2;
c.用1.500mol·L-1Na2S2O3标准溶液滴定生成的I2,发生反应:I2+2Na2S2O3=2NaI+Na2S4O6,消耗Na2S2O3溶液20.00mL。
测得样品中CH3COOOH的质量分数为
您最近一年使用:0次
2020-06-18更新
|
618次组卷
|
5卷引用:广西南宁市第十中学2020-2021学年高二上学期期中考试化学(理)试题
广西南宁市第十中学2020-2021学年高二上学期期中考试化学(理)试题云南省昆明市2020届高三“三诊一模”高考模拟考试(三模)理综化学试题(已下线)第一单元 物质的量测试题-2021年高考化学一轮复习名师精讲练福建省永安市第三中学2021届高三9月月考化学试题甘肃省天水市甘谷县第四中学2021届高三上学期第二次检测化学试题
名校
解题方法
6 . 某小组以CoCl2·6H2O、过氧化氢、液氨、氯化铵固体为原料,在活性炭催化下,合成了橙黄色晶体X。为确定其组成,进行如下实验:
①氨的测定:精确称取wgX,加适量水溶解,注入圆底烧瓶中,然后逐滴加入足量10%NaOH溶液,通入水蒸气,将样品溶液中的氨全部蒸出,用V1mL c1mol·L-1的盐酸溶液吸收。蒸氨结束后取下接收瓶,用c2mol·L-1 NaOH标准溶液滴定过剩的HCl,到终点时消耗V2mLNaOH溶液。
②氯的测定:准确称取样品X配成溶液后用AgNO3标准溶液滴定,K2CrO4溶液为指示剂,至出现砖红色沉淀不再消失为终点(Ag2CrO4为砖红色)。
回答下列问题:
(1)用NaOH标准溶液滴定过剩的HCl时,应使用_______ 式滴定管,该滴定实验可使用的指示剂为_______ ,达到滴定终点的现象为____________________________
(2)样品中氨的质量分数表达式为__________________________
(3)滴定终点时,若溶液中c(Ag+)=2.0×10-5mol·L-1 ,c(CrO42-)为________ mol·L-1。(已知:Ksp(Ag2CrO4)=1.12×10-12)。
①氨的测定:精确称取wgX,加适量水溶解,注入圆底烧瓶中,然后逐滴加入足量10%NaOH溶液,通入水蒸气,将样品溶液中的氨全部蒸出,用V1mL c1mol·L-1的盐酸溶液吸收。蒸氨结束后取下接收瓶,用c2mol·L-1 NaOH标准溶液滴定过剩的HCl,到终点时消耗V2mLNaOH溶液。
②氯的测定:准确称取样品X配成溶液后用AgNO3标准溶液滴定,K2CrO4溶液为指示剂,至出现砖红色沉淀不再消失为终点(Ag2CrO4为砖红色)。
回答下列问题:
(1)用NaOH标准溶液滴定过剩的HCl时,应使用
(2)样品中氨的质量分数表达式为
(3)滴定终点时,若溶液中c(Ag+)=2.0×10-5mol·L-1 ,c(CrO42-)为
您最近一年使用:0次
名校
解题方法
7 . 某化学活动小组按下图所示流程由粗氧化铜样品(含少量氧化亚铁及不溶于酸的杂质)制取无水硫酸铜。
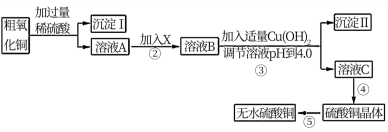
已知Fe3+、Cu2+、Fe2+三种离子在水溶液中形成氢氧化物沉淀的pH范围如下图所示:
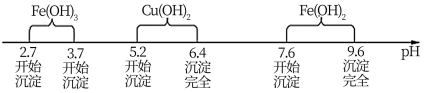
请回答下列问题:
(1)在整个实验过程中,下列实验装置不可能用到的是________ (填序号)。

(2)溶液A中所含溶质为________ ;物质X应选用________ (填序号)。
①氯水 ②双氧水 ③铁粉 ④高锰酸钾
(3)从溶液C中制取硫酸铜晶体的实验操作为______________________________ 。
(4)用“间接碘量法”可以测定溶液A(不含能与I-发生反应的杂质)中Cu2+的浓度。过程如下:
第一步:移取10.00 mL溶液A于100 mL容量瓶中,加水定容至100 mL。
第二步:取稀释后溶液20.00 mL于锥形瓶中,加入过量KI固体,充分反应生成白色沉淀与碘单质。
第三步:以淀粉溶液为指示剂,用0.050 00 mol·L-1的Na2S2O3标准溶液滴定,前后共测定三次,达到滴定终点时,消耗Na2S2O3标准溶液的体积如下表:(已知:I2+2S2O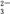 ===2I-+S4O
===2I-+S4O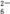 )
)
①CuSO4溶液与KI的反应的离子方程式为______________________________ 。
②滴定中,Na2S2O3标准溶液应放在________ (填“酸式滴定管”或“碱式滴定管”)中,滴定终点的现象是______________________________ 。
③溶液A中c(Cu2+)=________ mol·L-1。

已知Fe3+、Cu2+、Fe2+三种离子在水溶液中形成氢氧化物沉淀的pH范围如下图所示:

请回答下列问题:
(1)在整个实验过程中,下列实验装置不可能用到的是

(2)溶液A中所含溶质为
①氯水 ②双氧水 ③铁粉 ④高锰酸钾
(3)从溶液C中制取硫酸铜晶体的实验操作为
(4)用“间接碘量法”可以测定溶液A(不含能与I-发生反应的杂质)中Cu2+的浓度。过程如下:
第一步:移取10.00 mL溶液A于100 mL容量瓶中,加水定容至100 mL。
第二步:取稀释后溶液20.00 mL于锥形瓶中,加入过量KI固体,充分反应生成白色沉淀与碘单质。
第三步:以淀粉溶液为指示剂,用0.050 00 mol·L-1的Na2S2O3标准溶液滴定,前后共测定三次,达到滴定终点时,消耗Na2S2O3标准溶液的体积如下表:(已知:I2+2S2O
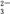 ===2I-+S4O
===2I-+S4O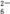 )
)| 滴定次数 | 第一次 | 第二次 | 第三次 |
| 滴定前读数(mL) | 0.10 | 0.36 | 1.10 |
| 滴定后读数(mL) | 20.12 | 20.34 | 22.12 |
①CuSO4溶液与KI的反应的离子方程式为
②滴定中,Na2S2O3标准溶液应放在
③溶液A中c(Cu2+)=
您最近一年使用:0次
解题方法
8 . 碘化亚铜(CuI)是阳极射线管复盖物,也是重要的有机反应催化剂,不溶于水和乙醇。下图是用废铜电缆(杂质中含有少量铁)制取无水碘化亚铜的流程。

(1)过程①得到的溶液呈蓝色,其原因是______ (用化学方程式表示),当温度高于40℃时,过程①反应速率减慢,原因是________________ 。
(2)过程②调节溶液pH适宜选用的试剂是_______ (填正确答案的字母编号);已知25℃时,Cu(OH)2的Ksp=2.2×10-20,Fe(OH)3的Ksp=4×10-35,lg2=0.30,则过程②调节溶液PH时,溶液的PH不小于________ 。
A.NaOH B.NH3·H2O C.CuO D.CuCO3
(3)过程③的氧化产物能使淀粉变蓝,对应的离子方程式为________________ 。
(4)过程④用乙醇洗涤沉淀的目的为________________ 。
(5)准确称取mg CuI样品,加入足量的Fe2(SO4)3溶液中,CuI被完全氧化生成Cu2+和I2。待样品完全反应后,用amol/L酸性KMnO4溶液滴定,达到终点时,消耗酸性KMnO4溶液的体积平均值为VmL。则样品中CuI的质量分数为_______ (已知: 5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O)。

(1)过程①得到的溶液呈蓝色,其原因是
(2)过程②调节溶液pH适宜选用的试剂是
A.NaOH B.NH3·H2O C.CuO D.CuCO3
(3)过程③的氧化产物能使淀粉变蓝,对应的离子方程式为
(4)过程④用乙醇洗涤沉淀的目的为
(5)准确称取mg CuI样品,加入足量的Fe2(SO4)3溶液中,CuI被完全氧化生成Cu2+和I2。待样品完全反应后,用amol/L酸性KMnO4溶液滴定,达到终点时,消耗酸性KMnO4溶液的体积平均值为VmL。则样品中CuI的质量分数为
您最近一年使用:0次
9 . 在精制饱和食盐水中加入碳酸氢铵可制备小苏打(NaHCO3),并提取氯化铵作为肥料或进一步提纯为工业氯化铵。完成下列填空:
(1)写出上述制备小苏打的化学方程式__________
(2)滤出小苏打后,母液提取氯化铵有两种方法:
①通入氨,冷却、加食盐,过滤 ②不通氨,冷却、加食盐,过滤
对两种方法的评价正确的是___________ (选填编号)
a.①析出的氯化铵纯度更高 b.②析出的氯化铵纯度更高
c.①的滤液可直接循环使用 d.②的滤液可直接循环使用
(3)提取的NH4Cl中含少量Fe2+、SO42-。将产品溶解,加入H2O2,加热至沸,再加入BaCl2溶液,过滤,蒸发结晶,得到工业氯化铵。
加热至沸的目的是________________ ;滤渣的主要成分是________________ 。
(4)称取1.840g小苏打样品(含少量NaCl),配成250ml溶液,取出25.00ml用0.1000mol/L盐酸滴定,消耗盐酸21.50ml。选甲基橙而不选酚酞作为指示剂的原因是_________ 。
(5)将一定质量小苏打样品(含少量NaCl)溶于足量盐酸,蒸干后称量固体质量,也可测定小苏打的含量。若蒸发过程中有少量液体溅出,则测定结果__ 。(选填“偏高”、“偏低”或“无影响”)
(1)写出上述制备小苏打的化学方程式
(2)滤出小苏打后,母液提取氯化铵有两种方法:
①通入氨,冷却、加食盐,过滤 ②不通氨,冷却、加食盐,过滤
对两种方法的评价正确的是
a.①析出的氯化铵纯度更高 b.②析出的氯化铵纯度更高
c.①的滤液可直接循环使用 d.②的滤液可直接循环使用
(3)提取的NH4Cl中含少量Fe2+、SO42-。将产品溶解,加入H2O2,加热至沸,再加入BaCl2溶液,过滤,蒸发结晶,得到工业氯化铵。
加热至沸的目的是
(4)称取1.840g小苏打样品(含少量NaCl),配成250ml溶液,取出25.00ml用0.1000mol/L盐酸滴定,消耗盐酸21.50ml。选甲基橙而不选酚酞作为指示剂的原因是
(5)将一定质量小苏打样品(含少量NaCl)溶于足量盐酸,蒸干后称量固体质量,也可测定小苏打的含量。若蒸发过程中有少量液体溅出,则测定结果
您最近一年使用:0次
10 . 常温下,向20mL的某稀H2SO4溶液中滴入0.1mol/L氨水,溶液中水电离出氢离子浓度随滴入氨水体积变化如图。下列分析正确的是


| A.E溶液中存在:c(NH4+)>c(SO42-)> c(OH-)> c(H+) |
| B.稀硫酸的浓度为0.1mol/L |
| C.C点溶液pH=14-b |
| D.V2 =20mL |
您最近一年使用:0次
2016-12-09更新
|
247次组卷
|
2卷引用:2016届广西壮族自治区贺州市高三4月模拟考试理科化学试卷



