解题方法
1 . 实验室中有一未知浓度的稀盐酸,某学生为测定盐酸的浓度在实验室中进行如下实验,请完成下列填空:
(1)配制100mL0.1000mol·L-1NaOH标准溶液,配制过程中选用的玻璃仪器主要有烧杯、玻璃棒、量筒、胶头滴管和____ 。
配制好标准液后进行滴定,滴定操作步骤:
①准备:检漏→洗涤→装液→排气泡→读数,其中洗涤先用水洗后____ 。
②滴定:用酸式滴定管取25.00mL待测稀盐酸溶液放入锥形瓶中,并滴加2-3滴酚酞作指示剂,用标准NaOH溶液进行滴定,重复上述滴定操作2-3次。
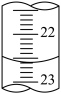
(2)从图中读出NaOH标准液终点滴定管的读数____ mL。
(3)滴定达到终点的标志是____ 。
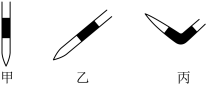
(4)排去碱式滴定管中气泡的方法应采用操作____ ,然后挤压玻璃球使尖嘴部分充满碱液。
(5)在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的有____ 。
(1)配制100mL0.1000mol·L-1NaOH标准溶液,配制过程中选用的玻璃仪器主要有烧杯、玻璃棒、量筒、胶头滴管和
配制好标准液后进行滴定,滴定操作步骤:
①准备:检漏→洗涤→装液→排气泡→读数,其中洗涤先用水洗后
②滴定:用酸式滴定管取25.00mL待测稀盐酸溶液放入锥形瓶中,并滴加2-3滴酚酞作指示剂,用标准NaOH溶液进行滴定,重复上述滴定操作2-3次。
(2)从图中读出NaOH标准液终点滴定管的读数

(3)滴定达到终点的标志是
(4)排去碱式滴定管中气泡的方法应采用操作

(5)在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的有
| A.碱式滴定管尖嘴部分有气泡,滴定后消失 |
| B.滴定终点读数时仰视读数 |
| C.酸式滴定管使用前,水洗后未用待测盐酸溶液润洗 |
| D.锥形瓶水洗后未干燥 |
您最近一年使用:0次
2022-09-21更新
|
108次组卷
|
2卷引用:甘肃省甘南藏族自治州舟曲县第一中学2021-2022学年高二上学期期中考试化学试题
2 . 酸碱盐在水溶液中反应以离子反应为特征,以化学平衡理论为基础。回答下列问题
(1)298K时,在20.0mL0.10mol·L-1氨水中滴入0.10mol·L-1的盐酸,溶液的pH与所加盐酸的体积关系如图所示。已知0.10mol·L-1氨水的电离度为1.32%,下列叙述正确的是_____。

(2)弱电解质的电离是微弱的,电离产生的微粒非常少,并且还要考虑水的电离,而多元弱酸是分步电离的。弱电解质离子的水解损失也是微量的(双水解除外)。比较下列几组溶液中指定微粒浓度的大小。相同浓度的下列溶液①CH3COONH4②CH3COONa③CH3COOH。c(CH3COO-)由大到小的顺序是_____ 。
(3)十二水合硫酸铝钾又称:明矾、白矾、钾矾、钾铝矾、钾明矾,是含有结晶水的硫酸钾和硫酸铝的复盐。主要产地有安徽省,温州矾矿素有“世界矾都”之称。请你用一个离子方程式表示明矾水溶液与NaHCO3溶液混合时发生的离子反应:_____ 。
(4)水解反应的逆反应是中和反应,盐溶液水解一般得到对应的弱酸或者弱碱。氯化铝为无色透明晶体或白色而微带浅黄色的结晶性粉末,易溶于水并强烈水解。将AlCl3溶液蒸干并灼热得到的固体物质是_____ 。
(5)在化学分析中采用K2CrO4为指示剂,以AgNO3标准溶液滴定溶液中的Cl-,利用Ag+与 生成砖红色沉淀,指示到达滴定终点。当溶液中Cl-恰好完全沉淀(浓度等于1.0×10-5mol·L-1)时,此时溶液中c(
生成砖红色沉淀,指示到达滴定终点。当溶液中Cl-恰好完全沉淀(浓度等于1.0×10-5mol·L-1)时,此时溶液中c( )等于
)等于_____ mol·L-1。(已知Ag2CrO4、AgCl的Ksp分别为2.0×10-12和2.0×10-10)
(1)298K时,在20.0mL0.10mol·L-1氨水中滴入0.10mol·L-1的盐酸,溶液的pH与所加盐酸的体积关系如图所示。已知0.10mol·L-1氨水的电离度为1.32%,下列叙述正确的是_____。

| A.该滴定过程应该选择酚酞作为指示剂 |
| B.M点对应的盐酸体积为20.0mL |
C.M点处的溶液中c( )=c(Cl-)=c(H+)=c(OH-) )=c(Cl-)=c(H+)=c(OH-) |
| D.N点处的溶液中pH<12 |
(3)十二水合硫酸铝钾又称:明矾、白矾、钾矾、钾铝矾、钾明矾,是含有结晶水的硫酸钾和硫酸铝的复盐。主要产地有安徽省,温州矾矿素有“世界矾都”之称。请你用一个离子方程式表示明矾水溶液与NaHCO3溶液混合时发生的离子反应:
(4)水解反应的逆反应是中和反应,盐溶液水解一般得到对应的弱酸或者弱碱。氯化铝为无色透明晶体或白色而微带浅黄色的结晶性粉末,易溶于水并强烈水解。将AlCl3溶液蒸干并灼热得到的固体物质是
(5)在化学分析中采用K2CrO4为指示剂,以AgNO3标准溶液滴定溶液中的Cl-,利用Ag+与
 生成砖红色沉淀,指示到达滴定终点。当溶液中Cl-恰好完全沉淀(浓度等于1.0×10-5mol·L-1)时,此时溶液中c(
生成砖红色沉淀,指示到达滴定终点。当溶液中Cl-恰好完全沉淀(浓度等于1.0×10-5mol·L-1)时,此时溶液中c( )等于
)等于
您最近一年使用:0次
名校
3 . 某废水中的铬元素以 和
和 的形式存在,其总铬含量的测定方法如下。
的形式存在,其总铬含量的测定方法如下。
步骤一:取100 mL废水,加热浓缩成20 mL溶液,然后加入NaOH溶液将 转化为
转化为 ;
;
步骤二:加入稍过量的 ,使
,使 在碱性条件下转化成
在碱性条件下转化成 ;
;
步骤三:加入硫酸酸化并煮沸后,加入足量的碘化钾将六价铬还原为 ,同时生成单质
,同时生成单质 。
。
步骤四:以淀粉为指示剂用0.01
 滴定,滴定过程中消耗
滴定,滴定过程中消耗 溶液30.00 mL。
溶液30.00 mL。
已知: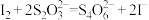 ,请回答:
,请回答:
(1)“步骤二”中 发生反应的离子方程式为
发生反应的离子方程式为___________ 。
(2)“步骤三”中加硫酸酸化时可以观察到溶液颜色变化为___________ 。
(3)在测定过程中,选出正确的滴定操作并排序:检查是否漏水→蒸馏水洗涤→标准液润洗滴定管→___________ →___________ →___________ →___________ →到达滴定终点,停止滴定,记录读数
a.轻轻转动酸式滴定管的活塞,使滴定管尖嘴部分充满溶液,无气泡
b.调整管中液面至“0”或“0”刻度以下,记录读数
c.调整管中液面,用胶头滴管滴加标准液恰好到“0”刻度
d.锥形瓶放于滴定管下,边摇边滴定,眼睛注视锥形瓶内颜色变化
e.装入 溶液至“0”刻度以上2~3 mL,固定好滴定管
溶液至“0”刻度以上2~3 mL,固定好滴定管
f.锥形瓶放于滴定管下,边摇边滴定,眼睛注视滴定管内液面变化
g.将滴定管尖向上弯曲,轻轻挤压玻璃珠使滴定管的尖嘴部分充满溶液至无气泡
(4)该废水中铬元素的质量浓度为___________  。
。
(5)若“步骤三”中省略加热煮沸操作会导致废水中铬元素含量的测量结果偏高。请解释原因:___________
 和
和 的形式存在,其总铬含量的测定方法如下。
的形式存在,其总铬含量的测定方法如下。步骤一:取100 mL废水,加热浓缩成20 mL溶液,然后加入NaOH溶液将
 转化为
转化为 ;
;步骤二:加入稍过量的
 ,使
,使 在碱性条件下转化成
在碱性条件下转化成 ;
;步骤三:加入硫酸酸化并煮沸后,加入足量的碘化钾将六价铬还原为
 ,同时生成单质
,同时生成单质 。
。步骤四:以淀粉为指示剂用0.01

 滴定,滴定过程中消耗
滴定,滴定过程中消耗 溶液30.00 mL。
溶液30.00 mL。已知:
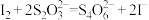 ,请回答:
,请回答:(1)“步骤二”中
 发生反应的离子方程式为
发生反应的离子方程式为(2)“步骤三”中加硫酸酸化时可以观察到溶液颜色变化为
(3)在测定过程中,选出正确的滴定操作并排序:检查是否漏水→蒸馏水洗涤→标准液润洗滴定管→
a.轻轻转动酸式滴定管的活塞,使滴定管尖嘴部分充满溶液,无气泡
b.调整管中液面至“0”或“0”刻度以下,记录读数
c.调整管中液面,用胶头滴管滴加标准液恰好到“0”刻度
d.锥形瓶放于滴定管下,边摇边滴定,眼睛注视锥形瓶内颜色变化
e.装入
 溶液至“0”刻度以上2~3 mL,固定好滴定管
溶液至“0”刻度以上2~3 mL,固定好滴定管f.锥形瓶放于滴定管下,边摇边滴定,眼睛注视滴定管内液面变化
g.将滴定管尖向上弯曲,轻轻挤压玻璃珠使滴定管的尖嘴部分充满溶液至无气泡
(4)该废水中铬元素的质量浓度为
 。
。(5)若“步骤三”中省略加热煮沸操作会导致废水中铬元素含量的测量结果偏高。请解释原因:
您最近一年使用:0次
2021-11-23更新
|
210次组卷
|
2卷引用:甘肃省白银市第八中学2021-2022学年高二上学期第二次月考(11月)化学试题
名校
4 . 常温下用0.10 mol·L-1NaOH溶液分别滴定20.00mL浓度均为0.10mol·L-1CH3COOH(Ka=1.75×10-5)溶液和HCN(Ka=4.9×10-10)溶液所得滴定曲线如图。下列说法正确的是


| A.曲线I和曲线II分别代表的是CH3COOH和HCN |
| B.点③和点④所示溶液中由水电离出的c(H+): ③>④ |
C.点①和点②所示溶液中: |
D.在点②和③之间(不包括端点)存在关系: (A-代表溶液中的酸根离子) (A-代表溶液中的酸根离子) |
您最近一年使用:0次
2021-09-07更新
|
589次组卷
|
5卷引用:甘肃省嘉峪关市第一中学2021届高三下学期七模考试理综化学试题
名校
解题方法
5 . 实验室有一瓶混有氯化钠的氢氧化钠固体试剂,为了测定其纯度,用浓度为0.2mol/L的标准盐酸进行滴定,完成下列问题:

(1)用标准盐酸滴定时,应将标准盐酸注入_________ 中(从图1中选填“甲”或“乙”),该仪器的名称是_____________ .
(2)若用酚酞作指示剂,判断达到滴定终点的现象是___________________________________________ .
(3)图2是某次滴定前、后滴定管中的液面,滴定后盐酸的体积为________ mL.
(4)以下是实验数据记录表
通过计算可得,氢氧化钠的物质的量浓度为____________________ .
(5)下列操作会引起实验结果偏高的是__________ (填编号).
A.滴定开始时读数仰视,终点时读数俯视
B.锥形瓶先用蒸馏水洗涤后,再用待测液润洗
C.滴定前,滴定管尖嘴有气泡,滴定后无气泡
D.在锥形瓶装液前,留有少量蒸馏水

(1)用标准盐酸滴定时,应将标准盐酸注入
(2)若用酚酞作指示剂,判断达到滴定终点的现象是
(3)图2是某次滴定前、后滴定管中的液面,滴定后盐酸的体积为
(4)以下是实验数据记录表
滴定次数 | 待测液体积(mL) | 盐酸的读数(mL) | |
滴定前 | 滴定后 | ||
1 | 10.00 | 0.00 | 19.96 |
2 | 10.00 | 0.10 | 20.14 |
3 | 10.00 | 0.30 | 22.34 |
(5)下列操作会引起实验结果偏高的是
A.滴定开始时读数仰视,终点时读数俯视
B.锥形瓶先用蒸馏水洗涤后,再用待测液润洗
C.滴定前,滴定管尖嘴有气泡,滴定后无气泡
D.在锥形瓶装液前,留有少量蒸馏水
您最近一年使用:0次
2021-01-09更新
|
55次组卷
|
2卷引用:甘肃省兰州市第四片区2020-2021学年高二上学期期末考试化学试题
名校
6 . 滴定实验是化学学科中重要的定量实验。 请回答下列问题:
(1)酸碱中和滴定——用标准盐酸滴定未知浓度的NaOH溶液,下列操作造成测定结果偏高的是______ (填选项字母)
A.滴定终点读数时,俯视滴定管刻度,其他操作正确。
B.盛装未知液的锥形瓶用蒸馏水洗过,未用未知液润洗
C.酸式滴定管用蒸馏水洗净后,未用标准盐酸润洗
D.滴定前,盛装标准液的滴定管尖嘴有气泡,滴定后气泡消失
(2)氧化还原滴定——取一定量的草酸溶液置于锥形瓶中,加入适量稀硫酸,用浓度为0.1000 mol·L-1的高锰酸钾溶液滴定,表格中记录了实验数据:
①滴定时发生的离子反应方程式___________ 。
②KMnO4溶液应装在___________ (填“酸”或“碱”)式滴定管中,滴定终点时滴定现象是___________ 。
③该草酸溶液的物质的量浓度为___________ 。
(3)沉淀滴定――滴定剂和被滴定物的生成物比滴定剂与指示剂的生成物更难溶。参考下表中的数据,若用AgNO3滴定NaCl溶液,可选用的指示剂是___________ (填选项字母)。当Cl-恰好沉淀完全时,此时指示剂也恰好开始显色,请问此时指示剂的物质的量浓度为___________ 。
A.NaSCN B.NaBr C.NaCN D.Na2CrO4
(1)酸碱中和滴定——用标准盐酸滴定未知浓度的NaOH溶液,下列操作造成测定结果偏高的是
A.滴定终点读数时,俯视滴定管刻度,其他操作正确。
B.盛装未知液的锥形瓶用蒸馏水洗过,未用未知液润洗
C.酸式滴定管用蒸馏水洗净后,未用标准盐酸润洗
D.滴定前,盛装标准液的滴定管尖嘴有气泡,滴定后气泡消失
(2)氧化还原滴定——取一定量的草酸溶液置于锥形瓶中,加入适量稀硫酸,用浓度为0.1000 mol·L-1的高锰酸钾溶液滴定,表格中记录了实验数据:
| 滴定次数 | 待测液体积 (mL) | 标准KMnO4溶液体积(mL) | |
| 滴定前读数 | 滴定后读数 | ||
| 第一次 | 25.00 | 0.50 | 20.40 |
| 第二次 | 25.00 | 3.00 | 23.00 |
| 第三次 | 25.00 | 1.00 | 22.50 |
| 第四次 | 25.00 | 4.00 | 24.10 |
②KMnO4溶液应装在
③该草酸溶液的物质的量浓度为
(3)沉淀滴定――滴定剂和被滴定物的生成物比滴定剂与指示剂的生成物更难溶。参考下表中的数据,若用AgNO3滴定NaCl溶液,可选用的指示剂是
| 难溶物 | AgCl | AgBr | AgCN | Ag2CrO4 | AgSCN |
| 颜色 | 白 | 浅黄 | 白 | 砖红 | 白 |
| Ksp | 1.0×10-10 | 5.35×10-13 | 1.21×10-16 | 1.12×10-12 | 1.0×10-12 |
您最近一年使用:0次
2020-12-31更新
|
373次组卷
|
3卷引用:甘肃省天水市一中2021届高三上学期第四次考试理综化学试题
名校
解题方法
7 . 下列关于酸碱中和滴定的叙述中,正确的是( )
| A.进行酸碱中和滴定实验时,盛装待测液的锥形瓶使用前应先用待测液润洗 |
| B.滴定前应排除尖嘴部分的气泡 |
| C.滴定过程中两眼应注视滴定管内液面变化 |
| D.锥形瓶内溶液颜色突变说明到达滴定终点 |
您最近一年使用:0次
2020-02-06更新
|
148次组卷
|
3卷引用:甘肃省武威第十八中学2020-2021学年高二上学期期末考试化学试题
甘肃省武威第十八中学2020-2021学年高二上学期期末考试化学试题云南省丽江市宁蒗县第一中学2019—2020学年高二上学期期末考试化学试题(已下线)3.2.2 酸碱中和滴定(基础练)-2020-2021学年高二化学十分钟同步课堂专练(苏教版选修4)
名校
8 . 某校化学兴趣小组的同学运用滴定法对一含有少量Na2SO4的NaOH样品中NaOH的含量进行测定,请回答下列问题:
(1)用分析天平准确称取该样品5.360g,全部溶于水配制成1000.0mL的溶液。用碱式滴定管取其中20.00mL放在锥形瓶中,滴加几滴甲基橙做指示剂。用标准的盐酸溶液滴定待测的氢氧化钠溶液时,左手把握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视着____ 。滴定终点的现象是____________ 。
(2)下列操作中可能使所测氢氧化钠溶液的浓度数值偏低的是_____ (填写序号)
A.酸式滴定管未用标准盐酸溶液润洗就直接注入标准盐酸溶液
B.滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,滴定结束时俯视读数
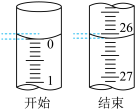
(3)若滴定开始和结束时,酸式滴定管中的液面如图所示:则滴定终点的读数为____ mL。
(4)某学生根据三次实验分别记录有关数据如下:
请选用其中合理的数据列式计算出该样品中NaOH的质量百分含量。(写出计算过程)__
(1)用分析天平准确称取该样品5.360g,全部溶于水配制成1000.0mL的溶液。用碱式滴定管取其中20.00mL放在锥形瓶中,滴加几滴甲基橙做指示剂。用标准的盐酸溶液滴定待测的氢氧化钠溶液时,左手把握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视着
(2)下列操作中可能使所测氢氧化钠溶液的浓度数值偏低的是
A.酸式滴定管未用标准盐酸溶液润洗就直接注入标准盐酸溶液
B.滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,滴定结束时俯视读数
(3)若滴定开始和结束时,酸式滴定管中的液面如图所示:则滴定终点的读数为

(4)某学生根据三次实验分别记录有关数据如下:
| 滴定次数 | 待测氢氧化钠溶液的体积/mL | 0.1000mol/L盐酸的体积(mL) | ||
| 滴定前刻度 | 滴定后刻度 | |||
| 第1次 | 20.00 | 0.00 | 26.01 | |
| 第2次 | 20.00 | 1.56 | 30.30 | |
| 第3次 | 20.00 | 0.22 | 26.21 | |
请选用其中合理的数据列式计算出该样品中NaOH的质量百分含量。(写出计算过程)
您最近一年使用:0次
2019-04-29更新
|
164次组卷
|
4卷引用:甘肃省天水市一中2020-2021学年高二上学期第二学段(期末)考试化学试题
真题
名校
9 . 室温下,用0.l00mol/L NaOH溶液分别滴定20.00 mL 0.100 mol/L的盐酸和醋酸,滴定曲线如图所示。下列说法正确的是
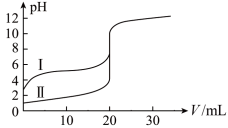

| A.II表示的是滴定醋酸的曲线 |
| B.pH=7时,滴定醋酸消耗的V(NaOH)小于20 mL |
| C.V(NaOH)=" 20.00" mL时,两份溶液中c(Cl-)= C(CH3COO-) |
| D.V(NaOH) ="10.00" mL时,醋酸溶液中c(Na+)> C(CH3COO-)> c(H+)> c(OH-) |
您最近一年使用:0次
2019-01-30更新
|
4228次组卷
|
50卷引用:甘肃省天水市第一中学2020-2021学年高二下学期开学考试化学试题
甘肃省天水市第一中学2020-2021学年高二下学期开学考试化学试题2015-2016学年甘肃省天水一中高二上学期第一次段中考试化学试卷宁夏海原县第一中学2021届高三上学期期末考试化学试题黑龙江省鹤岗市第一中学2021-2022学年高二上学期期中考试化学试题北京市日坛中学2021-2022学年高二上学期期中考试化学试题2014年全国普通高等学校招生统一考试理科综合能力测试化学(海南卷)(已下线)2014-2015学年吉林省延边二中高二上学期期中理科化学卷2015届安徽省芜湖一中高三上学期期末理综化学试卷2014-2015学年河北省正定中学高二下第三次月考化学试卷2015-2016学年山西省怀仁一中高二上11月月考化学试卷2015-2016学年山西省曲沃中学高二上学期12月月考化学试卷2015-2016学年重庆市杨家坪中学高二上学期第三次月考化学试卷2015-2016学年四川省广安市邻水等高二下学期期末联考化学试卷2017届江西省赣中南五校高三上学期第一次模拟考试化学试卷2016-2017学年安徽省六安一中高二上阶段测二化学卷2017届四川省眉山中学高三2月月考理科综合化学试卷安徽省黄山市2016-2017学年高二上学期期末质量检测化学试题湖北省武昌区2017届高三5月调研考试理综化学试题浙江省温州中学2017-2018学年高二上学期期中考试化学试题安徽省淮南市第二中学2017-2018学年高二上学期第二次月考化学试题陕西省西安市长安区第一中学2018届高三上学期第五次质量检测化学试题吉林省辽源市田家炳高级中学等五校2018届高三上学期期末联考化学试题广西陆川中学2017-2018学年高三化学上学期期末考试题江西省抚州市临川区第一中学2018届高三上学期期末考试理综-化学试题福建省莆田第一中学2017-2018学年高二下学期期初考试化学试题内蒙古自治区翁牛特旗乌丹第一中学2018-2019学年高二上学期期中考试化学试题【全国百强校】陕西省西安市长安区第一中学2018-2019学年高二(理)上学期期末考试化学试题【全国百强校】福建省仙游第一中学2018-2019学年高二下学期第一次月考化学试题【区级联考】湖北省武汉市武昌区2019届高三下学期五月调研考试理科综合化学试题(已下线)专题10 水溶液中的离子平衡——2019年高考真题和模拟题化学分项汇编广西桂林十八中2020届高三上学期8月第一次月考化学试题河南省鹤壁市浚县二中2019-2020学年高二上学期第二次月考化学试题苏教版选修四化学反应原理专题3第三单元 盐类的水解 同步检测试卷【全国百强校】广西壮族自治区玉林高级中学2020届高三上学期第一次月考(8月)理综化学试题山西运城市运康中学校2019-2020学年高三12月月考化学试题广东省广州市天河中学2019-2020学年高二上学期能力性考试(11月月考)化学试题2020年春季人教版高中化学选修4第三章《水溶液中的离子平衡》测试卷2020届高三化学二轮冲刺新题专练—混合溶液中微粒浓度大小的比较夯基提能2020届高三化学选择题对题专练——选修4化学反应原理——酸碱中和滴定专题2.3 水溶液中的离子平衡(疑难突破)——巅峰冲刺2020年高考化学二轮专项提升云南省昆明市东川区明月中学2018-2019学年高二下学期期中考试化学试题四川省凉山州2018-2019学年高二下学期期期末考试化学试题陕西省延安市吴起高级中学2020-2021学年高二上学期第一次月考化学试题安徽省池州市第一中学2020-2021学年高二12月月考化学试题陕西省西安市长安区第一中学2017-2018学年高二上学期第四次教学质量检测化学试题湖北省恩施利川市第五中学2019-2020学年高二上学期期中考试化学试题浙江省诸暨市2017-2018学年高一下学期期末考试化学试题 北京市日坛中学2022-2023学年高二上学期期中考试化学试题北京市第二中学2023-2024学年高二上学期第二学段 段考化学试题重庆市璧山来凤中学2023-2024学年高二上学期12月月考化学试题
名校
10 . 某学生用0.1000 mol/L NaOH溶液滴定未知浓度的盐酸溶液,操作可分解为如下几步:
A.用蒸馏水洗干净滴定管;B. 用待测定的溶液润洗酸式滴定管;C.用酸式滴定管取稀盐酸20.00 mL,注入锥形瓶中,加入酚酞;D.另取锥形瓶,再重复操作一次;E.检查滴定管是否漏水;F.取下碱式滴定管用标准的NaOH溶液润洗后,将标准液注入碱式滴定管“0”刻度以上2~3 cm处,再把碱式滴定管固定好,调节液面至“0”刻度或“0”刻度以下;
G.把锥形瓶放在滴定管下面,瓶下垫一张白纸,边滴边摇动锥形瓶直至滴定终点,记下滴定管液面所在刻度。完成以下填空:
(1)正确操作的顺序是(用序号字母填写)_____________ 。
(2)操作F中应该选择图中________ 滴定管(填标号)。

(3)滴定时边滴边摇动锥形瓶,眼睛应观察________ 。
A. 滴定管内液面的变化 B. 锥形瓶内溶液颜色的变化
滴定终点溶液颜色的变化是____________________________ 。
(4)滴定结果如表所示:
滴定中误差较大的是第________ 次实验,造成这种误差的可能原因是________ 。
A. 碱式滴定管在装液前未用标准NaOH溶液润洗2~3次
B. 滴定开始前碱式滴定管尖嘴部分有气泡,在滴定终点读数时未发现气泡
C. 滴定开始前碱式滴定管尖嘴部分没有气泡,在滴定终点读数时发现尖嘴部分有气泡
D. 达到滴定终点时,仰视溶液凹液面最低点读数
E. 滴定过程中,锥形瓶摇荡得太剧烈,以致有些液滴飞溅出来
(5)该盐酸的浓度为________ mol/L。
(6)如果准确移取20.00 mL 0.1000 mol/L NaOH溶液于锥形瓶中,滴入酚酞指示剂,然后用未知浓度的盐酸(装在酸式滴定管中)滴定,是否也可测定出盐酸的物质的量浓度?________ (填“是”或“否”)。
A.用蒸馏水洗干净滴定管;B. 用待测定的溶液润洗酸式滴定管;C.用酸式滴定管取稀盐酸20.00 mL,注入锥形瓶中,加入酚酞;D.另取锥形瓶,再重复操作一次;E.检查滴定管是否漏水;F.取下碱式滴定管用标准的NaOH溶液润洗后,将标准液注入碱式滴定管“0”刻度以上2~3 cm处,再把碱式滴定管固定好,调节液面至“0”刻度或“0”刻度以下;
G.把锥形瓶放在滴定管下面,瓶下垫一张白纸,边滴边摇动锥形瓶直至滴定终点,记下滴定管液面所在刻度。完成以下填空:
(1)正确操作的顺序是(用序号字母填写)
(2)操作F中应该选择图中

(3)滴定时边滴边摇动锥形瓶,眼睛应观察
A. 滴定管内液面的变化 B. 锥形瓶内溶液颜色的变化
滴定终点溶液颜色的变化是
(4)滴定结果如表所示:
| 滴定次数 | 待测溶液体积/mL | 标准溶液的体积/mL | |
| 滴定前刻度 | 滴定后刻度 | ||
| 1 | 20 | 1.02 | 21.03 |
| 2 | 20 | 2.00 | 25.00 |
| 3 | 20 | 0.60 | 20.60 |
滴定中误差较大的是第
A. 碱式滴定管在装液前未用标准NaOH溶液润洗2~3次
B. 滴定开始前碱式滴定管尖嘴部分有气泡,在滴定终点读数时未发现气泡
C. 滴定开始前碱式滴定管尖嘴部分没有气泡,在滴定终点读数时发现尖嘴部分有气泡
D. 达到滴定终点时,仰视溶液凹液面最低点读数
E. 滴定过程中,锥形瓶摇荡得太剧烈,以致有些液滴飞溅出来
(5)该盐酸的浓度为
(6)如果准确移取20.00 mL 0.1000 mol/L NaOH溶液于锥形瓶中,滴入酚酞指示剂,然后用未知浓度的盐酸(装在酸式滴定管中)滴定,是否也可测定出盐酸的物质的量浓度?
您最近一年使用:0次
2018-12-10更新
|
385次组卷
|
6卷引用:甘肃省岷县第二中学2020-2021学年高二上学期期末考试化学试题



