解题方法
1 . 水的电离过程为H2O OH++OH-。在25℃、35℃时水的离子积常数分别为1.0×10-14、2.1×10-14。下列叙述正确的是
OH++OH-。在25℃、35℃时水的离子积常数分别为1.0×10-14、2.1×10-14。下列叙述正确的是
 OH++OH-。在25℃、35℃时水的离子积常数分别为1.0×10-14、2.1×10-14。下列叙述正确的是
OH++OH-。在25℃、35℃时水的离子积常数分别为1.0×10-14、2.1×10-14。下列叙述正确的是| A.水的电离是放热过程 | B.水的电离度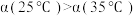 |
C.在35℃时,纯水中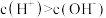 | D.纯水中 随着温度的升高而增大 随着温度的升高而增大 |
您最近一年使用:0次
2024-03-20更新
|
54次组卷
|
4卷引用:河南省开封市2023-2024学年高二上学期11月期中考试化学试题
解题方法
2 . 下列电离方程式中正确的是
A. | B.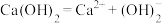 |
C.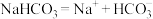 | D.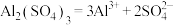 |
您最近一年使用:0次
名校
3 . 已知常温下部分弱电解质的电离平衡常数如下表:
(1)常温下,物质的量浓度相同的三种溶液①NaF溶液;②NaClO溶液;③ 溶液,其pH由大到小的顺序是
溶液,其pH由大到小的顺序是___________ (填序号)。
(2)浓度均为0.1 mol/L① ;②
;② ;③
;③ ;④氨水;⑤
;④氨水;⑤ 五种溶液中,
五种溶液中, 由大到小的顺序
由大到小的顺序___________ (填序号)。
(3)25℃时,将a mol/L的氨水与0.01 mol/L的盐酸等体积混合,反应完后溶液中 ,用含a的代数式表示
,用含a的代数式表示 的电离平衡常数
的电离平衡常数
___________ 。
(4)泡沫灭火器中盛有 、
、 两种溶液,当它们混合时,发生反应的离子方程式为
两种溶液,当它们混合时,发生反应的离子方程式为___________ 。
(5)室温下, 的NaOH溶液和
的NaOH溶液和 的
的 溶液,设由水电离产生的
溶液,设由水电离产生的 的物质的量浓度分别为A和B,则
的物质的量浓度分别为A和B,则 等于
等于___________ 。
(6)亚磷酸溶液中的 H3PO3、H2PO 、HPO
、HPO 的物质的量分数δ(x)随 c(H+)的变化如图所示。
的物质的量分数δ(x)随 c(H+)的变化如图所示。
已知: 。
。

图像中c点c(H3PO3)=c(HPO ),那c点对应的c(H+)=
),那c点对应的c(H+)=___________ mol/L(只列出计算式)。
(7)25℃时,H3PO4的电离常数为Ka1=7.5×10-3,Ka2=6.2×10-8,Ka3=4.4×10-13。足量NaF溶液和H3PO4溶液反应的离子方程式为___________ 。
| 化学式 | HF | HClO |  |  | H3PO3 |
| 电离常数 | 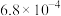 | 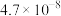 |  ; ; |  | Ka1=5.0×10-2Ka2=2.6×10-7 |
(1)常温下,物质的量浓度相同的三种溶液①NaF溶液;②NaClO溶液;③
 溶液,其pH由大到小的顺序是
溶液,其pH由大到小的顺序是(2)浓度均为0.1 mol/L①
 ;②
;② ;③
;③ ;④氨水;⑤
;④氨水;⑤ 五种溶液中,
五种溶液中, 由大到小的顺序
由大到小的顺序(3)25℃时,将a mol/L的氨水与0.01 mol/L的盐酸等体积混合,反应完后溶液中
 ,用含a的代数式表示
,用含a的代数式表示 的电离平衡常数
的电离平衡常数
(4)泡沫灭火器中盛有
 、
、 两种溶液,当它们混合时,发生反应的离子方程式为
两种溶液,当它们混合时,发生反应的离子方程式为(5)室温下,
 的NaOH溶液和
的NaOH溶液和 的
的 溶液,设由水电离产生的
溶液,设由水电离产生的 的物质的量浓度分别为A和B,则
的物质的量浓度分别为A和B,则 等于
等于(6)亚磷酸溶液中的 H3PO3、H2PO
 、HPO
、HPO 的物质的量分数δ(x)随 c(H+)的变化如图所示。
的物质的量分数δ(x)随 c(H+)的变化如图所示。已知:
 。
。
图像中c点c(H3PO3)=c(HPO
 ),那c点对应的c(H+)=
),那c点对应的c(H+)=(7)25℃时,H3PO4的电离常数为Ka1=7.5×10-3,Ka2=6.2×10-8,Ka3=4.4×10-13。足量NaF溶液和H3PO4溶液反应的离子方程式为
您最近一年使用:0次
4 . 已知25℃时,醋酸、碳酸、氢氰酸的电离平衡常数如下表:
回答下列问题:
(1)25℃时,pH相等的三种溶液①CH3COONa溶液、②Na2CO3溶液、③NaCN溶液,浓度由大到小的顺序为___________ (填序号)。
(2)25℃时,向NaCN溶液中通入少量CO2,反应的离子方程式为___________ 。
(3)将浓度为0.02mol·L-1的HCN与0.01 mol·L-1NaOH溶液等体积混合,则混合溶液中c(H+ )___________ c(OH- )(填“>”、“<”或 “=”)。
(4)常温下,向浓度为0.1mol·L-1、体积为V L的氨水中逐滴加入 一定浓度的盐酸,用pH计测溶液的pH,变化曲线如图所示,d点两种溶液恰好完全反应。根据图中信息回答下列问题:
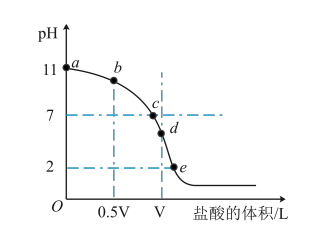
①该温度时NH3·H2O的电离常数Kb≈___________ ;
②b、c、d三点的溶液中,由水电离出的c(H+)由大到小的顺序为___________ ;
③根据以上滴定曲线判断点d所示溶液中:c(Cl-)= c(NH3·H2O)+___________ 。
| 化学式 | CH3COOH | H2CO3 | HCN |
| 电离平衡常数 | Ka=1.8×10-5 | Ka1=4.3×10-7 Ka2=5.6×10-11 | Ka=6.2×10-10 |
(1)25℃时,pH相等的三种溶液①CH3COONa溶液、②Na2CO3溶液、③NaCN溶液,浓度由大到小的顺序为
(2)25℃时,向NaCN溶液中通入少量CO2,反应的离子方程式为
(3)将浓度为0.02mol·L-1的HCN与0.01 mol·L-1NaOH溶液等体积混合,则混合溶液中c(H+ )
(4)常温下,向浓度为0.1mol·L-1、体积为V L的氨水中逐滴加入 一定浓度的盐酸,用pH计测溶液的pH,变化曲线如图所示,d点两种溶液恰好完全反应。根据图中信息回答下列问题:

①该温度时NH3·H2O的电离常数Kb≈
②b、c、d三点的溶液中,由水电离出的c(H+)由大到小的顺序为
③根据以上滴定曲线判断点d所示溶液中:c(Cl-)= c(NH3·H2O)+
您最近一年使用:0次
名校
5 . CH3COOH与CH3COONa等物质的量混合配制成的稀溶液,pH=4.7,下列说法或离子浓度关系正确的是
| A.CH3COONa的水解程度大于CH3COOH的电离程度 |
| B.CH3COONa的存在抑制了CH3COOH的电离 |
| C.c(CH3COO-)>c(Na+)>c(OH-)> c(H+) |
| D.c(CH3COO-)+c(OH-)<c(CH3COOH)+c(H+) |
您最近一年使用:0次
6 . 已知25℃时部分弱电解质的电离平衡常数数据如表所示,回答下列问题:
(1)物质的量浓度均为 的下列四种溶液:
的下列四种溶液: 由小到大排列的顺序是
由小到大排列的顺序是___________ 。
a. b.
b. c.
c. d.
d.
(2)写出向氰化钠溶液中通入少量二氧化碳的离子方程式:___________ 。
(3)25℃时,将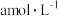 的醋酸溶液与
的醋酸溶液与 氢氧化钠溶液等体积混合。反应后溶液恰好显中性,表示醋酸的电离平衡常数
氢氧化钠溶液等体积混合。反应后溶液恰好显中性,表示醋酸的电离平衡常数
___________ (用含a、b的代数式表示)。
(4)标准状况下将 ,通入
,通入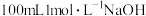 溶液中,用溶液中微粒的浓度符号完成下列等式:
溶液中,用溶液中微粒的浓度符号完成下列等式:
___________ 。
| 化学式 |  |  |  |
| 电离平衡常数 |  |   |  |
(1)物质的量浓度均为
 的下列四种溶液:
的下列四种溶液: 由小到大排列的顺序是
由小到大排列的顺序是a.
 b.
b. c.
c. d.
d.
(2)写出向氰化钠溶液中通入少量二氧化碳的离子方程式:
(3)25℃时,将
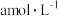 的醋酸溶液与
的醋酸溶液与 氢氧化钠溶液等体积混合。反应后溶液恰好显中性,表示醋酸的电离平衡常数
氢氧化钠溶液等体积混合。反应后溶液恰好显中性,表示醋酸的电离平衡常数
(4)标准状况下将
 ,通入
,通入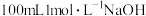 溶液中,用溶液中微粒的浓度符号完成下列等式:
溶液中,用溶液中微粒的浓度符号完成下列等式:
您最近一年使用:0次
7 . 草酸 是一种有机二元弱酸,是植物常具有的成分,具有广泛的用途。草酸晶体
是一种有机二元弱酸,是植物常具有的成分,具有广泛的用途。草酸晶体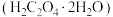 无色,熔点为101℃,易溶于水,受热易脱水、升华,170℃以上分解。常温下它的电离常数
无色,熔点为101℃,易溶于水,受热易脱水、升华,170℃以上分解。常温下它的电离常数 ,
,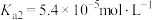 。回答下列问题:
。回答下列问题:
(1)设计实验证明草酸为弱酸的方案及其现象均正确的有_____。
(2)草酸可以使酸性高锰酸钾 溶液褪色,生成
溶液褪色,生成 价锰离子,医学上常用酸性
价锰离子,医学上常用酸性 溶液和草酸
溶液和草酸 溶液反应来测血液中血钙的含量。测定方法是取
溶液反应来测血液中血钙的含量。测定方法是取 血液用蒸馏水稀释后,向其中加入足量的
血液用蒸馏水稀释后,向其中加入足量的 溶液,反应生成
溶液,反应生成 沉淀,将沉淀用稀硫酸溶解得到
沉淀,将沉淀用稀硫酸溶解得到 后,再用
后,再用 溶液滴定。
溶液滴定。
①溶解沉淀时_____ (填“能”或“不能”)用稀盐酸,原因是_____ 。
②滴定过程中发生反应的离子方程式为_____ 。
③若上述滴定中消耗了 的溶液
的溶液 ,则
,则 该血液中含钙
该血液中含钙_____ g。
④下列操作会引起测定结果偏高的是_____ 。
A.滴定管在盛装 溶液前未润洗
溶液前未润洗
B.滴定过程中,锥形瓶振荡的太剧烈,以致部分液体溅出
C.滴定前读数正确,滴定终点时俯视读数
D.装待测液的锥形瓶用蒸馏水洗涤后,没用待测液润洗
(3)常温下,向 溶液中加入
溶液中加入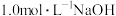 溶液调节
溶液调节 ,加水控制溶液体积为500mL,测得溶液中微粒的分布系数
,加水控制溶液体积为500mL,测得溶液中微粒的分布系数 随
随 变化如图所示。
变化如图所示。

[ ,x代表
,x代表 、
、 或
或 ]
]
 的电离平衡常数Ka2=
的电离平衡常数Ka2=_____ ;当 为4.9时,溶液中
为4.9时,溶液中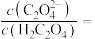
_____ ;M点溶液中 的物质的量浓度为
的物质的量浓度为_____  。
。
 是一种有机二元弱酸,是植物常具有的成分,具有广泛的用途。草酸晶体
是一种有机二元弱酸,是植物常具有的成分,具有广泛的用途。草酸晶体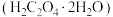 无色,熔点为101℃,易溶于水,受热易脱水、升华,170℃以上分解。常温下它的电离常数
无色,熔点为101℃,易溶于水,受热易脱水、升华,170℃以上分解。常温下它的电离常数 ,
,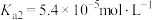 。回答下列问题:
。回答下列问题:(1)设计实验证明草酸为弱酸的方案及其现象均正确的有_____。
A.室温下,取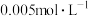 的 的 溶液,测其 溶液,测其 |
B.室温下,取 的 的 溶液,测其pH<7 溶液,测其pH<7 |
C.室温下,取 的 的 溶液稀释100倍后,测其 溶液稀释100倍后,测其 |
D.标准状况下,取 的 的 溶液 溶液 与足量锌粉反应,收集到 与足量锌粉反应,收集到 体积为 体积为 |
(2)草酸可以使酸性高锰酸钾
 溶液褪色,生成
溶液褪色,生成 价锰离子,医学上常用酸性
价锰离子,医学上常用酸性 溶液和草酸
溶液和草酸 溶液反应来测血液中血钙的含量。测定方法是取
溶液反应来测血液中血钙的含量。测定方法是取 血液用蒸馏水稀释后,向其中加入足量的
血液用蒸馏水稀释后,向其中加入足量的 溶液,反应生成
溶液,反应生成 沉淀,将沉淀用稀硫酸溶解得到
沉淀,将沉淀用稀硫酸溶解得到 后,再用
后,再用 溶液滴定。
溶液滴定。①溶解沉淀时
②滴定过程中发生反应的离子方程式为
③若上述滴定中消耗了
 的溶液
的溶液 ,则
,则 该血液中含钙
该血液中含钙④下列操作会引起测定结果偏高的是
A.滴定管在盛装
 溶液前未润洗
溶液前未润洗B.滴定过程中,锥形瓶振荡的太剧烈,以致部分液体溅出
C.滴定前读数正确,滴定终点时俯视读数
D.装待测液的锥形瓶用蒸馏水洗涤后,没用待测液润洗
(3)常温下,向
 溶液中加入
溶液中加入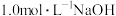 溶液调节
溶液调节 ,加水控制溶液体积为500mL,测得溶液中微粒的分布系数
,加水控制溶液体积为500mL,测得溶液中微粒的分布系数 随
随 变化如图所示。
变化如图所示。
[
 ,x代表
,x代表 、
、 或
或 ]
] 的电离平衡常数Ka2=
的电离平衡常数Ka2= 为4.9时,溶液中
为4.9时,溶液中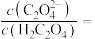
 的物质的量浓度为
的物质的量浓度为 。
。
您最近一年使用:0次
名校
解题方法
8 . 下列说法正确的是
A.酸性: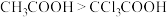 |
| B.HF酸电离平衡正向移动时,其电离程度一定增大 |
C.甲基是推电子基团,所以结合氢离子的能力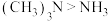 |
D.分子: ,键角: ,键角: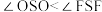 |
您最近一年使用:0次
名校
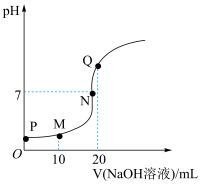
9 . 向20mL0.1mol/L的某酸HA中滴加 ,随NaOH加入溶液pH呈现如下变化。下列说法不正确的是
,随NaOH加入溶液pH呈现如下变化。下列说法不正确的是
 ,随NaOH加入溶液pH呈现如下变化。下列说法不正确的是
,随NaOH加入溶液pH呈现如下变化。下列说法不正确的是
A.P点溶液的 大于1 大于1 | B.M点存在: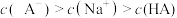 |
C.N点存在: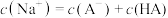 | D.水的电离程度: |
您最近一年使用:0次
2024-03-02更新
|
86次组卷
|
2卷引用:陕西省安康市2023-2024学年高二上学期期末考试化学试题
10 . 醋酸溶液中存在电离平衡CH3COOH CH3COO—+ H+,下列叙述不正确的是
CH3COO—+ H+,下列叙述不正确的是
 CH3COO—+ H+,下列叙述不正确的是
CH3COO—+ H+,下列叙述不正确的是A.升高温度,平衡正向移动,醋酸的电离常数 增大 增大 |
B. 溶液加少量的 溶液加少量的 固体,平衡逆向移动 固体,平衡逆向移动 |
C. 的 的 溶液加水稀释,溶液中 溶液加水稀释,溶液中 减小 减小 |
D.室温下,欲使 醋酸溶液的电离度增大,可加入少量冰醋酸 醋酸溶液的电离度增大,可加入少量冰醋酸 |
您最近一年使用:0次



