草酸 是一种有机二元弱酸,是植物常具有的成分,具有广泛的用途。草酸晶体
是一种有机二元弱酸,是植物常具有的成分,具有广泛的用途。草酸晶体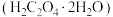 无色,熔点为101℃,易溶于水,受热易脱水、升华,170℃以上分解。常温下它的电离常数
无色,熔点为101℃,易溶于水,受热易脱水、升华,170℃以上分解。常温下它的电离常数 ,
,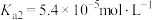 。回答下列问题:
。回答下列问题:
(1)设计实验证明草酸为弱酸的方案及其现象均正确的有_____。
(2)草酸可以使酸性高锰酸钾 溶液褪色,生成
溶液褪色,生成 价锰离子,医学上常用酸性
价锰离子,医学上常用酸性 溶液和草酸
溶液和草酸 溶液反应来测血液中血钙的含量。测定方法是取
溶液反应来测血液中血钙的含量。测定方法是取 血液用蒸馏水稀释后,向其中加入足量的
血液用蒸馏水稀释后,向其中加入足量的 溶液,反应生成
溶液,反应生成 沉淀,将沉淀用稀硫酸溶解得到
沉淀,将沉淀用稀硫酸溶解得到 后,再用
后,再用 溶液滴定。
溶液滴定。
①溶解沉淀时_____ (填“能”或“不能”)用稀盐酸,原因是_____ 。
②滴定过程中发生反应的离子方程式为_____ 。
③若上述滴定中消耗了 的溶液
的溶液 ,则
,则 该血液中含钙
该血液中含钙_____ g。
④下列操作会引起测定结果偏高的是_____ 。
A.滴定管在盛装 溶液前未润洗
溶液前未润洗
B.滴定过程中,锥形瓶振荡的太剧烈,以致部分液体溅出
C.滴定前读数正确,滴定终点时俯视读数
D.装待测液的锥形瓶用蒸馏水洗涤后,没用待测液润洗
(3)常温下,向 溶液中加入
溶液中加入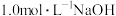 溶液调节
溶液调节 ,加水控制溶液体积为500mL,测得溶液中微粒的分布系数
,加水控制溶液体积为500mL,测得溶液中微粒的分布系数 随
随 变化如图所示。
变化如图所示。

[ ,x代表
,x代表 、
、 或
或 ]
]
 的电离平衡常数Ka2=
的电离平衡常数Ka2=_____ ;当 为4.9时,溶液中
为4.9时,溶液中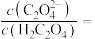
_____ ;M点溶液中 的物质的量浓度为
的物质的量浓度为_____  。
。
 是一种有机二元弱酸,是植物常具有的成分,具有广泛的用途。草酸晶体
是一种有机二元弱酸,是植物常具有的成分,具有广泛的用途。草酸晶体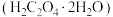 无色,熔点为101℃,易溶于水,受热易脱水、升华,170℃以上分解。常温下它的电离常数
无色,熔点为101℃,易溶于水,受热易脱水、升华,170℃以上分解。常温下它的电离常数 ,
,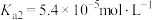 。回答下列问题:
。回答下列问题:(1)设计实验证明草酸为弱酸的方案及其现象均正确的有_____。
A.室温下,取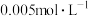 的 的 溶液,测其 溶液,测其 |
B.室温下,取 的 的 溶液,测其pH<7 溶液,测其pH<7 |
C.室温下,取 的 的 溶液稀释100倍后,测其 溶液稀释100倍后,测其 |
D.标准状况下,取 的 的 溶液 溶液 与足量锌粉反应,收集到 与足量锌粉反应,收集到 体积为 体积为 |
(2)草酸可以使酸性高锰酸钾
 溶液褪色,生成
溶液褪色,生成 价锰离子,医学上常用酸性
价锰离子,医学上常用酸性 溶液和草酸
溶液和草酸 溶液反应来测血液中血钙的含量。测定方法是取
溶液反应来测血液中血钙的含量。测定方法是取 血液用蒸馏水稀释后,向其中加入足量的
血液用蒸馏水稀释后,向其中加入足量的 溶液,反应生成
溶液,反应生成 沉淀,将沉淀用稀硫酸溶解得到
沉淀,将沉淀用稀硫酸溶解得到 后,再用
后,再用 溶液滴定。
溶液滴定。①溶解沉淀时
②滴定过程中发生反应的离子方程式为
③若上述滴定中消耗了
 的溶液
的溶液 ,则
,则 该血液中含钙
该血液中含钙④下列操作会引起测定结果偏高的是
A.滴定管在盛装
 溶液前未润洗
溶液前未润洗B.滴定过程中,锥形瓶振荡的太剧烈,以致部分液体溅出
C.滴定前读数正确,滴定终点时俯视读数
D.装待测液的锥形瓶用蒸馏水洗涤后,没用待测液润洗
(3)常温下,向
 溶液中加入
溶液中加入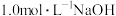 溶液调节
溶液调节 ,加水控制溶液体积为500mL,测得溶液中微粒的分布系数
,加水控制溶液体积为500mL,测得溶液中微粒的分布系数 随
随 变化如图所示。
变化如图所示。
[
 ,x代表
,x代表 、
、 或
或 ]
] 的电离平衡常数Ka2=
的电离平衡常数Ka2= 为4.9时,溶液中
为4.9时,溶液中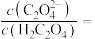
 的物质的量浓度为
的物质的量浓度为 。
。
更新时间:2024-03-12 18:56:41
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】“绿水青山就是金山银山”,运用化学反应原理研究碳、氮、硫的单质及其化合物的反应对工业生产、缓解环境污染、解决能源危机等具有重要意义。
(1)已知:①C(s)+O2(g)=CO2(g) △H1=-393.5kJ/mol
②C(s)+CO2(g)=2CO(g) △H2=+172.5kJ/mol
③4Fe(s)+3O2(g)=2Fe2O3(s) △H3=-1651.0kJ/mol
CO还原氧化铁的热化学方程式为_____________ 。
(2)氢硫酸、碳酸均为二元弱酸,其常温下的电离常数如下表:
①煤的气化过程中产生的有害气体H2S可用足量的Na2CO3溶液吸收,该反应的离子方程式为_______ ;
②常温下,0.1mol·L-1 NaHCO3溶液和0.1mol·L-1 NaHS溶液的pH相比,pH较小的为________ 溶液(填化学式)。
(3)一定条件下,向某恒容密闭容器中充入x mol CO2和y mol H2,发生反应:CO2(g)+3H2(g) ⇌CH3OH(g)+H2O(g) ΔH (此反应在低温时为自发反应)。
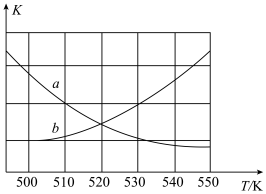
①下图能表示该反应的平衡常数K与温度T之间的变化关系曲线为_____ (填“a”或“b”),其判断依据是__________ 。
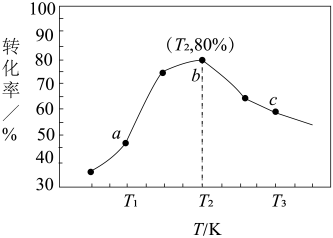
②若x=2、y=3,测得在相同时间内不同温度下H2的转化率如下图所示,则在该时间段内,恰好达到化学平衡时,此时容器内的压强与反应开始时的压强之比为_____________ 。
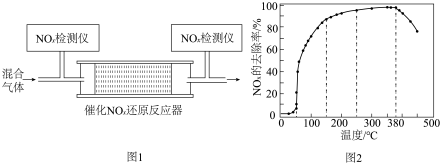
(4)在有氧条件下,新型催化剂M能催化NH3与NOx反应生成N2。
①NH3与NO2生成N2的反应中,当生成28g N2时,转移的电子数为____ mol(结果保留三位有效数字)。
②将一定比例的O2、NH3和NOx的混合气体,匀速通入装有催化剂M的反应器中反应(装置如图1)。反应相同时间NOx的去除率随反应温度的变化曲线如图2所示,在50~250 ℃范围内随着温度的升高,NOx的去除率先迅速上升后上升缓慢的主要原因是______ ;当反应温度高于380 ℃时,NOx的去除率迅速下降的原因可能是____ 。
(1)已知:①C(s)+O2(g)=CO2(g) △H1=-393.5kJ/mol
②C(s)+CO2(g)=2CO(g) △H2=+172.5kJ/mol
③4Fe(s)+3O2(g)=2Fe2O3(s) △H3=-1651.0kJ/mol
CO还原氧化铁的热化学方程式为
(2)氢硫酸、碳酸均为二元弱酸,其常温下的电离常数如下表:
| H2CO3 | H2S | |
| Ka1 | 4.410-7 | 1.310-7 |
| Ka2 | 4.710-11 | 7.110-15 |
①煤的气化过程中产生的有害气体H2S可用足量的Na2CO3溶液吸收,该反应的离子方程式为
②常温下,0.1mol·L-1 NaHCO3溶液和0.1mol·L-1 NaHS溶液的pH相比,pH较小的为
(3)一定条件下,向某恒容密闭容器中充入x mol CO2和y mol H2,发生反应:CO2(g)+3H2(g) ⇌CH3OH(g)+H2O(g) ΔH (此反应在低温时为自发反应)。
①下图能表示该反应的平衡常数K与温度T之间的变化关系曲线为

②若x=2、y=3,测得在相同时间内不同温度下H2的转化率如下图所示,则在该时间段内,恰好达到化学平衡时,此时容器内的压强与反应开始时的压强之比为

(4)在有氧条件下,新型催化剂M能催化NH3与NOx反应生成N2。
①NH3与NO2生成N2的反应中,当生成28g N2时,转移的电子数为
②将一定比例的O2、NH3和NOx的混合气体,匀速通入装有催化剂M的反应器中反应(装置如图1)。反应相同时间NOx的去除率随反应温度的变化曲线如图2所示,在50~250 ℃范围内随着温度的升高,NOx的去除率先迅速上升后上升缓慢的主要原因是

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】最新“人工固氮”的研究报道:常温常压、光照条件下,N2在催化剂表面与某物质发生反应,相应的 K 常数表达式为 
(1)写出相应的化学方程式______
(2)已知该反应的平衡常数K与温度的关系如图,则此反应的正反应_____ (填“吸热”“放热”或“不能确定”)

(3)常温下,如果上述反应在体积不变的密闭容器发生,当反应达到平衡时, (选填编号)。
现向三个体积均为2L的恒容密闭容器Ⅰ、Ⅱ、Ⅲ中,均充入1molN2和3molH2,发生反应3H2(g)+N2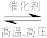 2NH3(g)(正反应放热)。
2NH3(g)(正反应放热)。
(4)三个容器的反应温度分别为 T1、T2、T3且恒定不变。当反应均进行到5min时H2 的体积分数如图所示,其中只有一个容器中的反应已经达到平衡状态。5min时三个容器中的反应达到化学平衡状态的是容器_____ (填序号)。

(5)0~5 min 内容器Ⅰ中用 NH3表示的化学反应速率v(NH3)________ 。
(6)当三个容器中的反应均达到平衡状态时,N2 的转化率最高的是容器____ (填序号,下同);平衡常数最小的是容器_____ 。
(7)将反应生成的混合气体通入水中即可得氨水。用水稀释 0.1mol·L-1氨水, 溶液中随着水量的增加而增大的是 (填字母标号)。

(1)写出相应的化学方程式
(2)已知该反应的平衡常数K与温度的关系如图,则此反应的正反应

(3)常温下,如果上述反应在体积不变的密闭容器发生,当反应达到平衡时, (选填编号)。
| A.容器中气体的平均分子量不随时间而变化 |
| B.v(N2)/ v(O2)=2:3 |
| C.容器中气体的密度不随时间而变化 |
| D.通入稀有气体能提高反应的速率 |
现向三个体积均为2L的恒容密闭容器Ⅰ、Ⅱ、Ⅲ中,均充入1molN2和3molH2,发生反应3H2(g)+N2
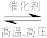 2NH3(g)(正反应放热)。
2NH3(g)(正反应放热)。(4)三个容器的反应温度分别为 T1、T2、T3且恒定不变。当反应均进行到5min时H2 的体积分数如图所示,其中只有一个容器中的反应已经达到平衡状态。5min时三个容器中的反应达到化学平衡状态的是容器

(5)0~5 min 内容器Ⅰ中用 NH3表示的化学反应速率v(NH3)
(6)当三个容器中的反应均达到平衡状态时,N2 的转化率最高的是容器
(7)将反应生成的混合气体通入水中即可得氨水。用水稀释 0.1mol·L-1氨水, 溶液中随着水量的增加而增大的是 (填字母标号)。
A. |
B. |
| C.c(H+)·c(OH-) |
D. |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】次磷酸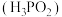 为无色油状液体或易潮解的晶体,易溶于热水、乙醇、乙醚,可用于作杀菌剂、神经系统的强壮剂、金属表面的处理剂,以及生产催化剂和次磷酸盐等。
为无色油状液体或易潮解的晶体,易溶于热水、乙醇、乙醚,可用于作杀菌剂、神经系统的强壮剂、金属表面的处理剂,以及生产催化剂和次磷酸盐等。 次磷酸最多消耗
次磷酸最多消耗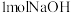 。请回答下列问题:
。请回答下列问题:
(1) 属于
属于___________ (填“正”“酸式”或“碱式”)盐;其在水中的电离方程式为___________ 。
(2)常温下 的次磷酸溶液在加水稀释过程中,下列说法中正确的是___________(填标号)。
的次磷酸溶液在加水稀释过程中,下列说法中正确的是___________(填标号)。
(3)某课外兴趣小组用 的
的 标准溶液滴定
标准溶液滴定 未知浓度的次磷酸溶液,实验过程中记录数据如表,溶液
未知浓度的次磷酸溶液,实验过程中记录数据如表,溶液 、含磷微粒的分布系数
、含磷微粒的分布系数 随滴加
随滴加 溶液体积
溶液体积 (
( 溶液)的变化关系如图所示。
溶液)的变化关系如图所示。

①滴定过程中表示溶液 变化曲线的是
变化曲线的是___________ (填“a”“b”或“c”)。
②下列操作中,可能使所测 溶液的浓度偏低的是
溶液的浓度偏低的是___________ (填标号)。
A.碱式滴定管未用氢氧化钠标准溶液润洗就直接注入标准溶液
B.滴定结束读取氢氧化钠溶液体积时俯视读数
C.滴定前盛放 溶液的锥形瓶用蒸馏水洗净后没有干燥
溶液的锥形瓶用蒸馏水洗净后没有干燥
D.滴定前,碱式滴定管尖嘴部分无气泡,滴定后有气泡
③若选用无色酚酞作指示剂,则到达滴定终点时的标志是___________ 。
④当滴入 溶液的体积为
溶液的体积为 时,溶液呈
时,溶液呈______ (填“酸”“碱”或“中”)性;
_______ (填“>”“<”或“=”) ;根据数据计算,该次磷酸溶液的浓度为
;根据数据计算,该次磷酸溶液的浓度为________  。
。
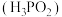 为无色油状液体或易潮解的晶体,易溶于热水、乙醇、乙醚,可用于作杀菌剂、神经系统的强壮剂、金属表面的处理剂,以及生产催化剂和次磷酸盐等。
为无色油状液体或易潮解的晶体,易溶于热水、乙醇、乙醚,可用于作杀菌剂、神经系统的强壮剂、金属表面的处理剂,以及生产催化剂和次磷酸盐等。 次磷酸最多消耗
次磷酸最多消耗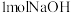 。请回答下列问题:
。请回答下列问题:(1)
 属于
属于(2)常温下
 的次磷酸溶液在加水稀释过程中,下列说法中正确的是___________(填标号)。
的次磷酸溶液在加水稀释过程中,下列说法中正确的是___________(填标号)。A. 的电离程度增大 的电离程度增大 | B.溶液导电性增强 |
| C.溶液中离子总数增多 | D. 的值增大 的值增大 |
(3)某课外兴趣小组用
 的
的 标准溶液滴定
标准溶液滴定 未知浓度的次磷酸溶液,实验过程中记录数据如表,溶液
未知浓度的次磷酸溶液,实验过程中记录数据如表,溶液 、含磷微粒的分布系数
、含磷微粒的分布系数 随滴加
随滴加 溶液体积
溶液体积 (
( 溶液)的变化关系如图所示。
溶液)的变化关系如图所示。| 实验编号 |  溶液浓度/ 溶液浓度/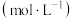 | 滴定完成消耗 溶液的体积/ 溶液的体积/ | 次磷酸溶液的体积/ |
| 1 | 0.1000 | 22.10 | 20.00 |
| 2 | 0.1000 | 24.92 | 20.00 |
| 3 | 0.1000 | 21.90 | 20.00 |

①滴定过程中表示溶液
 变化曲线的是
变化曲线的是②下列操作中,可能使所测
 溶液的浓度偏低的是
溶液的浓度偏低的是A.碱式滴定管未用氢氧化钠标准溶液润洗就直接注入标准溶液
B.滴定结束读取氢氧化钠溶液体积时俯视读数
C.滴定前盛放
 溶液的锥形瓶用蒸馏水洗净后没有干燥
溶液的锥形瓶用蒸馏水洗净后没有干燥D.滴定前,碱式滴定管尖嘴部分无气泡,滴定后有气泡
③若选用无色酚酞作指示剂,则到达滴定终点时的标志是
④当滴入
 溶液的体积为
溶液的体积为 时,溶液呈
时,溶液呈
 ;根据数据计算,该次磷酸溶液的浓度为
;根据数据计算,该次磷酸溶液的浓度为 。
。
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】草酸亚铁(FeC2O4)难溶于水,是合成锂离子电池正极材料磷酸亚铁锂的原料。草酸亚铁可以由(NH4)2Fe(SO4)2和H2C2O4反应得到。
(1)25℃,H2C2O4、HC2O 、C2O
、C2O 的物质的量分数[
的物质的量分数[ ]与pH的关系如下图所示。
]与pH的关系如下图所示。

①NaHC2O4的水解平衡常数Kh=____ 。
②向(NH4)2Fe(SO4)2溶液中加入H2C2O4后有FeC2O4沉淀析出。若测得上层清液中溶液的pH=5.2,c(HC2O )=1×10-3 mol·L-1,则清液中c(Fe2+)=
)=1×10-3 mol·L-1,则清液中c(Fe2+)=____ mol·L-1。[已知Ksp(FeC2O4)=2.0×10-7)]
(2)为测定FeC2O4·xH2O晶体中x的数值,现进行如下实验:称取0.3600 g该晶体于锥形瓶中,加入0.05000 mol·L-1 KMnO4溶液24.00 mL。滴定过程中发生反应如下:MnO +FeC2O4+H+-Mn2++Fe3++CO2↑+H2O(未配平)
+FeC2O4+H+-Mn2++Fe3++CO2↑+H2O(未配平)
①滴定终点的实验现象是____ 。
②开始滴定时,溶液变色较慢,滴定一段时间,溶液变色较快。滴定后期溶液变色较快的原因是____ 。
(1)25℃,H2C2O4、HC2O
 、C2O
、C2O 的物质的量分数[
的物质的量分数[ ]与pH的关系如下图所示。
]与pH的关系如下图所示。
①NaHC2O4的水解平衡常数Kh=
②向(NH4)2Fe(SO4)2溶液中加入H2C2O4后有FeC2O4沉淀析出。若测得上层清液中溶液的pH=5.2,c(HC2O
 )=1×10-3 mol·L-1,则清液中c(Fe2+)=
)=1×10-3 mol·L-1,则清液中c(Fe2+)=(2)为测定FeC2O4·xH2O晶体中x的数值,现进行如下实验:称取0.3600 g该晶体于锥形瓶中,加入0.05000 mol·L-1 KMnO4溶液24.00 mL。滴定过程中发生反应如下:MnO
 +FeC2O4+H+-Mn2++Fe3++CO2↑+H2O(未配平)
+FeC2O4+H+-Mn2++Fe3++CO2↑+H2O(未配平)①滴定终点的实验现象是
②开始滴定时,溶液变色较慢,滴定一段时间,溶液变色较快。滴定后期溶液变色较快的原因是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】25℃和100℃下水的电离平衡曲线如图中所示。

请回答下列问题:
(1)100℃时某溶液中由水电离出的c(H+)为1×10-9 mol/L,则该溶液的pH可能为___________ 。
(2)25℃时对水进行下列操作,能抑制水的电离的是___________ (填选项字母)。
a. 通入适量SO2气体 b. 加入适量硫酸氢钠固体
c. 升温至60℃ d. 加入一小块Na
(3)25℃时,将pH=10的NaOH溶液与pH=2的H2SO4溶液混合,若所得混合溶液的pH=7,则NaOH溶液与H2SO4溶液的体积比为___________ ,100℃时,若10体积pH=a的某强酸溶液与1体积pH=b的某强碱溶液混合后溶液呈中性,则a+b=___________ 。
(4)现有25℃下浓度均为0.1 mol/L的几种溶液:
a. 盐酸 b. 硫酸 c. 氯化铵 d. 氨水 e. NaOH溶液。
①上述5种溶液中,pH从小到大的顺序为___________ (用选项字母表示)。
②将等体积的b、d混合,则溶液的pH___________ 7(真“>”“<”或“=”),混合溶液中各离子浓度的大小关系为:___________ 。若x L的c溶液和y L的d溶液混合后溶液呈中性,则NH3·H2O的电离常数为___________ 。(用含x、y的代数式表示)

请回答下列问题:
(1)100℃时某溶液中由水电离出的c(H+)为1×10-9 mol/L,则该溶液的pH可能为
(2)25℃时对水进行下列操作,能抑制水的电离的是
a. 通入适量SO2气体 b. 加入适量硫酸氢钠固体
c. 升温至60℃ d. 加入一小块Na
(3)25℃时,将pH=10的NaOH溶液与pH=2的H2SO4溶液混合,若所得混合溶液的pH=7,则NaOH溶液与H2SO4溶液的体积比为
(4)现有25℃下浓度均为0.1 mol/L的几种溶液:
a. 盐酸 b. 硫酸 c. 氯化铵 d. 氨水 e. NaOH溶液。
①上述5种溶液中,pH从小到大的顺序为
②将等体积的b、d混合,则溶液的pH
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】高铁酸钾(K2FeO4)是一种绿色氧化剂,在许多领域展现出广阔的应用前景。
(1)湿法制备K2FeO4:在KOH溶液中,用KClO直接氧化Fe(NO3)3即可制得K2FeO4。该反应的离子方程式为_________________________________ 。
(2)测定K2FeO4:样品纯度:i.称取样品mg,加入到盛有过量碱性亚铬酸钠[NaCr(OH)4]溶液的锥形瓶中充分反应;ii.将所得铬酸钠(Na2CrO4)溶液酸化;iii.在所得Na2Cr2O7溶液中加入8—9滴二苯胺磺酸钠溶液作指示剂,用c mol·L-1(NH4)2Fe(SO4)2溶液滴定至终点,消耗溶液体积为V mL。整个过程中发生的反应如下:
ⅰ.___ Cr(OH)4-+___ FeO42- +__ ( ) =__ Fe(OH)3(H2O)3↓+__ CrO42-+__ ( )
ⅱ.2CrO42- + 2H+=Cr2O72- + H2O;
ⅲ.Cr2O72- + 6Fe2+ + 14H+ = 2Cr3+ + 6Fe3+ + 7H2O
①配平方程式i;
②利用上述数据计算该样品的纯度为________________ (用含字母的代数式表示)。
(3)高铁酸盐在水溶液中有四种含铁形体。25℃时,它们的物质的量分数随pH的变化如图所示:
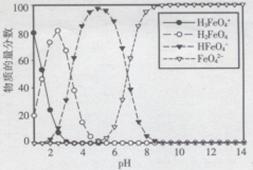
①pH=2.2时,溶液中主要含铁形体浓度的大小关系为________ ;为获得尽可能纯净的高铁酸盐,pH应控制在______________ 。
②已知H3FeO4+的电离常数分别为: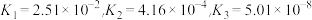
当PH=4时,溶液中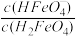 =
=___________ 。
③向pH=6的高铁酸盐溶液中加入KOH溶液,发生反应的离子方程式为______________ 。
(4)某新型电池以金属锂为负极,K2FeO4为正极,溶有LiPF6的有机溶剂为电解质。工作时Li+通过电解质迁移入K2FeO4晶体中,生成K2Li2FeO4。该电池的正极反应式为______________ .
(1)湿法制备K2FeO4:在KOH溶液中,用KClO直接氧化Fe(NO3)3即可制得K2FeO4。该反应的离子方程式为
(2)测定K2FeO4:样品纯度:i.称取样品mg,加入到盛有过量碱性亚铬酸钠[NaCr(OH)4]溶液的锥形瓶中充分反应;ii.将所得铬酸钠(Na2CrO4)溶液酸化;iii.在所得Na2Cr2O7溶液中加入8—9滴二苯胺磺酸钠溶液作指示剂,用c mol·L-1(NH4)2Fe(SO4)2溶液滴定至终点,消耗溶液体积为V mL。整个过程中发生的反应如下:
ⅰ.
ⅱ.2CrO42- + 2H+=Cr2O72- + H2O;
ⅲ.Cr2O72- + 6Fe2+ + 14H+ = 2Cr3+ + 6Fe3+ + 7H2O
①配平方程式i;
②利用上述数据计算该样品的纯度为
(3)高铁酸盐在水溶液中有四种含铁形体。25℃时,它们的物质的量分数随pH的变化如图所示:

①pH=2.2时,溶液中主要含铁形体浓度的大小关系为
②已知H3FeO4+的电离常数分别为:
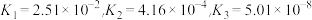
当PH=4时,溶液中
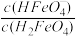 =
=③向pH=6的高铁酸盐溶液中加入KOH溶液,发生反应的离子方程式为
(4)某新型电池以金属锂为负极,K2FeO4为正极,溶有LiPF6的有机溶剂为电解质。工作时Li+通过电解质迁移入K2FeO4晶体中,生成K2Li2FeO4。该电池的正极反应式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】铜及其化合物在工农业生产及日常生活中应用非常广泛.
(1)纳米级Cu2O由于具有优良的催化性能而受到关注,下表为制取Cu2O的三种方法:

①工业上常用方法Ⅱ和方法Ⅲ制取Cu2O而很少用方法I,其原因是____________ 。
②已知:
2Cu(s)+1/2O2(g)═Cu2O(s)△H=-169kJ•mol-1,
C(s)+1/2O2(g)═CO(g)△H=-110.5kJ•mol-1,
Cu(s)+1/2O2(g)═2CuO(s)△H=-157kJ•mol-1
则方法I发生的反应:2CuO(s)+C(s)=Cu20(s)+CO(g); △H=____________ kJ/mol。
(2)氢化亚铜是一种红色固体,可由下列反应制备:4CuSO4+3H3PO2+6H2O=4CuH↓+4H2SO4+3H3PO4.
该反应每转移3mol电子,生成CuH的物质的量为____________ 。
(3)氯化铜溶液中铜各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与c(Cl-) 的关系如图所示。

①当c(Cl-)=9mol•L-1时,溶液中主要的3种含铜物种浓度大小关系为____________ 。
②在c(Cl-)=1mol•L-1的氯化铜溶液中,滴入AgNO3溶液,含铜物种间转化的离子方程式为____________ (任写一个).
(4)已知:Cu(OH)2是二元弱碱;亚磷酸(H3PO3)是二元弱酸,与NaOH溶液反应,生成Na2HPO3.
①在铜盐溶液中Cu2+发生水解反应的平衡常数为____________ ,(已知:25℃时,Ksp[Cu(OH)2]=2.0×10-20mol3•L-3)
②电解Na2HPO3溶液可得到亚磷酸,装置如图(说明:阳膜只允许阳离子通过,阴膜只允许阴离子通过),则产品室中反应的离子方程式为____________ 。
(1)纳米级Cu2O由于具有优良的催化性能而受到关注,下表为制取Cu2O的三种方法:

①工业上常用方法Ⅱ和方法Ⅲ制取Cu2O而很少用方法I,其原因是
②已知:
2Cu(s)+1/2O2(g)═Cu2O(s)△H=-169kJ•mol-1,
C(s)+1/2O2(g)═CO(g)△H=-110.5kJ•mol-1,
Cu(s)+1/2O2(g)═2CuO(s)△H=-157kJ•mol-1
则方法I发生的反应:2CuO(s)+C(s)=Cu20(s)+CO(g); △H=
(2)氢化亚铜是一种红色固体,可由下列反应制备:4CuSO4+3H3PO2+6H2O=4CuH↓+4H2SO4+3H3PO4.
该反应每转移3mol电子,生成CuH的物质的量为
(3)氯化铜溶液中铜各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与c(Cl-) 的关系如图所示。

①当c(Cl-)=9mol•L-1时,溶液中主要的3种含铜物种浓度大小关系为
②在c(Cl-)=1mol•L-1的氯化铜溶液中,滴入AgNO3溶液,含铜物种间转化的离子方程式为
(4)已知:Cu(OH)2是二元弱碱;亚磷酸(H3PO3)是二元弱酸,与NaOH溶液反应,生成Na2HPO3.
①在铜盐溶液中Cu2+发生水解反应的平衡常数为
②电解Na2HPO3溶液可得到亚磷酸,装置如图(说明:阳膜只允许阳离子通过,阴膜只允许阴离子通过),则产品室中反应的离子方程式为

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】含硅元素的化合物广泛存在于自然界中,与其他矿物共同构成岩石.晶体硅(熔点 1410℃)用途广泛,制取与提纯方法有多种.
(1)炼钢开始和结束阶段都可能发生反应:Si+2FeO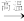 2Fe+SiO2,其目的是
2Fe+SiO2,其目的是________________ .
A.得到副产品硅酸盐水泥 B.制取SiO2,提升钢的硬度
C.除去生铁中过多的Si杂质 D.除过量FeO,防止钢变脆
(2)一种由粗硅制纯硅过程如下:Si(粗)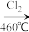 SiCl4
SiCl4 SiCl4(纯)
SiCl4(纯)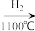 Si(纯),在上述由SiCl4制纯硅的反应中,测得每生成 1.12kg纯硅需吸收a kJ热量,写出该反应的热化学方程式:
Si(纯),在上述由SiCl4制纯硅的反应中,测得每生成 1.12kg纯硅需吸收a kJ热量,写出该反应的热化学方程式:________________ .
对于钠的卤化物(NaX)和硅的卤化物(SiX4)下列叙述正确的是________________
A.NaX易水解
B.SiX4是共价化合物
C.NaX的熔点一般高于SiX4
D.SiF4晶体是由共价键形成的空间网状结构
(3)粗硅经系列反应可生成硅烷(SiH4),硅烷分解也可以生成高纯硅.硅烷的热稳定性弱于甲烷,所以Si元素的非金属性弱于C元素,用原子结构解释其原因:________________ .
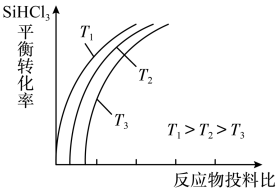
(4)此外,还可以将粗硅转化成三氯氢硅(SiHCl3),通过反应:SiHCl3(g)+H2(g)⇌Si(s)+3HCl(g)制得高纯硅.不同温度下,SiHCl3的平衡转化率随反应物的投料比(反应初始时,各反应物的物质的量之比)的变化关系如图所示.下列说法正确的是________________ (填字母序号).
a.该反应的平衡常数随温度升高而增大
b.横坐标表示的投料比应该是
c.实际生产中为提高SiHCl3的利用率,可适当降低压强
(5)硅元素最高价氧化物对应的水化物是H2SiO3.室温下,0.1mol/L的硅酸钠溶液和0.1mol/L的碳酸钠溶液,碱性更强的是___________ ,其原因是________________ .已知:H2SiO3:Ka1=2.0×10﹣10、Ka2=1.0×10﹣12,H2CO3:Ka1=4.3×10﹣7Ka2=5.6×10 ﹣11.
(1)炼钢开始和结束阶段都可能发生反应:Si+2FeO
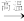 2Fe+SiO2,其目的是
2Fe+SiO2,其目的是A.得到副产品硅酸盐水泥 B.制取SiO2,提升钢的硬度
C.除去生铁中过多的Si杂质 D.除过量FeO,防止钢变脆
(2)一种由粗硅制纯硅过程如下:Si(粗)
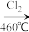 SiCl4
SiCl4 SiCl4(纯)
SiCl4(纯)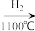 Si(纯),在上述由SiCl4制纯硅的反应中,测得每生成 1.12kg纯硅需吸收a kJ热量,写出该反应的热化学方程式:
Si(纯),在上述由SiCl4制纯硅的反应中,测得每生成 1.12kg纯硅需吸收a kJ热量,写出该反应的热化学方程式:对于钠的卤化物(NaX)和硅的卤化物(SiX4)下列叙述正确的是
A.NaX易水解
B.SiX4是共价化合物
C.NaX的熔点一般高于SiX4
D.SiF4晶体是由共价键形成的空间网状结构
(3)粗硅经系列反应可生成硅烷(SiH4),硅烷分解也可以生成高纯硅.硅烷的热稳定性弱于甲烷,所以Si元素的非金属性弱于C元素,用原子结构解释其原因:
(4)此外,还可以将粗硅转化成三氯氢硅(SiHCl3),通过反应:SiHCl3(g)+H2(g)⇌Si(s)+3HCl(g)制得高纯硅.不同温度下,SiHCl3的平衡转化率随反应物的投料比(反应初始时,各反应物的物质的量之比)的变化关系如图所示.下列说法正确的是

a.该反应的平衡常数随温度升高而增大
b.横坐标表示的投料比应该是

c.实际生产中为提高SiHCl3的利用率,可适当降低压强
(5)硅元素最高价氧化物对应的水化物是H2SiO3.室温下,0.1mol/L的硅酸钠溶液和0.1mol/L的碳酸钠溶液,碱性更强的是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】I.一定温度下,向1L密闭容器中加入1molHI(g),发生反应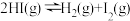 ,H2物质的量随时间的变化如图所示。
,H2物质的量随时间的变化如图所示。

(1)0-2min内的平均反应速率 (HI)=
(HI)=____ 。该温度下, 的平衡常数K=
的平衡常数K=____ 。
(2)相同温度下,若开始入HI(g)的物质的量是原来的2倍,则____ 原来的2倍。
a.平衡常数 b.HI的平衡浓度 c.达到平衡的时间 d.平衡时 的体积分数
的体积分数
(3)上述反应中,正反应速率为 正=k正
正=k正 c2(HI),逆反应速率为
c2(HI),逆反应速率为 逆=k逆
逆=k逆 c(H2)
c(H2) c(I2),其中k正、k逆为速率常数,则k正=
c(I2),其中k正、k逆为速率常数,则k正=____ (以K和k逆表示)。
Ⅱ.已知Ka、Kb、Kw、Kh、Ksp分别表示弱酸的电离平衡常数、弱碱的电离平衡常数、水的离子积常数、盐的水解平衡常数、难溶电解质的溶度积常数。
(1)有关上述常数的说法正确的是________ 。
a.它们都能反映一定条件下对应变化进行的程度
b.它们的大小都随温度的升高而增大
c.常温下,CH3COOH在水中的Ka大于在饱和CH3COONa溶液中的Ka
d.一定温度下,在CH3COONa溶液中,Kw=Ka·Kh
(2)25℃时,将a mol·L-1的氨水与0.01 mol·L-1的盐酸等体积混合所得溶液中c(NH )=c(Cl-),则溶液显
)=c(Cl-),则溶液显_____ 性(填“酸”“碱”或“中”);用含a的代数式表示NH3·H2O的电离平衡常数Kb=________ 。
(3)已知:25℃时,HA的Ka=1×10-6,则25℃时,浓度均为0.01mol·L-1的HA与NaA等体积混合,则混合溶液呈________ 性(填“酸”“碱”或“中”)。
(4)已知常温下Fe(OH)3和Mg(OH)2的Ksp分别为8.0×10-38、1.0×10-11,向浓度均为0.1 mol·L-1的FeCl3、MgCl2的混合溶液中加入碱液,要使Fe3+完全沉淀而Mg2+不沉淀,应该调节溶液的pH范围是________ (已知lg2≈0.3)。
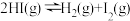 ,H2物质的量随时间的变化如图所示。
,H2物质的量随时间的变化如图所示。
(1)0-2min内的平均反应速率
 (HI)=
(HI)= 的平衡常数K=
的平衡常数K=(2)相同温度下,若开始入HI(g)的物质的量是原来的2倍,则
a.平衡常数 b.HI的平衡浓度 c.达到平衡的时间 d.平衡时
 的体积分数
的体积分数(3)上述反应中,正反应速率为
 正=k正
正=k正 c2(HI),逆反应速率为
c2(HI),逆反应速率为 逆=k逆
逆=k逆 c(H2)
c(H2) c(I2),其中k正、k逆为速率常数,则k正=
c(I2),其中k正、k逆为速率常数,则k正=Ⅱ.已知Ka、Kb、Kw、Kh、Ksp分别表示弱酸的电离平衡常数、弱碱的电离平衡常数、水的离子积常数、盐的水解平衡常数、难溶电解质的溶度积常数。
(1)有关上述常数的说法正确的是
a.它们都能反映一定条件下对应变化进行的程度
b.它们的大小都随温度的升高而增大
c.常温下,CH3COOH在水中的Ka大于在饱和CH3COONa溶液中的Ka
d.一定温度下,在CH3COONa溶液中,Kw=Ka·Kh
(2)25℃时,将a mol·L-1的氨水与0.01 mol·L-1的盐酸等体积混合所得溶液中c(NH
 )=c(Cl-),则溶液显
)=c(Cl-),则溶液显(3)已知:25℃时,HA的Ka=1×10-6,则25℃时,浓度均为0.01mol·L-1的HA与NaA等体积混合,则混合溶液呈
(4)已知常温下Fe(OH)3和Mg(OH)2的Ksp分别为8.0×10-38、1.0×10-11,向浓度均为0.1 mol·L-1的FeCl3、MgCl2的混合溶液中加入碱液,要使Fe3+完全沉淀而Mg2+不沉淀,应该调节溶液的pH范围是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】某化学实验小组用0.2000 mol/L的酸性KMnO4溶液测定草酸晶体的纯度(草酸晶体化学式为H2C2O4·2H2O,杂质不与KMnO4反应)。实验步骤如下:
(1)称取13.0 g草酸晶体,配成250.00 mL水溶液。此操作过程所需用到的仪器是:天平(含砝码)、烧杯、药匙、玻璃棒、胶头滴管和___________
(2)量取草酸溶液25.00 mL放入锥形瓶中,用0.2000 mol/L的酸性KMnO4溶液滴定。
①滴定时,KMnO4溶液应装在___________ (填“酸式”、“碱式”)滴定管中。
②滴定时所发生反应的离子方程式:___________ 。
③滴定达到终点的标志是___________ 。
(3)按正确操作测得有关数据记录如下:

① a的读数如图所示,则a=___________ ;
②草酸晶体的纯度为___________ (结果保留两位小数)。
(4)在上述实验中,下列操作(其它操作正确)一定会造成测定结果偏高的是___________。
(1)称取13.0 g草酸晶体,配成250.00 mL水溶液。此操作过程所需用到的仪器是:天平(含砝码)、烧杯、药匙、玻璃棒、胶头滴管和
(2)量取草酸溶液25.00 mL放入锥形瓶中,用0.2000 mol/L的酸性KMnO4溶液滴定。
①滴定时,KMnO4溶液应装在
②滴定时所发生反应的离子方程式:
③滴定达到终点的标志是
(3)按正确操作测得有关数据记录如下:
| 滴定次数 | 草酸溶液体积 | 酸性KMnO4溶液体积 | |
| 滴定前读数/m L | 滴定后读数/m L | ||
| 第一次 | 25.00 | 0.20 | 20.58 |
| 第二次 | 25.00 | 4.00 | 24.40 |
| 第三次 | 25.00 | 2.38 | a |

① a的读数如图所示,则a=
②草酸晶体的纯度为
(4)在上述实验中,下列操作(其它操作正确)一定会造成测定结果偏高的是___________。
| A.称取13.0 g草酸晶体时,将草酸晶体放在托盘天平右盘 |
| B.锥形瓶水洗后用草酸溶液润洗 |
| C.读取KMnO4溶液体积时,开始仰视读数,滴定结束时俯视读数 |
| D.盛KMnO4溶液的酸式滴定管尖嘴部分有气泡,滴定后气泡消失 |
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】硒被誉为“生命的火种”。亚硒酸钙(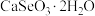 ,难溶于水)常作饲料添加剂,
,难溶于水)常作饲料添加剂, 常作制备含硒营养物质的原料。一种含硒废料制备亚硒酸钙和二氧化硒的流程如图(部分条件和部分产物省略)。回答下列问题:
常作制备含硒营养物质的原料。一种含硒废料制备亚硒酸钙和二氧化硒的流程如图(部分条件和部分产物省略)。回答下列问题:

已知部分信息如下:
①含硒废料的主要成分是 和
和 ,“焙烧”中固体产物为
,“焙烧”中固体产物为 、
、 和
和 ;
;
② 易溶于水,
易溶于水, 难溶于水。
难溶于水。
(1)“焙烧”时常采用逆流操作,即空气从焙烧炉下部通入,废料粉从上部加入,这样操作的目的是___________ 。“焙烧”中被氧化的元素有___________ (填元素符号)。
(2)“浸渣”的主要成分是___________ (填化学式)。
(3)“沉硒”的化学方程式为___________ 。
(4)洗涤产品时,测定洗涤液pH,当pH为7时可认为产品已洗净,其原理是___________ 。
(5)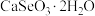 热失重时质量与温度的关系如图所示。
热失重时质量与温度的关系如图所示。

380℃时固体的成分是___________ (填化学式)。
(6)测定 产品纯度。
产品纯度。
称取wg产品溶于水,加入足量 溶液和适量稀硝酸,充分反应后,用
溶液和适量稀硝酸,充分反应后,用 溶液滴定至终点,消耗VmL滴定液。
溶液滴定至终点,消耗VmL滴定液。
发生反应:①
②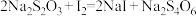
在下列试剂中,宜选择的指示剂为___________ (填标号)。
A. 溶液 B.
溶液 B. 淀粉溶液
淀粉溶液
C. 酚酞溶液 D.
酚酞溶液 D. 甲基橙溶液
甲基橙溶液
该产品中 的质量分数为
的质量分数为___________ %。
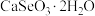 ,难溶于水)常作饲料添加剂,
,难溶于水)常作饲料添加剂, 常作制备含硒营养物质的原料。一种含硒废料制备亚硒酸钙和二氧化硒的流程如图(部分条件和部分产物省略)。回答下列问题:
常作制备含硒营养物质的原料。一种含硒废料制备亚硒酸钙和二氧化硒的流程如图(部分条件和部分产物省略)。回答下列问题:
已知部分信息如下:
①含硒废料的主要成分是
 和
和 ,“焙烧”中固体产物为
,“焙烧”中固体产物为 、
、 和
和 ;
;②
 易溶于水,
易溶于水, 难溶于水。
难溶于水。(1)“焙烧”时常采用逆流操作,即空气从焙烧炉下部通入,废料粉从上部加入,这样操作的目的是
(2)“浸渣”的主要成分是
(3)“沉硒”的化学方程式为
(4)洗涤产品时,测定洗涤液pH,当pH为7时可认为产品已洗净,其原理是
(5)
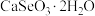 热失重时质量与温度的关系如图所示。
热失重时质量与温度的关系如图所示。
380℃时固体的成分是
(6)测定
 产品纯度。
产品纯度。称取wg产品溶于水,加入足量
 溶液和适量稀硝酸,充分反应后,用
溶液和适量稀硝酸,充分反应后,用 溶液滴定至终点,消耗VmL滴定液。
溶液滴定至终点,消耗VmL滴定液。发生反应:①

②
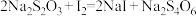
在下列试剂中,宜选择的指示剂为
A.
 溶液 B.
溶液 B. 淀粉溶液
淀粉溶液C.
 酚酞溶液 D.
酚酞溶液 D. 甲基橙溶液
甲基橙溶液该产品中
 的质量分数为
的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】实验室以活性炭为催化剂,由CoCl2制备三氯化六氨合钴(Ⅲ){[Co(NH3)6]Cl3}的装置如图所示:

已知:Ksp[Co(OH)2]=6×10-15;[Co(NH3)6]2+具有较强还原性,Co2+不易被氧化。
回答下列问题:
(1)仪器c的名称是_____ ;d中无水CaCl2的作用是_____ 。
(2)向混合液中先加入浓氨水,目的是_____ ,混合液中NH4Cl的作用是_____ ;充分反应后再加入双氧水,水浴加热,控制温度为55℃的原因是_____ 。
(3)CoCl2制备[Co(NH3)6]Cl3的化学方程式为_____ ;将反应后的混合物趁热过滤,待滤液冷却后加入适量浓盐酸,冰水冷却、抽滤、乙醇洗涤、干燥,得到[Co(NH3)6]Cl3晶体。抽滤采用如图装置。抽滤完毕,接下来的操作为_____ (填选项字母)。抽滤的优点是_____ 。

A.先关闭水龙头,后拔掉橡胶管
B.先拔掉橡胶管,后关闭水龙头
(4)为测定产品中钴的含量,进行下列实验:
Ⅰ.称取3.5400g产品,加入足量NaOH溶液蒸出NH3,再加入稀硫酸,使[Co(NH3)6]Cl3全部转化为Co3+,然后将溶液配制成250mL,取25.00mL于锥形瓶中,加入过量的KI溶液,用0.1000mol·L-1Na2S2O3标准溶液滴定至终点,消耗标准溶液13.30mL。(已知反应2Na2S2O3+I2=Na2S4O6+2NaI)
Ⅱ.另取与步骤Ⅰ中等量的KI溶液于锥形瓶中,用上述标准溶液进行滴定,消耗Na2S2O3标准溶液1.30mL。
①样品中钴元素的质量分数为_____ ;
②若步骤Ⅱ滴定前滴定管内无气泡,滴定后有气泡,会使测定结果_____ (填“偏大”“偏小”或“不变”)。

已知:Ksp[Co(OH)2]=6×10-15;[Co(NH3)6]2+具有较强还原性,Co2+不易被氧化。
回答下列问题:
(1)仪器c的名称是
(2)向混合液中先加入浓氨水,目的是
(3)CoCl2制备[Co(NH3)6]Cl3的化学方程式为

A.先关闭水龙头,后拔掉橡胶管
B.先拔掉橡胶管,后关闭水龙头
(4)为测定产品中钴的含量,进行下列实验:
Ⅰ.称取3.5400g产品,加入足量NaOH溶液蒸出NH3,再加入稀硫酸,使[Co(NH3)6]Cl3全部转化为Co3+,然后将溶液配制成250mL,取25.00mL于锥形瓶中,加入过量的KI溶液,用0.1000mol·L-1Na2S2O3标准溶液滴定至终点,消耗标准溶液13.30mL。(已知反应2Na2S2O3+I2=Na2S4O6+2NaI)
Ⅱ.另取与步骤Ⅰ中等量的KI溶液于锥形瓶中,用上述标准溶液进行滴定,消耗Na2S2O3标准溶液1.30mL。
①样品中钴元素的质量分数为
②若步骤Ⅱ滴定前滴定管内无气泡,滴定后有气泡,会使测定结果
您最近一年使用:0次



