1 . 肼 (N2H4)是一种二元弱碱。常温下,向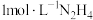 水溶液中滴加盐酸,所得混合溶液中
水溶液中滴加盐酸,所得混合溶液中 或
或 与pH的变化关系如图所示。下列说法错误的是
与pH的变化关系如图所示。下列说法错误的是

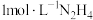 水溶液中滴加盐酸,所得混合溶液中
水溶液中滴加盐酸,所得混合溶液中 或
或 与pH的变化关系如图所示。下列说法错误的是
与pH的变化关系如图所示。下列说法错误的是
A.常温下, 的电离平衡常数 的电离平衡常数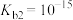 |
B.常温下,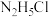 溶液的 溶液的 |
C.M点溶液中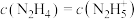 |
D.当溶液 时, 时,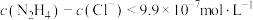 |
您最近一年使用:0次
2024-03-18更新
|
216次组卷
|
3卷引用:2024届河北省百师联盟高三下学期开学摸底联考化学试题
名校
2 . 水是最常用的溶剂,许多化学反应都需要在水溶液中进行,用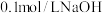 溶液滴定体积均为
溶液滴定体积均为 、浓度均为
、浓度均为 盐酸和醋酸溶液,得到如图所示的滴定曲线,下列说法正确的是
盐酸和醋酸溶液,得到如图所示的滴定曲线,下列说法正确的是

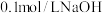 溶液滴定体积均为
溶液滴定体积均为 、浓度均为
、浓度均为 盐酸和醋酸溶液,得到如图所示的滴定曲线,下列说法正确的是
盐酸和醋酸溶液,得到如图所示的滴定曲线,下列说法正确的是
A.用 溶液滴定醋酸溶液通常选择的指示剂为甲基橙,符合其滴定曲线的是Ⅰ 溶液滴定醋酸溶液通常选择的指示剂为甲基橙,符合其滴定曲线的是Ⅰ |
B. 盐酸和醋酸溶液中,由水电离出的 盐酸和醋酸溶液中,由水电离出的 较大的是盐酸 较大的是盐酸 |
C. |
D.曲线Ⅰ中M点对应的溶液中,各离子的浓度由大到小的顺序是 |
您最近一年使用:0次
名校
3 . 常温下,向三元酸 溶液中滴加
溶液中滴加 溶液,溶液中含A微粒的物质的量分数
溶液,溶液中含A微粒的物质的量分数 随溶液pH的变化如图所示,下列说法错误的是
随溶液pH的变化如图所示,下列说法错误的是

 溶液中滴加
溶液中滴加 溶液,溶液中含A微粒的物质的量分数
溶液,溶液中含A微粒的物质的量分数 随溶液pH的变化如图所示,下列说法错误的是
随溶液pH的变化如图所示,下列说法错误的是
A.P为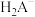 的物质的量分数与溶液pH的关系曲线 的物质的量分数与溶液pH的关系曲线 |
B.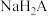 溶液显碱性 溶液显碱性 |
C.滴加 溶液至 溶液至 ,溶液中 ,溶液中 |
D.常温下, 的水解常数为 的水解常数为 |
您最近一年使用:0次
名校
4 . 常温下,下列说法中错误的是
A. 的 的 和 和 混合溶液中: 混合溶液中: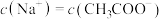 |
B. 溶液中, 溶液中,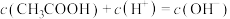 |
C. 的氨水,稀释10倍后,其 的氨水,稀释10倍后,其 ,则 ,则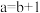 |
D.pH相同的① 、② 、② 、③ 、③ 三种溶液的 三种溶液的 :①>②>③ :①>②>③ |
您最近一年使用:0次
5 . 下列有关说法错误的是
A.等pH等体积的 溶液和 溶液和 溶液,后者中和 溶液,后者中和 的能力更强 的能力更强 |
B.加水稀释 溶液,则溶液中离子浓度都减小 溶液,则溶液中离子浓度都减小 |
C. 溶液pH为4,则 溶液pH为4,则 约为 约为 |
D.向 、 、 的饱和溶液中加入少量 的饱和溶液中加入少量 固体,溶液中 固体,溶液中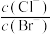 不变 不变 |
您最近一年使用:0次
名校
6 . 在常温下,向0.1mol·L1HR酸溶液中滴加NaOH溶液。混合溶液中存在c(HR)+c(R)=0.1mol·L1,c(HR)、c(R)随溶液pH变化曲线如图所示。下列说法错误的是
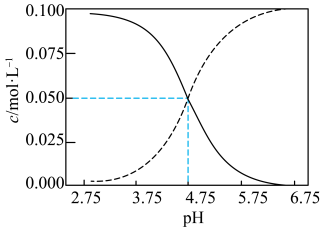

| A.pH=4对应溶液中存在:c(HR)>c(R)>c(H)>c(OH) |
| B.随着c(R)增大,水的电离程度逐渐增大 |
| C.在2L纯水中同时加入0.1molHR、0.1molNaR得到溶液pH=4.75 |
D.常温下,R的水解常数Kh(已知:Kh=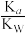 )的数量级为1010 )的数量级为1010 |
您最近一年使用:0次
名校
7 . 已知部分弱酸的电离平衡常数如表所示:
下列离子方程式正确的是
| 弱酸 | CH3COOH | HClO | H2CO3 | H2SO3 |
| 电离平衡常数(25℃) | Ka=1.80×10-5 | Ka=2.95×10-8 | Ka1=4.30×10-7 Ka2=5.60×10-11 | Ka1=1.54×10-2 Ka2=1.02×10-7 |
A.少量CO2通入NaClO溶液中:CO2+H2O+2ClO-= +2HClO +2HClO |
| B.少量SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-=CaSO3↓+2HClO |
C.少量SO2通入Na2CO3溶液中:SO2+H2O+2 = = +2 +2 |
D.相同浓度的NaHCO3溶液与NaHSO3溶液等体积混合:H++ =CO2↑+H2O =CO2↑+H2O |
您最近一年使用:0次
名校
8 . 常温下,某水溶液中二元弱酸 的物质的量浓度为
的物质的量浓度为 ,该溶液中存在
,该溶液中存在 ,通过调节溶液
,通过调节溶液 可使
可使 转化为
转化为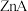 沉淀,体系中
沉淀,体系中 与
与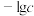 关系如图所示(
关系如图所示( 为
为 、
、 和
和 的浓度,单位为
的浓度,单位为 ),下列说法错误的是
),下列说法错误的是

 的物质的量浓度为
的物质的量浓度为 ,该溶液中存在
,该溶液中存在 ,通过调节溶液
,通过调节溶液 可使
可使 转化为
转化为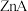 沉淀,体系中
沉淀,体系中 与
与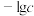 关系如图所示(
关系如图所示( 为
为 、
、 和
和 的浓度,单位为
的浓度,单位为 ),下列说法错误的是
),下列说法错误的是
A.线①表示 |
B.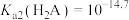 |
C. 的溶液中 的溶液中 |
D. 的溶液中 的溶液中 |
您最近一年使用:0次
名校
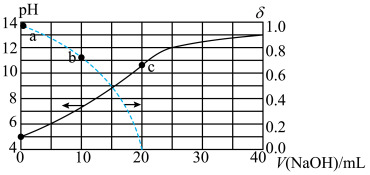
9 . 常温时,用 的
的 溶液滴定20.00mL
溶液滴定20.00mL 的
的 溶液。溶液的
溶液。溶液的 、分布系数
、分布系数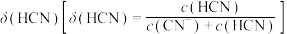 随滴加
随滴加 溶液体积的变化关系如图所示。下列有关说法正确的是
溶液体积的变化关系如图所示。下列有关说法正确的是
 的
的 溶液滴定20.00mL
溶液滴定20.00mL 的
的 溶液。溶液的
溶液。溶液的 、分布系数
、分布系数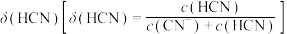 随滴加
随滴加 溶液体积的变化关系如图所示。下列有关说法正确的是
溶液体积的变化关系如图所示。下列有关说法正确的是
A. 酸的 酸的 约为 约为 |
B.b点溶液粒子浓度关系为: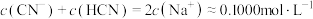 |
C.c点溶液离子浓度关系为: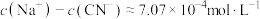 |
D.滴定过程中,水的电离程度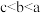 |
您最近一年使用:0次
名校
解题方法
10 . 常温下,向25 mL 0.1 mol⋅L-1NaOH溶液中逐滴加入0.2 mol⋅L-1 溶液,所得滴定曲线如图所示,下列说法错误的是
溶液,所得滴定曲线如图所示,下列说法错误的是

已知:不考虑溶液混合时体积和温度的变化。
 溶液,所得滴定曲线如图所示,下列说法错误的是
溶液,所得滴定曲线如图所示,下列说法错误的是
已知:不考虑溶液混合时体积和温度的变化。
| A.a点溶液中,所含微粒种类共有4种 |
B.b点溶液中,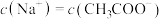 |
C.c点溶液中, |
| D.a→c的过程中,水的电离程度先增大后减小 |
您最近一年使用:0次
2024-03-01更新
|
71次组卷
|
2卷引用:河北省定州市第二中学2023-2024学年高二下学期开学化学试题



