1 . 已知: ,
, 。25℃时,向
。25℃时,向 溶液中滴加
溶液中滴加 的NaOH溶液。溶液中
的NaOH溶液。溶液中 与加入NaOH溶液体积的关系如图所示。下列说法
与加入NaOH溶液体积的关系如图所示。下列说法错误 的是
 ,
, 。25℃时,向
。25℃时,向 溶液中滴加
溶液中滴加 的NaOH溶液。溶液中
的NaOH溶液。溶液中 与加入NaOH溶液体积的关系如图所示。下列说法
与加入NaOH溶液体积的关系如图所示。下列说法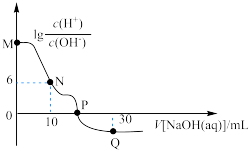
A.M点溶液中存在: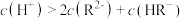 |
B.25℃时. 的水解常数 的水解常数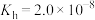 |
| C.P点加入NaOH溶液的体积小于20mL |
D.Q点溶液中存在: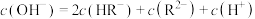 |
您最近一年使用:0次
名校
2 . 向100mL NaOH溶液中通入一定量 充分反应后,向所得溶液中,逐滴滴加1mol/L的盐酸,所得气体的体积与所加盐酸体积的关系如图所示。
充分反应后,向所得溶液中,逐滴滴加1mol/L的盐酸,所得气体的体积与所加盐酸体积的关系如图所示。 充分反应后,所得溶液的溶质为
充分反应后,所得溶液的溶质为___________ (填化学式)。
(2)已知25℃碳酸的 ,
, ,忽略
,忽略 和
和 浓度的变化,在滴加盐酸前,此时溶液pH=
浓度的变化,在滴加盐酸前,此时溶液pH=___________ 。
(3)关于该溶液的表达式正确的是___________。
 充分反应后,向所得溶液中,逐滴滴加1mol/L的盐酸,所得气体的体积与所加盐酸体积的关系如图所示。
充分反应后,向所得溶液中,逐滴滴加1mol/L的盐酸,所得气体的体积与所加盐酸体积的关系如图所示。
 充分反应后,所得溶液的溶质为
充分反应后,所得溶液的溶质为(2)已知25℃碳酸的
 ,
, ,忽略
,忽略 和
和 浓度的变化,在滴加盐酸前,此时溶液pH=
浓度的变化,在滴加盐酸前,此时溶液pH=(3)关于该溶液的表达式正确的是___________。
A. |
B. |
C. |
D. |
您最近一年使用:0次
3 . 已知常温下部分弱电解质的电离平衡常数如表:
(1)常温下,pH相同的三种溶液①NaF溶液;②NaClO溶液;③Na2CO3溶液,其物质的量浓度由大到小的顺序是_______ 。(填序号)
(2)向足量的次氯酸钠中通入少量的二氧化碳的离子方程式_______ 。
(3)室温下,经测定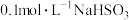 溶液
溶液 ,则
,则
_______  (填“>”、“=”、“<”)。
(填“>”、“=”、“<”)。
(4) 时,将
时,将 的氨水与
的氨水与 的盐酸等体积混合所得溶液中
的盐酸等体积混合所得溶液中 ,则溶液显
,则溶液显_______ (填“酸”“碱”或“中”)性;用含a的代数式表示 的电离平衡常数
的电离平衡常数
_______ 。
(5)将含 的烟气通入该氨水中,当溶液显中性时,溶液中
的烟气通入该氨水中,当溶液显中性时,溶液中
_______ 。
| 化学式 |  |  |  |  |  |
| 电离常数 |  |  |  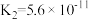 |   |  |
(2)向足量的次氯酸钠中通入少量的二氧化碳的离子方程式
(3)室温下,经测定
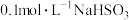 溶液
溶液 ,则
,则
 (填“>”、“=”、“<”)。
(填“>”、“=”、“<”)。(4)
 时,将
时,将 的氨水与
的氨水与 的盐酸等体积混合所得溶液中
的盐酸等体积混合所得溶液中 ,则溶液显
,则溶液显 的电离平衡常数
的电离平衡常数
(5)将含
 的烟气通入该氨水中,当溶液显中性时,溶液中
的烟气通入该氨水中,当溶液显中性时,溶液中
您最近一年使用:0次
名校
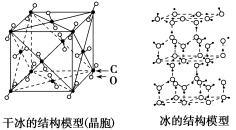
4 . 碳族元素的物质是化学世界中最庞大的家族,“天问一号”轨道飞行器近距离拍摄了火星北极,看到大量白色冰冻区域, 主要是二氧化碳低温凝结形成的干冰,虽然看起来和地球两极很像,但实际温度却比地球两极冷多了!
(1)已知 25℃时,H2CO3的Ka1=4.2×10-7、Ka2=4.8×10- 11,HCN的Ka=4.0×10-10,若向NaCN 溶液中通入少量 CO2,发生反应的离子方程式为___________ 。
(2)下列关于二氧化碳的说法正确的是___________。
(3)干冰和冰的晶体模型如下图存在差别的本质原因___________ 。___________ 。
(5)金刚石晶体中,每个C被___________ 个六元环共用。
(6)晶体硅和碳化硅熔点较高的是___________ (填化学式)。
(7)已知CN-与N2结构相似,推算HCN分子中σ键与π键数目之比为___________ 。
(1)已知 25℃时,H2CO3的Ka1=4.2×10-7、Ka2=4.8×10- 11,HCN的Ka=4.0×10-10,若向NaCN 溶液中通入少量 CO2,发生反应的离子方程式为
(2)下列关于二氧化碳的说法正确的是___________。
A.电子式为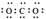 | B.空间填充模型为  |
| C.CO2 是极性分子, 能溶于水 | D.CO2 的水溶液能够导电,但 CO2是非电解质 |
(5)金刚石晶体中,每个C被
(6)晶体硅和碳化硅熔点较高的是
(7)已知CN-与N2结构相似,推算HCN分子中σ键与π键数目之比为
您最近一年使用:0次
名校
5 . 向0.1mol∙L-1FeSO4溶液中持续通入H2S至饱和,有微量黑色的FeS沉淀生成,该溶液中[H2S]=0.1mol∙L-1。(忽略FeSO4浓度的变化和溶液体积的变化)。已知常温下,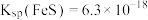 ,H2S的电离常数分别为:
,H2S的电离常数分别为: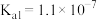 、
、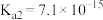 。
。
(1)写出生成黑色沉淀的离子方程式___________ 。
(2)溶液中[S2-]=___________ mol∙L-1;溶液中[H+]=___________ mol∙L-1。
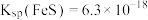 ,H2S的电离常数分别为:
,H2S的电离常数分别为: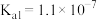 、
、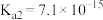 。
。(1)写出生成黑色沉淀的离子方程式
(2)溶液中[S2-]=
您最近一年使用:0次
2024高三下·全国·专题练习
6 . 已知Ka(Kb)、Kw、Kh、Ksp分别表示弱酸的电离平衡常数(弱碱的电离平衡常数)、水的离子积常数、盐的水解平衡常数、难溶电解质的溶度积常数。通过查阅资料获得温度为25℃时以下数据:Kw=1.0×10-14,Ka(CH3COOH)=1.8×10-5,Ka(HSCN)=0.13,Ka(HF)=4.0×10-4,Ksp[Mg(OH)2]=1.8×10-11。
(1)为探究Mg(OH)2在酸中的溶解性,利用以上数据可以计算出反应:Mg(OH)2(s)+2CH3COOH(aq) Mg2+(aq)+2CH3COO-(aq)+2H2O(l)在25℃时的平衡常数K=
Mg2+(aq)+2CH3COO-(aq)+2H2O(l)在25℃时的平衡常数K=___________ ,并据此推断Mg(OH)2___________ (填“能”或“不能”)溶解于醋酸(已知1.83≈5.8)。
(1)为探究Mg(OH)2在酸中的溶解性,利用以上数据可以计算出反应:Mg(OH)2(s)+2CH3COOH(aq)
 Mg2+(aq)+2CH3COO-(aq)+2H2O(l)在25℃时的平衡常数K=
Mg2+(aq)+2CH3COO-(aq)+2H2O(l)在25℃时的平衡常数K=
您最近一年使用:0次
2024高三下·全国·专题练习
解题方法
7 . 天津地处环渤海湾,海水资源丰富。科研人员把铁的配合物 (L为配体)溶于弱碱性的海水中,制成吸收液,将气体
(L为配体)溶于弱碱性的海水中,制成吸收液,将气体 转化为单质硫,改进了湿法脱硫工艺。该工艺包含两个阶段:①
转化为单质硫,改进了湿法脱硫工艺。该工艺包含两个阶段:① 的吸收氧化;②
的吸收氧化;② 的再生。反应原理如下:
的再生。反应原理如下:
①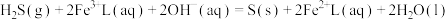

②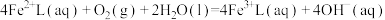
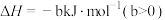
回答下列问题:
(1) 的电离方程式为
的电离方程式为___________ 。25℃时, 溶液中
溶液中 、
、 、
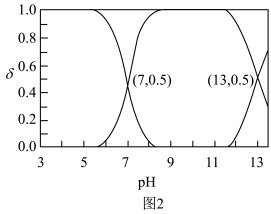
、 在含硫粒子总浓度中所占分数
在含硫粒子总浓度中所占分数 随溶液pH的变化关系如图2,由图2计算,
随溶液pH的变化关系如图2,由图2计算, 的
的
___________ ,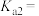
___________ 。再生反应在常温下进行,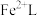 解离出的
解离出的 易与溶液中的
易与溶液中的 形成沉淀。若溶液中的
形成沉淀。若溶液中的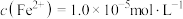 ,
,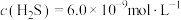 ,为避免有FeS沉淀生成,应控制溶液pH不大于
,为避免有FeS沉淀生成,应控制溶液pH不大于___________ (已知25℃时,FeS的 为
为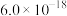 )。
)。
 (L为配体)溶于弱碱性的海水中,制成吸收液,将气体
(L为配体)溶于弱碱性的海水中,制成吸收液,将气体 转化为单质硫,改进了湿法脱硫工艺。该工艺包含两个阶段:①
转化为单质硫,改进了湿法脱硫工艺。该工艺包含两个阶段:① 的吸收氧化;②
的吸收氧化;② 的再生。反应原理如下:
的再生。反应原理如下:①
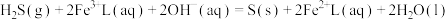

②
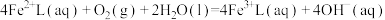
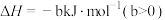
回答下列问题:
(1)
 的电离方程式为
的电离方程式为 溶液中
溶液中 、
、 、
、 在含硫粒子总浓度中所占分数
在含硫粒子总浓度中所占分数 随溶液pH的变化关系如图2,由图2计算,
随溶液pH的变化关系如图2,由图2计算, 的
的
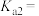
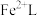 解离出的
解离出的 易与溶液中的
易与溶液中的 形成沉淀。若溶液中的
形成沉淀。若溶液中的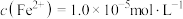 ,
,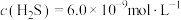 ,为避免有FeS沉淀生成,应控制溶液pH不大于
,为避免有FeS沉淀生成,应控制溶液pH不大于 为
为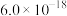 )。
)。
您最近一年使用:0次
2024高三下·全国·专题练习
8 . 一定条件下,水气变换反应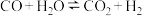 的中间产物是
的中间产物是 。为探究该反应过程,研究
。为探究该反应过程,研究 水溶液在密封石英管中的分解反应:
水溶液在密封石英管中的分解反应:
I.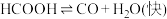
II.
研究发现,在反应I、II中, 仅对反应I有催加速作用;反应I速率远大于反应II,近似认为反应I建立平衡后始终处于平衡状态。忽略水电离,其浓度视为常数。回答下列问题:
仅对反应I有催加速作用;反应I速率远大于反应II,近似认为反应I建立平衡后始终处于平衡状态。忽略水电离,其浓度视为常数。回答下列问题:
(1)反应I正反应速率方程为: ,k为反应速率常数。
,k为反应速率常数。 温度下,
温度下, 电离平衡常数为
电离平衡常数为 ,当
,当 平衡浓度为
平衡浓度为 时,
时, 浓度为
浓度为___________  ,此时反应I的反应速率
,此时反应I的反应速率
___________  (用含
(用含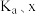 和k的代数式表示)。
和k的代数式表示)。
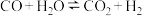 的中间产物是
的中间产物是 。为探究该反应过程,研究
。为探究该反应过程,研究 水溶液在密封石英管中的分解反应:
水溶液在密封石英管中的分解反应:I.
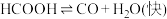
II.

研究发现,在反应I、II中,
 仅对反应I有催加速作用;反应I速率远大于反应II,近似认为反应I建立平衡后始终处于平衡状态。忽略水电离,其浓度视为常数。回答下列问题:
仅对反应I有催加速作用;反应I速率远大于反应II,近似认为反应I建立平衡后始终处于平衡状态。忽略水电离,其浓度视为常数。回答下列问题:(1)反应I正反应速率方程为:
 ,k为反应速率常数。
,k为反应速率常数。 温度下,
温度下, 电离平衡常数为
电离平衡常数为 ,当
,当 平衡浓度为
平衡浓度为 时,
时, 浓度为
浓度为 ,此时反应I的反应速率
,此时反应I的反应速率
 (用含
(用含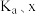 和k的代数式表示)。
和k的代数式表示)。
您最近一年使用:0次
9 . 生物质铁炭纳米材料可以活化过一硫酸盐,降解废水中有机污染物.
(1)生物质铁炭纳米材料活化过—硫酸钾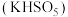 降解有机污染物的反应历程如图-1所示.图中
降解有机污染物的反应历程如图-1所示.图中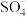 和
和 分别表示硫酸根自由基和羟基自由基.
分别表示硫酸根自由基和羟基自由基. (S的化合价为
(S的化合价为 )在水中的电离过程为:
)在水中的电离过程为: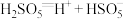 、
、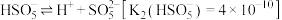 .写出
.写出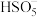 的结构式:
的结构式:_______ 。
②生物质铁炭纳米材料降解有机污染物的机理可描述为______ 。
③若有机污染物为苯酚,写出酸性条件下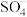 与苯酚反应的化学方程式:
与苯酚反应的化学方程式:______ 。
(2)与直接使用纳米铁颗粒相比,使用生物质铁炭纳米材料降解的优点是:______ 。
(3)铁炭纳米材料在不同 对有机污染物去除率(
对有机污染物去除率( 溶液有机物浓度与初始有机物浓度的比值)的影响如图-2所示,
溶液有机物浓度与初始有机物浓度的比值)的影响如图-2所示, 越小有机污染物去除率越高的原因是:
越小有机污染物去除率越高的原因是:______ 。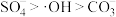 。水中存在一定量
。水中存在一定量 和无
和无 存在时对铁炭纳米材料降解有机污染物的影响如图-3所示.
存在时对铁炭纳米材料降解有机污染物的影响如图-3所示. 的存在对有机污染物的降解有影响,原因是:
的存在对有机污染物的降解有影响,原因是:______ 。
(1)生物质铁炭纳米材料活化过—硫酸钾
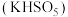 降解有机污染物的反应历程如图-1所示.图中
降解有机污染物的反应历程如图-1所示.图中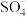 和
和 分别表示硫酸根自由基和羟基自由基.
分别表示硫酸根自由基和羟基自由基.
 (S的化合价为
(S的化合价为 )在水中的电离过程为:
)在水中的电离过程为: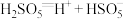 、
、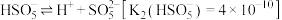 .写出
.写出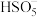 的结构式:
的结构式:②生物质铁炭纳米材料降解有机污染物的机理可描述为
③若有机污染物为苯酚,写出酸性条件下
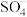 与苯酚反应的化学方程式:
与苯酚反应的化学方程式:(2)与直接使用纳米铁颗粒相比,使用生物质铁炭纳米材料降解的优点是:
(3)铁炭纳米材料在不同
 对有机污染物去除率(
对有机污染物去除率( 溶液有机物浓度与初始有机物浓度的比值)的影响如图-2所示,
溶液有机物浓度与初始有机物浓度的比值)的影响如图-2所示, 越小有机污染物去除率越高的原因是:
越小有机污染物去除率越高的原因是: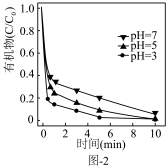
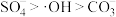 。水中存在一定量
。水中存在一定量 和无
和无 存在时对铁炭纳米材料降解有机污染物的影响如图-3所示.
存在时对铁炭纳米材料降解有机污染物的影响如图-3所示. 的存在对有机污染物的降解有影响,原因是:
的存在对有机污染物的降解有影响,原因是: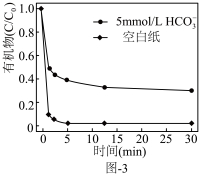
您最近一年使用:0次
名校
10 . 自然界碳的循环与 、碳酸及碳酸盐有着密切的联系。
、碳酸及碳酸盐有着密切的联系。
(1) 的空间构型为
的空间构型为___________ , 分子中σ键与π键的个数比为
分子中σ键与π键的个数比为___________ 。
(2)常温常压下,空气中 溶于水达到平衡时
溶于水达到平衡时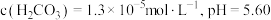 。若忽略水的电离及
。若忽略水的电离及 的第二级电离,则碳酸的一级电离常数
的第二级电离,则碳酸的一级电离常数
___________ (已知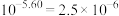 ,结果保留1位小数)。
,结果保留1位小数)。
(3)已知 的二级电离常数
的二级电离常数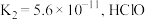 的电离常数
的电离常数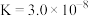 。将少量
。将少量 通入过量的
通入过量的 溶液中,反应的离子方程式为
溶液中,反应的离子方程式为___________ 。
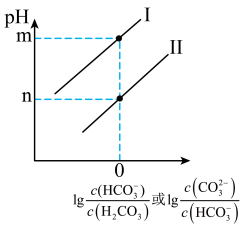
(4)在常温下向 水溶液中滴加
水溶液中滴加 溶液,所得溶液的
溶液,所得溶液的 与粒子浓度的变化关系如图。则下图中
与粒子浓度的变化关系如图。则下图中___________ 线(填“I”或“Ⅱ”)表示 ,碳酸的两级电离常数
,碳酸的两级电离常数 与
与 的关系为
的关系为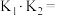
___________ (用含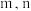 的式子表示)。
的式子表示)。
 、碳酸及碳酸盐有着密切的联系。
、碳酸及碳酸盐有着密切的联系。(1)
 的空间构型为
的空间构型为 分子中σ键与π键的个数比为
分子中σ键与π键的个数比为(2)常温常压下,空气中
 溶于水达到平衡时
溶于水达到平衡时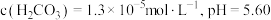 。若忽略水的电离及
。若忽略水的电离及 的第二级电离,则碳酸的一级电离常数
的第二级电离,则碳酸的一级电离常数
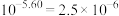 ,结果保留1位小数)。
,结果保留1位小数)。(3)已知
 的二级电离常数
的二级电离常数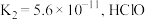 的电离常数
的电离常数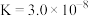 。将少量
。将少量 通入过量的
通入过量的 溶液中,反应的离子方程式为
溶液中,反应的离子方程式为(4)在常温下向
 水溶液中滴加
水溶液中滴加 溶液,所得溶液的
溶液,所得溶液的 与粒子浓度的变化关系如图。则下图中
与粒子浓度的变化关系如图。则下图中 ,碳酸的两级电离常数
,碳酸的两级电离常数 与
与 的关系为
的关系为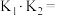
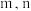 的式子表示)。
的式子表示)。
您最近一年使用:0次
2024-03-16更新
|
158次组卷
|
2卷引用:安徽省合肥市第一中学2023-2024学年高二上学期期末考试化学试题



