名校
1 . 硼酸,化学式H3BO3,为白色结晶性粉末,大量用于玻璃工业,也可用作防腐、消毒剂。硼酸在水中存在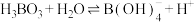 的平衡。下列关于硼酸说法正确的是
的平衡。下列关于硼酸说法正确的是
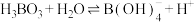 的平衡。下列关于硼酸说法正确的是
的平衡。下列关于硼酸说法正确的是| A.H3BO3是一元弱酸 |
| B.升高温度,该平衡逆向移动 |
| C.滴加少量浓盐酸,该平衡正向移动 |
D.H3BO3和足量的NaOH溶液反应: |
您最近一年使用:0次
2023-11-12更新
|
326次组卷
|
2卷引用:天津市部分区2023-2024学年高二上学期期中考试化学试题
名校
2 . 弱酸型指示剂( )在溶液中存在如下平衡:
)在溶液中存在如下平衡: ,下列有关
,下列有关 溶液说法中正确的是[已知:
溶液说法中正确的是[已知: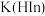 为
为 的电离平衡常数,
的电离平衡常数,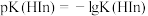 ]
]
 )在溶液中存在如下平衡:
)在溶液中存在如下平衡: ,下列有关
,下列有关 溶液说法中正确的是[已知:
溶液说法中正确的是[已知: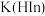 为
为 的电离平衡常数,
的电离平衡常数,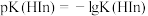 ]
]A.常温下,向 溶液中滴加 溶液中滴加 ,溶液变红 ,溶液变红 |
B.常温下,溶液 减小过程中,上述平衡向右移动 减小过程中,上述平衡向右移动 |
C. 可能是甲基橙指示剂 可能是甲基橙指示剂 |
D.当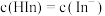 时, 时, 溶液中 溶液中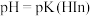 |
您最近一年使用:0次
3 . 甲酸(HCOOH)是一种有机弱酸,通常存在于蜂类、某些蚁类和毛虫的分泌物中。下列关于甲酸溶液的说法正确的是
| A.升高温度,溶液pH增大 |
| B.加水稀释,溶液pH增大 |
| C.加入少量NaOH固体,溶液pH减小 |
| D.加入少量HCOONa固体,溶液pH减小 |
您最近一年使用:0次
解题方法
4 . 25℃时有以下5种溶液:①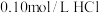 溶液;②
溶液;②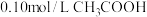 溶液;③
溶液;③ 溶液;④
溶液;④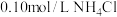 溶液;⑤
溶液;⑤ 溶液。
溶液。
(1)泡沫灭火器中的原料之一是上述5种溶液中的一种,此灭火器灭火的原理为_______ (用离子方程式表示)。
(2)往②加入少量 固体,此溶液的pH
固体,此溶液的pH_______ (填“增大”“减小”或“不变”)。
(3)①和②两种溶液中水的电离程度大小为①_______ ②(填“>”“<”或者“=”)。
(4)将②与③等体积混合后,溶液中存在的离子浓度由大到小的顺序是_______ (用离子符号表示)。
(5)用pH试纸测得④的 ,则此溶液中水电离出来的氢氧根离子浓度为
,则此溶液中水电离出来的氢氧根离子浓度为_______  。
。
(6)用 的标准盐酸滴定50.00mL未知浓度的NaOH溶液的酸碱中和滴定实验中,下列有关说法正确的是_______。
的标准盐酸滴定50.00mL未知浓度的NaOH溶液的酸碱中和滴定实验中,下列有关说法正确的是_______。
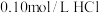 溶液;②
溶液;②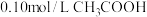 溶液;③
溶液;③ 溶液;④
溶液;④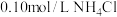 溶液;⑤
溶液;⑤ 溶液。
溶液。(1)泡沫灭火器中的原料之一是上述5种溶液中的一种,此灭火器灭火的原理为
(2)往②加入少量
 固体,此溶液的pH
固体,此溶液的pH(3)①和②两种溶液中水的电离程度大小为①
(4)将②与③等体积混合后,溶液中存在的离子浓度由大到小的顺序是
(5)用pH试纸测得④的
 ,则此溶液中水电离出来的氢氧根离子浓度为
,则此溶液中水电离出来的氢氧根离子浓度为 。
。(6)用
 的标准盐酸滴定50.00mL未知浓度的NaOH溶液的酸碱中和滴定实验中,下列有关说法正确的是_______。
的标准盐酸滴定50.00mL未知浓度的NaOH溶液的酸碱中和滴定实验中,下列有关说法正确的是_______。| A.用蒸馏水洗净酸式滴定管、锥形瓶后可分别直接注入标准盐酸和待测液NaOH溶液 |
| B.滴定时左手旋转滴定管的玻璃活塞,右手不停地摇动锥形瓶,两眼注视滴定管液面变化 |
| C.此中和滴定实验的指示剂可采用酚酞,滴定终点的现象为:溶液由无色变为红色,且30s内颜色不变 |
| D.若滴定前仰视读数、滴定后俯视读数,则所测NaOH溶液的浓度偏低 |
您最近一年使用:0次
2022-11-05更新
|
292次组卷
|
2卷引用:湘湖教育三新探索协作体2022-2023学年高二上学期11月期中联考化学试题
解题方法
5 . 设NA为阿伏加德罗常数的值,下列关于常温下pH=2的H2C2O4溶液的说法错误的是
| A.1L该溶液中的H+数目为0.01NA |
B.c(H+)=c( )+ 2c( )+ 2c( )+c(OH-) )+c(OH-) |
| C.加水稀释,溶液pH增大 |
| D.加入NaHC2O4固体,溶液酸性增强 |
您最近一年使用:0次
6 . 25℃时,下列有关电解质溶液的说法正确的是( )
A.加水稀释0.1mol/L氨水,溶液中c(H+)·c(OH-)和 均不变 均不变 |
| B.配制Fe(NO3)2溶液时,为了防止Fe2+水解可向溶液中加入适量的稀硝酸 |
C.向盐酸中滴加氨水至溶液呈中性,所得溶液中c(NH )=c(Cl-) )=c(Cl-) |
| D.向CH3COOH溶液中加入少量CH3COONa固体,溶液的pH降低 |
您最近一年使用:0次
2020-11-09更新
|
722次组卷
|
2卷引用:北京市丰台区 2020-2021 学年高三上学期期中考试化学试题
7 . 常压下,取不同浓度、不同温度的氨水进行各项内容的测定,得到下表实验数据。
(1)温度升高, 的电离平衡向
的电离平衡向________ (填“左”或“右”)移动,能支持该结论的表中数据是________ (填序号)。
a.电离常数 b.电离度 c. d.
d.
(2)表中 基本不变的原因是
基本不变的原因是________________ 。
(3)常温下,在氨水中加入一定量的氯化铵晶体,下列说法错误的是________ (填序号)。
A.溶液的 增大 B.氨水的电离度减小 C.
增大 B.氨水的电离度减小 C. 减小 D.
减小 D. 减小
减小
温度 | 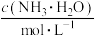 | 电离常数 | 电离度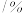 |  |
| 0 | 16.56 | 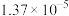 | 9.098 | 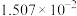 |
| 10 | 15.16 | 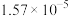 | 10.18 | 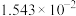 |
| 20 | 13.63 | 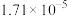 | 11.2 | 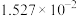 |
(1)温度升高,
 的电离平衡向
的电离平衡向a.电离常数 b.电离度 c.
 d.
d.
(2)表中
 基本不变的原因是
基本不变的原因是(3)常温下,在氨水中加入一定量的氯化铵晶体,下列说法错误的是
A.溶液的
 增大 B.氨水的电离度减小 C.
增大 B.氨水的电离度减小 C. 减小 D.
减小 D. 减小
减小
您最近一年使用:0次
2020-09-14更新
|
394次组卷
|
4卷引用:鲁科版(2019)选择性必修1第3章 物质在水溶液中的行为 第2节 弱电解质的电离 盐类的水解 课时1 弱电解质的电离平衡
鲁科版(2019)选择性必修1第3章 物质在水溶液中的行为 第2节 弱电解质的电离 盐类的水解 课时1 弱电解质的电离平衡人教版(2019)高二选择性必修第一册 第三章 水溶液中的离子反应与平衡 第一节 电离平衡 作业帮(已下线)3.1 电离平衡-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)福建师范大学附属中学2021-2022学年高二上学期期中考试化学试题
8 . 25℃时,下列有关 0.1 mol·L−1 醋酸溶液的说法中,正确的是
| A.pH =1 |
| B.c(H+) = c(CH3COO-) |
| C.加入少量 CH3COONa 固体后,醋酸的电离程度减小 |
| D.加入少量 0.1 mol·L−1 稀盐酸后,醋酸的电离程度增大,溶液 pH 减小 |
您最近一年使用:0次
2020-10-31更新
|
133次组卷
|
2卷引用:北京二中2020-2021学年高二上学期10月月考化学试题
名校
9 . 下列关于 NaOH 溶液和氨水的说法正确的是
| A.相同浓度两溶液中的 c(OH-) 相等 |
| B.pH=13 的两溶液稀释 100 倍,pH 都为 11 |
| C.100 mL 0.1 mol/L 的两溶液能中和等物质的量的盐酸 |
| D.两溶液中分别加入少量对应的 NaOH 固体,c(OH-) 均明显减小 |
您最近一年使用:0次
10 . 已知:25℃时,HCOOH的电离平衡常数K=1.75×10-5,H2CO3的电离平衡常数K1=4.4×10-7、K2=4.7×10-11。下列说法不正确的是( )
| A.向Na2CO3溶液中加入甲酸有气泡产生 |
| B.25℃时,向甲酸溶液中加入NaOH溶液,HCOOH的电离程度和K均增大 |
| C.向甲酸溶液中加入蒸馏水,c(H+)减小 |
| D.向碳酸溶液中加入NaHCO3固体,c(H+)减小 |
您最近一年使用:0次
2020-11-26更新
|
233次组卷
|
2卷引用:陕西省汉中市十校2020-2021学年高二上学期期中校际联考化学试题



