名校
1 . 由下列实验操作和现象,可得出相应正确结论的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向热的浓硝酸中加入红热的木炭,继续加热 | 产生红棕色气体 | 木炭与浓硝酸一定发生了反应 |
| B | 将少量硝酸铜受热分解(产物为CuO、NO2、O2)产生的气体收集后,用带火星的木条检验 | 木条复燃 |  不能支持燃烧 不能支持燃烧 |
| C | 向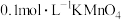 酸性溶液中滴加 酸性溶液中滴加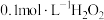 溶液 溶液 | 溶液褪色 |  具有漂白性 具有漂白性 |
| D | 将 溶液与 溶液与 溶液混合 溶液混合 | 生成白色沉淀 | 碱性: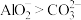 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2 . 常温下, 盐酸分别滴入
盐酸分别滴入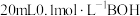 溶液与
溶液与 溶液中,测得溶液的
溶液中,测得溶液的 随滴入盐酸体积变化的图像如图所示。下列说法不正确的是
随滴入盐酸体积变化的图像如图所示。下列说法不正确的是
 盐酸分别滴入
盐酸分别滴入 溶液与
溶液与 溶液中,测得溶液的
溶液中,测得溶液的 随滴入盐酸体积变化的图像如图所示。下列说法不正确的是
随滴入盐酸体积变化的图像如图所示。下列说法不正确的是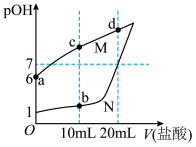
A.常温下, 的电离常数 的电离常数 约为 约为 |
| B.水的电离程度;d>c>a>b |
C.c点: |
| D.b、d点溶液混合后为酸性 |
您最近一年使用:0次
3 . 常温下,二元弱酸 体系中
体系中 [其中X表示
[其中X表示 或
或 ]随溶液
]随溶液 变化如图所示(通过加入
变化如图所示(通过加入 固体调节溶液
固体调节溶液 且忽略溶液体积变化)。下列说法中错误的是
且忽略溶液体积变化)。下列说法中错误的是
 体系中
体系中 [其中X表示
[其中X表示 或
或 ]随溶液
]随溶液 变化如图所示(通过加入
变化如图所示(通过加入 固体调节溶液
固体调节溶液 且忽略溶液体积变化)。下列说法中错误的是
且忽略溶液体积变化)。下列说法中错误的是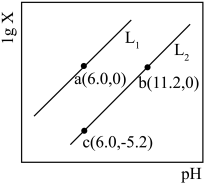
A. 表示 表示 随溶液 随溶液 的变化 的变化 |
B.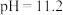 的溶液中存在 的溶液中存在 |
C.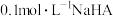 溶液中存在 溶液中存在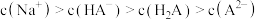 |
D.水的电离程度: |
您最近一年使用:0次
昨日更新
|
14次组卷
|
2卷引用:黑龙江省双鸭山市友谊县高级中学2024届高三下学期普通高中学业水平选择性考试模拟试题-化学试卷
名校
4 . 室温下,用相同浓度的HCl溶液,分别滴定浓度均为0.1mol/L的三种碱(XOH、YOH和ZOH)溶液,滴定曲线如图所示[已知 ]。
]。
 ]。
]。
A.三种碱的电离常数关系: |
B.滴定至M点时,溶液中: |
C. 时,三种溶液中: 时,三种溶液中: |
D.当中和百分数达100%时,将三种溶液混合后: |
您最近一年使用:0次
5 . 常温下,用浓度为 的盐酸滴定浓度均为
的盐酸滴定浓度均为 的
的 和
和 的混合溶液,滴定过程中溶液的
的混合溶液,滴定过程中溶液的 随
随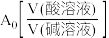 的变化曲线如图所示,下列说法正确的是
的变化曲线如图所示,下列说法正确的是
 的盐酸滴定浓度均为
的盐酸滴定浓度均为 的
的 和
和 的混合溶液,滴定过程中溶液的
的混合溶液,滴定过程中溶液的 随
随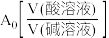 的变化曲线如图所示,下列说法正确的是
的变化曲线如图所示,下列说法正确的是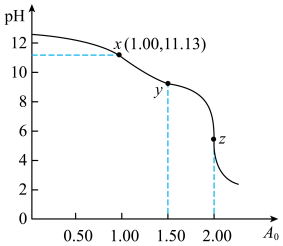
A.该温度下,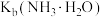 约为 约为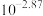 |
B.水的电离程度: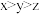 |
C.点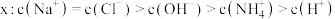 |
D.点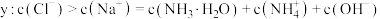 |
您最近一年使用:0次
昨日更新
|
23次组卷
|
2卷引用:黑龙江省部分学校2024届高三下学期第三次模拟化学试题
解题方法
6 . 某实验小组利用AgCl与Na2SO3反应生成 来“分银”,
来“分银”, 及其与
及其与 形成的微粒的浓度分数
形成的微粒的浓度分数 随溶液pH变化的关系如图,下列叙述错误的是(
随溶液pH变化的关系如图,下列叙述错误的是(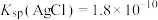 ,
,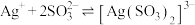 ,
,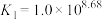 )
)
 来“分银”,
来“分银”, 及其与
及其与 形成的微粒的浓度分数
形成的微粒的浓度分数 随溶液pH变化的关系如图,下列叙述错误的是(
随溶液pH变化的关系如图,下列叙述错误的是(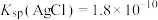 ,
,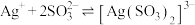 ,
,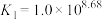 )
)
A.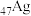 原子的价层电子排布式为 原子的价层电子排布式为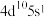 |
B.“分银”溶液中存在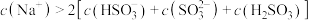 |
| C.“分银”时,需控制pH的范围大约为8~9 |
| D.可以用NaHSO3溶液代替Na2SO3溶液来“分银” |
您最近一年使用:0次
7 . 常温下,已知 溶液中含磷物质的浓度之和为
溶液中含磷物质的浓度之和为 ,溶液中各含磷物质的lgc与pOH的关系如图所示[
,溶液中各含磷物质的lgc与pOH的关系如图所示[ ]。下列说法错误的是
]。下列说法错误的是
 溶液中含磷物质的浓度之和为
溶液中含磷物质的浓度之和为 ,溶液中各含磷物质的lgc与pOH的关系如图所示[
,溶液中各含磷物质的lgc与pOH的关系如图所示[ ]。下列说法错误的是
]。下列说法错误的是
A.曲线②表示 随pOH的变化 随pOH的变化 |
B.pH=7.22的溶液中: |
C.b点时: |
D. 溶液中: 溶液中: |
您最近一年使用:0次
解题方法
8 . 25℃时,已知草酸钠(用 表示)溶液中含碳粒子的物质的量浓度之和为0.1
表示)溶液中含碳粒子的物质的量浓度之和为0.1 ,通入HCl气体调节溶液中的pOH(溶液体积变化忽略不计),溶液中各含碳粒子的pc-pOH关系如图所示。图中pc表示各含碳粒子的物质的量浓度负对数(
,通入HCl气体调节溶液中的pOH(溶液体积变化忽略不计),溶液中各含碳粒子的pc-pOH关系如图所示。图中pc表示各含碳粒子的物质的量浓度负对数( ),pOH表示
),pOH表示 的物质的量浓度负对数[
的物质的量浓度负对数[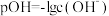 ]。
]。
 表示)溶液中含碳粒子的物质的量浓度之和为0.1
表示)溶液中含碳粒子的物质的量浓度之和为0.1 ,通入HCl气体调节溶液中的pOH(溶液体积变化忽略不计),溶液中各含碳粒子的pc-pOH关系如图所示。图中pc表示各含碳粒子的物质的量浓度负对数(
,通入HCl气体调节溶液中的pOH(溶液体积变化忽略不计),溶液中各含碳粒子的pc-pOH关系如图所示。图中pc表示各含碳粒子的物质的量浓度负对数( ),pOH表示
),pOH表示 的物质的量浓度负对数[
的物质的量浓度负对数[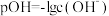 ]。
]。
A.曲线①表示 随pOH的变化 随pOH的变化 | B. |
| C.x点溶液的pH=2.7 | D.pH=7的溶液中: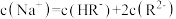 |
您最近一年使用:0次
9 . T K时,现有25 mL含KCl和KCN的溶液,用0.1000 mol⋅L 的硝酸银标准溶液对该混合液进行电位滴定(
的硝酸银标准溶液对该混合液进行电位滴定( 与
与 的反应可以忽略),获得电动势(E)和硝酸银标准溶液体积(V)的电位滴定曲线如图所示,曲线上的转折点即为化学计量点。下列说法不正确的是
的反应可以忽略),获得电动势(E)和硝酸银标准溶液体积(V)的电位滴定曲线如图所示,曲线上的转折点即为化学计量点。下列说法不正确的是 与
与 的反应过程为①
的反应过程为① ,
,
② ;
;
Ⅱ.T K时, ,
, .
.
 的硝酸银标准溶液对该混合液进行电位滴定(
的硝酸银标准溶液对该混合液进行电位滴定( 与
与 的反应可以忽略),获得电动势(E)和硝酸银标准溶液体积(V)的电位滴定曲线如图所示,曲线上的转折点即为化学计量点。下列说法不正确的是
的反应可以忽略),获得电动势(E)和硝酸银标准溶液体积(V)的电位滴定曲线如图所示,曲线上的转折点即为化学计量点。下列说法不正确的是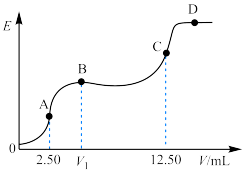
 与
与 的反应过程为①
的反应过程为① ,
,②
 ;
;Ⅱ.T K时,
 ,
, .
.A. ,A→B发生反应: ,A→B发生反应: ; ; |
B.原溶液中, |
C.C点时,溶液中 |
D.D点: |
您最近一年使用:0次
7日内更新
|
28次组卷
|
2卷引用:2024届新高考教学教研联盟高三下学期第一次联考化学试卷
10 . 25℃时,向一定浓度的 溶液中滴加NaOH溶液,混合液中
溶液中滴加NaOH溶液,混合液中 随pOH的变化如图所示,下列说法错误的是
随pOH的变化如图所示,下列说法错误的是 中x表示
中x表示 、
、 、
、 ;
;
② 。
。
 溶液中滴加NaOH溶液,混合液中
溶液中滴加NaOH溶液,混合液中 随pOH的变化如图所示,下列说法错误的是
随pOH的变化如图所示,下列说法错误的是
 中x表示
中x表示 、
、 、
、 ;
;②
 。
。A.曲线III表示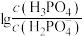 随pOH的变化关系 随pOH的变化关系 |
B.M点时,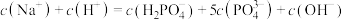 |
C.当溶液 时, 时, |
D. 的平衡常数为 的平衡常数为 |
您最近一年使用:0次



