1 . 常温下,取三份浓度均为 体积均为20mL的醋酸钠溶液,分别向其中滴加浓度均为
体积均为20mL的醋酸钠溶液,分别向其中滴加浓度均为 的氯化铵溶液、醋酸铵溶液和盐酸,滴加过程中溶液的pOH变化曲线如图所示
的氯化铵溶液、醋酸铵溶液和盐酸,滴加过程中溶液的pOH变化曲线如图所示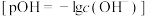 。
。
 体积均为20mL的醋酸钠溶液,分别向其中滴加浓度均为
体积均为20mL的醋酸钠溶液,分别向其中滴加浓度均为 的氯化铵溶液、醋酸铵溶液和盐酸,滴加过程中溶液的pOH变化曲线如图所示
的氯化铵溶液、醋酸铵溶液和盐酸,滴加过程中溶液的pOH变化曲线如图所示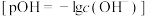 。
。
| A.曲线Ⅰ、Ⅱ、Ⅲ分别代表盐酸、氯化铵溶液和醋酸铵溶液 |
B.常温下 |
C.水的电离程度: |
D.d点存在: |
您最近一年使用:0次
名校
2 . 柠檬酸是一种重要的工业原料,化学式可表示为 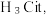 属于三元弱酸。 25℃时,柠檬酸的电离常数分别为:
属于三元弱酸。 25℃时,柠檬酸的电离常数分别为: 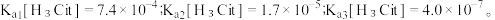
(1)25℃时, 不同pH范围内,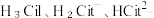 和
和 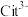 所占的比例 (该微粒浓度与四种微粒浓度之和的比值)如下图所示,则其中代表
所占的比例 (该微粒浓度与四种微粒浓度之和的比值)如下图所示,则其中代表  的曲线是
的曲线是_______ 。
(3)已知25℃时,碳酸的电离常数为: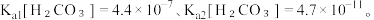 向NaHCO3溶液中加入NaH2Cit溶液,请写出反应的化学方程式
向NaHCO3溶液中加入NaH2Cit溶液,请写出反应的化学方程式_______ 。
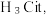 属于三元弱酸。 25℃时,柠檬酸的电离常数分别为:
属于三元弱酸。 25℃时,柠檬酸的电离常数分别为: 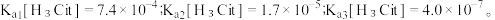
(1)25℃时, 不同pH范围内,
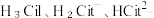 和
和 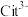 所占的比例 (该微粒浓度与四种微粒浓度之和的比值)如下图所示,则其中代表
所占的比例 (该微粒浓度与四种微粒浓度之和的比值)如下图所示,则其中代表  的曲线是
的曲线是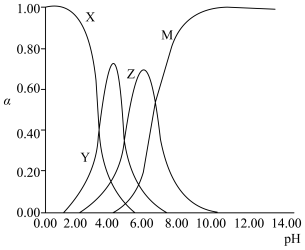
A.Na3Cit溶液中, |
B.Na3Cit溶液中,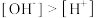 |
C.NaH2Cit溶液中, |
D.Na2HCit溶液中,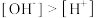 |
(3)已知25℃时,碳酸的电离常数为:
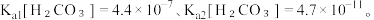 向NaHCO3溶液中加入NaH2Cit溶液,请写出反应的化学方程式
向NaHCO3溶液中加入NaH2Cit溶液,请写出反应的化学方程式
您最近一年使用:0次
名校
3 . 室温下,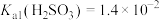 ,通过下列实验探究
,通过下列实验探究 、
、 溶液的性质:
溶液的性质:
实验1:用pH试纸测定0.1mol⋅L
 溶液的pH,测得pH约为10。
溶液的pH,测得pH约为10。
实验2:向0.1mol⋅L
 溶液中通入过量的
溶液中通入过量的 ,再滴入2滴紫色石蕊试剂,溶液呈红色。
,再滴入2滴紫色石蕊试剂,溶液呈红色。
实验3:向实验2溶液中逐滴滴加一定体积的盐酸,测得溶液pH为3。
实验4:向0.1mol⋅L
 溶液中加入等体积、等浓度的
溶液中加入等体积、等浓度的 溶液,产生白色沉淀。
溶液,产生白色沉淀。
下列说法正确的是
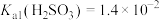 ,通过下列实验探究
,通过下列实验探究 、
、 溶液的性质:
溶液的性质:实验1:用pH试纸测定0.1mol⋅L

 溶液的pH,测得pH约为10。
溶液的pH,测得pH约为10。实验2:向0.1mol⋅L

 溶液中通入过量的
溶液中通入过量的 ,再滴入2滴紫色石蕊试剂,溶液呈红色。
,再滴入2滴紫色石蕊试剂,溶液呈红色。实验3:向实验2溶液中逐滴滴加一定体积的盐酸,测得溶液pH为3。
实验4:向0.1mol⋅L

 溶液中加入等体积、等浓度的
溶液中加入等体积、等浓度的 溶液,产生白色沉淀。
溶液,产生白色沉淀。下列说法正确的是
A.0.1mol⋅L 的 的 溶液中存在: 溶液中存在: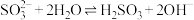 |
B.实验2可以得出: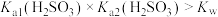 |
C.实验3得到的溶液中存在: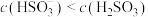 |
D.实验4中可推测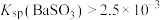 |
您最近一年使用:0次
名校
解题方法
4 . 铬及其化合物在催化、金属防腐等方面具有重要应用。
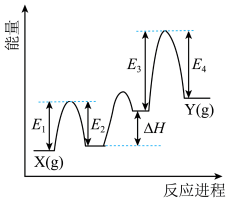
(1)催化剂Cr2O3可由(NH4)2Cr2O7加热分解制备,反应同时生成无污染气体。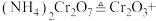
_______ +_______ 。
②Cr2O3催化丙烷脱氢过程中,部分反应历程如图, 过程的焓变为
过程的焓变为___________ (列式表示)。
③Cr2O3可用于NH3的催化氧化。设计从NH3出发经过3步反应制备HNO3的路线__________________ (用“→”表示含氮物质间的转化);其中一个有颜色变化的反应的化学方程式为____________ 。
(2) 溶液中存在多个平衡。本题条件下仅需考虑如下平衡:
溶液中存在多个平衡。本题条件下仅需考虑如下平衡:
(ⅰ)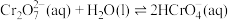
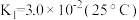
(ⅱ)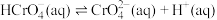

 溶液的说法正确的有
溶液的说法正确的有_______ 。
A.加入少量硫酸,溶液的pH不变
B.加入少量水稀释,溶液中离子总数增加
C.加入少量NaOH溶液,反应(ⅰ)的平衡逆向移动
D.加入少量K2Cr2O7固体,平衡时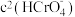 与
与 的比值保持不变
的比值保持不变
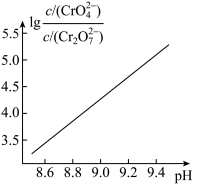
②25℃时,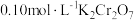 溶液中
溶液中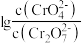 随pH的变化关系如图。当
随pH的变化关系如图。当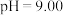 时,设
时,设 、
、 与
与 的平衡浓度分别为x、y、z mol/L,则x、y、z之间的关系式为
的平衡浓度分别为x、y、z mol/L,则x、y、z之间的关系式为____________  ;计算溶液中
;计算溶液中 的平衡浓度
的平衡浓度__________ (写出计算过程,结果保留两位有效数字)。
(1)催化剂Cr2O3可由(NH4)2Cr2O7加热分解制备,反应同时生成无污染气体。
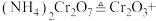
②Cr2O3催化丙烷脱氢过程中,部分反应历程如图,
 过程的焓变为
过程的焓变为③Cr2O3可用于NH3的催化氧化。设计从NH3出发经过3步反应制备HNO3的路线
(2)
 溶液中存在多个平衡。本题条件下仅需考虑如下平衡:
溶液中存在多个平衡。本题条件下仅需考虑如下平衡:(ⅰ)
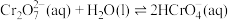
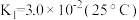
(ⅱ)
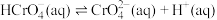

 溶液的说法正确的有
溶液的说法正确的有A.加入少量硫酸,溶液的pH不变
B.加入少量水稀释,溶液中离子总数增加
C.加入少量NaOH溶液,反应(ⅰ)的平衡逆向移动
D.加入少量K2Cr2O7固体,平衡时
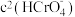 与
与 的比值保持不变
的比值保持不变②25℃时,
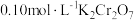 溶液中
溶液中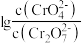 随pH的变化关系如图。当
随pH的变化关系如图。当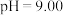 时,设
时,设 、
、 与
与 的平衡浓度分别为x、y、z mol/L,则x、y、z之间的关系式为
的平衡浓度分别为x、y、z mol/L,则x、y、z之间的关系式为 ;计算溶液中
;计算溶液中 的平衡浓度
的平衡浓度
您最近一年使用:0次
5 . 实验是探究物质性质的重要方法,下列操作中,实验现象与得出的结论相一致的是
| 选项 | 实验目的 | 操作及现象 | 结论 |
| A | 比较HClO和CH3COOH的酸性强弱 | 用pH计测定NaClO和CH3COONa的pH值,测得pH(NaClO)>pH(CH3COONa) | 酸性:HClO>CH3COOH |
| B | 验证反应2Fe3++2I- 2Fe2++I2是可逆反应 2Fe2++I2是可逆反应 | 向2mL 0.1mol/L FeCl3溶液加入几滴0.1mol/L KI溶液,充分反应。取反应后试样,滴加淀粉溶液,溶液变为蓝色;另取反应后试样,加入KSCN溶液,溶液变成血红色 | 反应2Fe3++2I- 2Fe2++I2是可逆反应 2Fe2++I2是可逆反应 |
| C | 判断 (AgCl)与 (AgCl)与 (AgI)的大小 (AgI)的大小 | 向等浓度的NaCl、NaI的混合溶液中滴入少量稀AgNO3溶液,有黄色沉淀生成 | Ksp(AgCl)>Ksp(AgI) |
| D | 判断某 溶液样品中是否含有 溶液样品中是否含有 | 向某 溶液样品中加入硫酸酸化的 溶液样品中加入硫酸酸化的 溶液,紫色褪去 溶液,紫色褪去 | 该样品中一定含有 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
6 . 常温下0.2mol•L-1NaHCO3溶液与0.1mol•L-1Na2CO3溶液等体积混合后,下列关于说法不正确 的是
A.NaHCO3=Na++ | B.c(Na+)>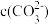 > > >c(OH-) >c(OH-) |
C.c(H+)+c(Na+)=c(OH-)+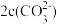 + + | D.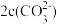 + + + +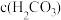 <c(Na+) <c(Na+) |
您最近一年使用:0次
解题方法
7 . 二氧化碳的捕集和利用是寻找双碳解决之策最重要的部分。
(1)室温下在
 的
的 溶液中通入
溶液中通入 ,溶液中含碳物种的浓度
,溶液中含碳物种的浓度
 (不考虑通入
(不考虑通入 所引起的溶液体积变化和
所引起的溶液体积变化和 的挥发)。已知:
的挥发)。已知: 电离常数分别为
电离常数分别为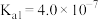 、
、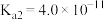 。
。
① 恰好完全转化为
恰好完全转化为 时,溶液中所含离子浓度由小到大的顺序为
时,溶液中所含离子浓度由小到大的顺序为___________ ,
___________ (用含碳微粒和氢离子浓度表示)。
②若吸收
 ,则溶液中
,则溶液中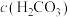
___________  (填“>”“<”或“=”),原因是
(填“>”“<”或“=”),原因是___________ (用必要的计算数据和文字说明)。
③常温下,
 溶液的
溶液的 ,则该溶液中
,则该溶液中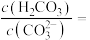
___________ 。
(2) 时,
时, 催化加氢法合成乙烯反应为:
催化加氢法合成乙烯反应为: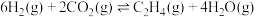
 。向2L的恒容密闭容器中加入
。向2L的恒容密闭容器中加入
 和
和
 ,在催化剂作用下发生反应,测得平衡时体系中各气体的物质的量随温度的变化关系如图所示。
,在催化剂作用下发生反应,测得平衡时体系中各气体的物质的量随温度的变化关系如图所示。___________ (填字母)。
② 下,自初始状态达到平衡时,放热为
下,自初始状态达到平衡时,放热为___________ kJ,该反应的化学平衡常数
___________ , 的平衡转化率为
的平衡转化率为___________ %。
(1)室温下在

 的
的 溶液中通入
溶液中通入 ,溶液中含碳物种的浓度
,溶液中含碳物种的浓度
 (不考虑通入
(不考虑通入 所引起的溶液体积变化和
所引起的溶液体积变化和 的挥发)。已知:
的挥发)。已知: 电离常数分别为
电离常数分别为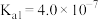 、
、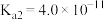 。
。①
 恰好完全转化为
恰好完全转化为 时,溶液中所含离子浓度由小到大的顺序为
时,溶液中所含离子浓度由小到大的顺序为
②若吸收

 ,则溶液中
,则溶液中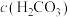
 (填“>”“<”或“=”),原因是
(填“>”“<”或“=”),原因是③常温下,

 溶液的
溶液的 ,则该溶液中
,则该溶液中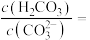
(2)
 时,
时, 催化加氢法合成乙烯反应为:
催化加氢法合成乙烯反应为: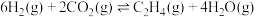
 。向2L的恒容密闭容器中加入
。向2L的恒容密闭容器中加入
 和
和
 ,在催化剂作用下发生反应,测得平衡时体系中各气体的物质的量随温度的变化关系如图所示。
,在催化剂作用下发生反应,测得平衡时体系中各气体的物质的量随温度的变化关系如图所示。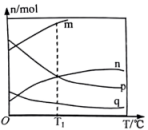
②
 下,自初始状态达到平衡时,放热为
下,自初始状态达到平衡时,放热为
 的平衡转化率为
的平衡转化率为
您最近一年使用:0次
8 . 草酸钠( )常用作还原剂。已知常温下,草酸的电离常数
)常用作还原剂。已知常温下,草酸的电离常数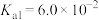 ,
,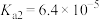 ,碳酸的电离常数
,碳酸的电离常数 ,
, 。回答下列问题:
。回答下列问题:
(1) 发生第一步水解的离子方程式为
发生第一步水解的离子方程式为___________ 。
(2)相同条件下,同浓度的① ,②
,② ,③
,③ ,④
,④ 四种溶液的pH由大到小的顺序为
四种溶液的pH由大到小的顺序为___________ (用编号表示)。
(3)将等浓度、等体积的 溶液与盐酸混合,溶液显酸性。混合后所得溶液中下列关系成立的是
溶液与盐酸混合,溶液显酸性。混合后所得溶液中下列关系成立的是___________ 。
a.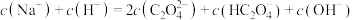
b.
c.
d.
(4) 溶液常用作氧化还原滴定的标准液。实验室欲配制250 mL 0.10 mol·L-1的
溶液常用作氧化还原滴定的标准液。实验室欲配制250 mL 0.10 mol·L-1的 溶液。
溶液。
①需托盘天平称取 固体
固体___________ g。
②配制溶液时,需要的玻璃仪器除烧杯、玻璃棒、量筒外还应有___________ 。
(5)用 标准液测定某高锰酸钾样品的纯度:
标准液测定某高锰酸钾样品的纯度:
步骤I:称取2.0g高锰酸钾样品,配成100mL溶液,取20mL溶液于锥形瓶中,并加入少量硫酸酸化。
步骤II:用(4)中配制的 标准液进行滴定,平行滴定三次,记录消耗
标准液进行滴定,平行滴定三次,记录消耗 溶液的体积如下表:
溶液的体积如下表:
①滴定终点判断的依据是___________ 。
②样品中 的质量分数为
的质量分数为___________ 。
③若(4)中称取的 固体已部分吸水潮解,会使测得的样品中
固体已部分吸水潮解,会使测得的样品中 的质量分数
的质量分数___________ (填“偏高”、“偏低”或“不变”)。
 )常用作还原剂。已知常温下,草酸的电离常数
)常用作还原剂。已知常温下,草酸的电离常数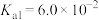 ,
,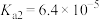 ,碳酸的电离常数
,碳酸的电离常数 ,
, 。回答下列问题:
。回答下列问题:(1)
 发生第一步水解的离子方程式为
发生第一步水解的离子方程式为(2)相同条件下,同浓度的①
 ,②
,② ,③
,③ ,④
,④ 四种溶液的pH由大到小的顺序为
四种溶液的pH由大到小的顺序为(3)将等浓度、等体积的
 溶液与盐酸混合,溶液显酸性。混合后所得溶液中下列关系成立的是
溶液与盐酸混合,溶液显酸性。混合后所得溶液中下列关系成立的是a.
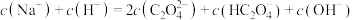
b.

c.

d.

(4)
 溶液常用作氧化还原滴定的标准液。实验室欲配制250 mL 0.10 mol·L-1的
溶液常用作氧化还原滴定的标准液。实验室欲配制250 mL 0.10 mol·L-1的 溶液。
溶液。①需托盘天平称取
 固体
固体②配制溶液时,需要的玻璃仪器除烧杯、玻璃棒、量筒外还应有
(5)用
 标准液测定某高锰酸钾样品的纯度:
标准液测定某高锰酸钾样品的纯度:步骤I:称取2.0g高锰酸钾样品,配成100mL溶液,取20mL溶液于锥形瓶中,并加入少量硫酸酸化。
步骤II:用(4)中配制的
 标准液进行滴定,平行滴定三次,记录消耗
标准液进行滴定,平行滴定三次,记录消耗 溶液的体积如下表:
溶液的体积如下表:| 第1次 | 第2次 | 第3次 | |
消耗 溶液的体积/mL 溶液的体积/mL | 49.80 | 46.75 | 50.20 |
②样品中
 的质量分数为
的质量分数为③若(4)中称取的
 固体已部分吸水潮解,会使测得的样品中
固体已部分吸水潮解,会使测得的样品中 的质量分数
的质量分数
您最近一年使用:0次
9 . 醋酸是常见的一元弱酸。请运用化学反应原理回答下列问题:
(1)室温下,pH=2的醋酸中,水电离出的c(H+)=___________ mol·L-1该醋酸和pH=2的盐酸溶液相比,导电性___________ (填“相同”“不同”或“无法判断”)。
(2)pH相同的盐酸和醋酸分别与足量的锌粒反应,生成等量的H2时所需时间较短的是___________ 。
(3)向 醋酸溶液中滴入
醋酸溶液中滴入 溶液,下列浓度大小顺序不可能出现的是
溶液,下列浓度大小顺序不可能出现的是___________ (填字母)。
a.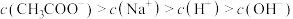
b.
c.
d.
(4)常温下,将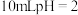 的醋酸溶液稀释至
的醋酸溶液稀释至 ,溶液的
,溶液的
___________ (填“>”“<”或“=”)4;在醋酸稀释过程中下列数值变大的是___________ 。
A. B.
B. C.
C. D.
D.
(5)醋酸中存在平衡: ,下列措施可使醋酸的
,下列措施可使醋酸的 增大,并且电离平衡向右移动的是___________。
增大,并且电离平衡向右移动的是___________。
(1)室温下,pH=2的醋酸中,水电离出的c(H+)=
(2)pH相同的盐酸和醋酸分别与足量的锌粒反应,生成等量的H2时所需时间较短的是
(3)向
 醋酸溶液中滴入
醋酸溶液中滴入 溶液,下列浓度大小顺序不可能出现的是
溶液,下列浓度大小顺序不可能出现的是a.
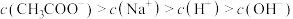
b.

c.

d.

(4)常温下,将
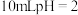 的醋酸溶液稀释至
的醋酸溶液稀释至 ,溶液的
,溶液的
A.
 B.
B. C.
C. D.
D.
(5)醋酸中存在平衡:
 ,下列措施可使醋酸的
,下列措施可使醋酸的 增大,并且电离平衡向右移动的是___________。
增大,并且电离平衡向右移动的是___________。A.加入 溶液 溶液 | B.加入盐酸 | C.加水稀释 | D.对醋酸溶液加热 |
您最近一年使用:0次
名校
10 . 室温下用0.1mol L﹣1Na2SO3溶液吸收SO2的一种脱硫工艺流程如图所示。已知H2SO3电离平衡常数分别为Ka1=1.0×10﹣2,Ka2=1.0×10﹣7,H2CO3电离平衡常数分别为Ka1=4.0×10﹣7、Ka2=5.0×10﹣11,Ksp(CaCO3)=3×10﹣9,Ksp(CaSO3)=3×10﹣7,忽略通入SO2所引起的溶液体积变化和H2O挥发。
L﹣1Na2SO3溶液吸收SO2的一种脱硫工艺流程如图所示。已知H2SO3电离平衡常数分别为Ka1=1.0×10﹣2,Ka2=1.0×10﹣7,H2CO3电离平衡常数分别为Ka1=4.0×10﹣7、Ka2=5.0×10﹣11,Ksp(CaCO3)=3×10﹣9,Ksp(CaSO3)=3×10﹣7,忽略通入SO2所引起的溶液体积变化和H2O挥发。
 L﹣1Na2SO3溶液吸收SO2的一种脱硫工艺流程如图所示。已知H2SO3电离平衡常数分别为Ka1=1.0×10﹣2,Ka2=1.0×10﹣7,H2CO3电离平衡常数分别为Ka1=4.0×10﹣7、Ka2=5.0×10﹣11,Ksp(CaCO3)=3×10﹣9,Ksp(CaSO3)=3×10﹣7,忽略通入SO2所引起的溶液体积变化和H2O挥发。
L﹣1Na2SO3溶液吸收SO2的一种脱硫工艺流程如图所示。已知H2SO3电离平衡常数分别为Ka1=1.0×10﹣2,Ka2=1.0×10﹣7,H2CO3电离平衡常数分别为Ka1=4.0×10﹣7、Ka2=5.0×10﹣11,Ksp(CaCO3)=3×10﹣9,Ksp(CaSO3)=3×10﹣7,忽略通入SO2所引起的溶液体积变化和H2O挥发。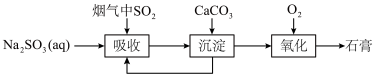
A.0.1mol L﹣1 Na2SO3溶液中:c(OH﹣)=c(H+)+c( L﹣1 Na2SO3溶液中:c(OH﹣)=c(H+)+c( )+c(H2SO3) )+c(H2SO3) |
B.NaHSO3溶液中:c( )<c(H2SO3) )<c(H2SO3) |
C.“沉淀”分离后的滤液中:c(Ca2+) c( c( )<Ksp(CaSO3) )<Ksp(CaSO3) |
D.“沉淀”时发生主要反应的离子方程式:CaCO3+ =CaSO3+ =CaSO3+ |
您最近一年使用:0次



