1 . 常温下,在 (弱酸)溶液中滴加
(弱酸)溶液中滴加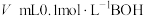 (弱碱)溶液生成强电解质
(弱碱)溶液生成强电解质 ,混合溶液中
,混合溶液中 与
与 的关系如图所示。下列叙述正确的是
的关系如图所示。下列叙述正确的是
 (弱酸)溶液中滴加
(弱酸)溶液中滴加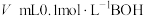 (弱碱)溶液生成强电解质
(弱碱)溶液生成强电解质 ,混合溶液中
,混合溶液中 与
与 的关系如图所示。下列叙述正确的是
的关系如图所示。下列叙述正确的是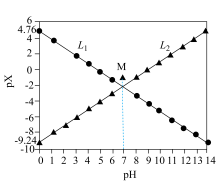
A. 代表 代表 与 与 的关系 的关系 |
B. 时达到 时达到 点, 点, 不水解 不水解 |
C.常温下, |
D.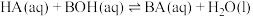 的平衡常数 的平衡常数 小于10000 小于10000 |
您最近一年使用:0次
2 . 某化学小组同学对FeCl3溶液与Na2SO3溶液的反应进行探究
(1)请用离子方程式表示Na2SO3溶液显碱性的原因___________ 。
(2)甲同学认为实验①发生了氧化还原,其反应的离子方程式为___________ ,取反应后的溶液中加入K3[Fe(CN)6]溶液,观察到___________ (填现象),证实了此结论。
(3)乙同学检验红褐色沉淀为Fe(OH)3,请用平衡移动原理解释生成沉淀的原因___________ 。
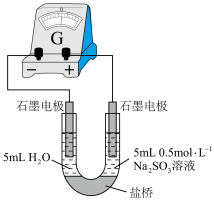
(4)丙组同学检验实验②中无Fe2+,为探究此浓度下是否能发生氧化还原反应,做了如下实验:向U形管的左侧加入___________ ,观察到___________ (填实验现象),证实此浓度下的FeCl3溶液与Na2SO3溶液可以发生氧化还原反应。 可形成难电离的红色配合物:
可形成难电离的红色配合物: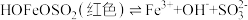 。请解释实验②中无Fe2+生成的原因
。请解释实验②中无Fe2+生成的原因___________ 。
(6)通过以上探究,FeCl3溶液与Na2SO3溶液的反应受___________ 因素影响(至少写出两项)。
| 实验操作 | 现象 | |
| ① |
| 溶液由棕黄色变为红色,无沉淀生成。 放置6小时后,溶液变为淡黄色,始终无沉淀生成。 |
② |
| 溶液由棕黄色变为红色,无沉淀生成。 放置6小时后,生成红褐色沉淀,上层清液为无色。 |
(1)请用离子方程式表示Na2SO3溶液显碱性的原因
(2)甲同学认为实验①发生了氧化还原,其反应的离子方程式为
(3)乙同学检验红褐色沉淀为Fe(OH)3,请用平衡移动原理解释生成沉淀的原因
(4)丙组同学检验实验②中无Fe2+,为探究此浓度下是否能发生氧化还原反应,做了如下实验:向U形管的左侧加入
 可形成难电离的红色配合物:
可形成难电离的红色配合物: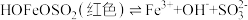 。请解释实验②中无Fe2+生成的原因
。请解释实验②中无Fe2+生成的原因(6)通过以上探究,FeCl3溶液与Na2SO3溶液的反应受
您最近一年使用:0次
名校
解题方法
3 . 常温下,用浓度为 的
的 标准溶液滴定浓度均为
标准溶液滴定浓度均为 的
的 和
和 的混合溶液,滴定过程中溶液的pH随
的混合溶液,滴定过程中溶液的pH随 (
(
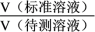 )的变化曲线如图所示。下列说法正确的是
)的变化曲线如图所示。下列说法正确的是

A.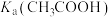 的数量级为 的数量级为 |
B.点a: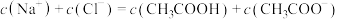 |
C.点b: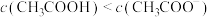 |
| D.水的电离程度:a<b<c<d |
您最近一年使用:0次
2024-01-20更新
|
113次组卷
|
2卷引用:广西钦州市第四中学2023-2024学年高二上学期1月考试化学试卷
名校
4 . 现用物质的量浓度为 的标准
的标准 溶液去测定
溶液去测定 溶液的物质的量浓度(已知:常温时,
溶液的物质的量浓度(已知:常温时,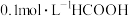 溶液的
溶液的 大于1)。试回答下列问题:
大于1)。试回答下列问题:
(1)量取 待测液应使用
待测液应使用___________ (填仪器名称)。下列溶液可用该滴定管盛装的是___________ 。
A. B.
B. C.
C.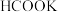 D.
D.
(2)该实验可使用___________ 作指示剂;判断滴定终点的依据是___________ 。
(3)下列操作使实验结果偏低的是___________ (填字母)。
A.滴定前读数正确,达滴定终点时仰视滴定管内液面读数
B.盛装 溶液的滴定管用蒸馏水洗净后立即量取
溶液的滴定管用蒸馏水洗净后立即量取 溶液
溶液
C.锥形瓶先水洗,然后用 溶液润洗
溶液润洗
D.达到滴定终点时,盛装 溶液的滴定管尖嘴有悬液
溶液的滴定管尖嘴有悬液
E.振荡锥形瓶时部分液体溅出
(4)滴定结果如下表所示:
则 溶液的物质的量浓度是
溶液的物质的量浓度是___________ 。
(5)室温下,用 溶液分别滴定
溶液分别滴定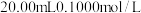 的
的 和
和 ,滴定曲线如图所示。
,滴定曲线如图所示。

①表示滴定盐酸的曲线是___________ (填Ⅰ或Ⅱ)。
② 时,滴定
时,滴定 消耗的
消耗的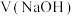
___________  (填“等于”,“大于”或“小于”);
(填“等于”,“大于”或“小于”);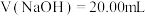 时,两份溶液中
时,两份溶液中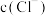
___________ 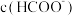 (填“等于”、“大于”或“小于”)。
(填“等于”、“大于”或“小于”)。
③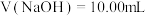 时,
时, 溶液中离子浓度从大到小的顺序是
溶液中离子浓度从大到小的顺序是___________ 。
 的标准
的标准 溶液去测定
溶液去测定 溶液的物质的量浓度(已知:常温时,
溶液的物质的量浓度(已知:常温时,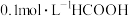 溶液的
溶液的 大于1)。试回答下列问题:
大于1)。试回答下列问题:(1)量取
 待测液应使用
待测液应使用A.
 B.
B. C.
C.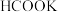 D.
D.
(2)该实验可使用
(3)下列操作使实验结果偏低的是
A.滴定前读数正确,达滴定终点时仰视滴定管内液面读数
B.盛装
 溶液的滴定管用蒸馏水洗净后立即量取
溶液的滴定管用蒸馏水洗净后立即量取 溶液
溶液C.锥形瓶先水洗,然后用
 溶液润洗
溶液润洗D.达到滴定终点时,盛装
 溶液的滴定管尖嘴有悬液
溶液的滴定管尖嘴有悬液E.振荡锥形瓶时部分液体溅出
(4)滴定结果如下表所示:
| 滴定次数 |  溶液的体积 溶液的体积 |  溶液的体积 溶液的体积 | |
滴定前刻度 | 滴定后刻度 | ||
| 1 | 20.00 | 4.01 | 24.05 |
| 2 | 20.00 | 0.15 | 22.76 |
| 3 | 20.00 | 1.96 | 21.99 |
| 4 | 20.00 | 3.54 | 23.59 |
 溶液的物质的量浓度是
溶液的物质的量浓度是(5)室温下,用
 溶液分别滴定
溶液分别滴定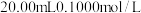 的
的 和
和 ,滴定曲线如图所示。
,滴定曲线如图所示。
①表示滴定盐酸的曲线是
②
 时,滴定
时,滴定 消耗的
消耗的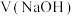
 (填“等于”,“大于”或“小于”);
(填“等于”,“大于”或“小于”);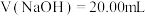 时,两份溶液中
时,两份溶液中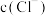
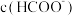 (填“等于”、“大于”或“小于”)。
(填“等于”、“大于”或“小于”)。③
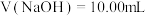 时,
时, 溶液中离子浓度从大到小的顺序是
溶液中离子浓度从大到小的顺序是
您最近一年使用:0次
名校
解题方法
5 . 25℃时,下列有关电解质溶液的说法错误的是
A.向 溶液中加入少量 溶液中加入少量 固体,溶液中 固体,溶液中 的值增大 的值增大 |
B.加水稀释 溶液,溶液中 溶液,溶液中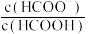 逐渐减小 逐渐减小 |
C. 的 的 溶液与 溶液与 的盐酸中, 的盐酸中, 溶液中水电离的 溶液中水电离的 大 大 |
D. 的 的 与 与 混合溶液中, 混合溶液中,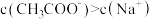 |
您最近一年使用:0次
名校
6 . 室温下向10mL0.1mol·L-1NaOH溶液中加入0.1mol·L-1的一元酸HA,测得溶液pH的变化曲线如图所示。下列说法正确的是

| A.a点所示溶液中c(Na+)>c(A−)>c(HA)>c(OH−) |
| B.pH=7时,c(Na+)=c(A−)+c(HA) |
| C.b点所示溶液中c(A−)>c(Na+) |
| D.a点所示溶液中水电离的c(H+)=10-8.7mol/L |
您最近一年使用:0次
2023-12-11更新
|
147次组卷
|
2卷引用:广西梧州高级中学2023-2024学年高二上学期期中考试化学试题
名校
解题方法
7 . 常温下,一元酸HA的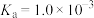 ,往Ⅰ和Ⅱ两室中分别加入HA溶液和MA溶液,中间用交换膜隔开(只有未电离的HA分子可自由通过交换膜,且不考虑溶液体积的变化),设
,往Ⅰ和Ⅱ两室中分别加入HA溶液和MA溶液,中间用交换膜隔开(只有未电离的HA分子可自由通过交换膜,且不考虑溶液体积的变化),设 ,达到平衡后,如下图所示,下列说法错误的是
,达到平衡后,如下图所示,下列说法错误的是

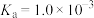 ,往Ⅰ和Ⅱ两室中分别加入HA溶液和MA溶液,中间用交换膜隔开(只有未电离的HA分子可自由通过交换膜,且不考虑溶液体积的变化),设
,往Ⅰ和Ⅱ两室中分别加入HA溶液和MA溶液,中间用交换膜隔开(只有未电离的HA分子可自由通过交换膜,且不考虑溶液体积的变化),设 ,达到平衡后,如下图所示,下列说法错误的是
,达到平衡后,如下图所示,下列说法错误的是
A.Ⅰ室中 | B.Ⅱ室中 |
C.Ⅰ室中 | D.MOH可能为弱碱 |
您最近一年使用:0次
名校
8 . 难溶盐CaF2可溶于盐酸,常温下,用HCl调节CaF2浊液的pH,测得体系中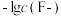 或
或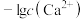 与
与 的关系如图所示。下列说法错误的是
的关系如图所示。下列说法错误的是

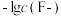 或
或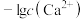 与
与 的关系如图所示。下列说法错误的是
的关系如图所示。下列说法错误的是
A.I代表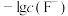 与 与 的变化曲线 的变化曲线 | B.常温下,HF的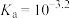 |
| C.Z点的坐标为(0,3.2) | D.Y点的溶液中存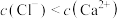 |
您最近一年使用:0次
名校
解题方法
9 . 已知H3PO4是一种三元中强酸。25℃时,向某浓度H3PO4溶液中逐滴加入NaOH溶液,滴加过程中各种含磷微粒的物质的量分数δ随溶液pH的变化曲线如图所示。下列说法正确的是
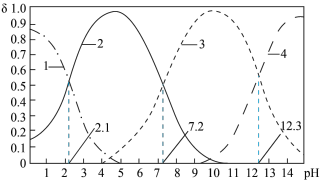

A.曲线2表示HPO ,曲线4表示PO ,曲线4表示PO |
B.25℃时,H3PO4的电离常数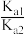 =10-5.1 =10-5.1 |
| C.pH=7.2时,溶液中由水电离出的c(H+)=10-6.8mol•L-1 |
D.pH=12.3时,溶液中5c(Na+)=2c(H3PO4)+2c(H2PO )+2c(HPO )+2c(HPO )+2c(PO )+2c(PO ) ) |
您最近一年使用:0次
2023-10-15更新
|
1259次组卷
|
5卷引用:广西玉林市2023-2024学年高二上学期11月期中考试化学试题
10 . 电解质在水溶液中存在各种行为,如电离、水解、沉淀溶解等,据所学知识回答下列问题:
(1)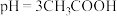 溶液中水电离出来的
溶液中水电离出来的 和溶液中的
和溶液中的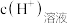 之比是
之比是___________ 。
(2)25℃时,将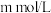 的醋酸和
的醋酸和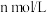 的氢氧化钠溶液等体积混合后,溶液的
的氢氧化钠溶液等体积混合后,溶液的 ,则溶液中
,则溶液中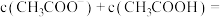
___________ ,m与n的大小关系是m___________ n(填“>”“=”或“<”)。
(3)将 分别放入:①
分别放入:① 水②
水② 溶液③
溶液③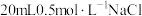 溶液④
溶液④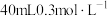 盐酸,各溶液中
盐酸,各溶液中 的浓度由大到小的排列顺序是
的浓度由大到小的排列顺序是___________ (用字母表示)。
(4)氯化铁溶液蒸干并灼烧的产物是___________ ,原因是___________ 。
(5)25℃时,醋酸的电离常数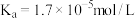 ,则该温度下
,则该温度下 的水解平衡常数
的水解平衡常数
___________  (保留到小数点后一位)。
(保留到小数点后一位)。
(1)
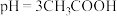 溶液中水电离出来的
溶液中水电离出来的 和溶液中的
和溶液中的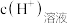 之比是
之比是(2)25℃时,将
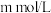 的醋酸和
的醋酸和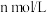 的氢氧化钠溶液等体积混合后,溶液的
的氢氧化钠溶液等体积混合后,溶液的 ,则溶液中
,则溶液中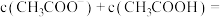
(3)将
 分别放入:①
分别放入:① 水②
水② 溶液③
溶液③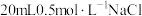 溶液④
溶液④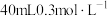 盐酸,各溶液中
盐酸,各溶液中 的浓度由大到小的排列顺序是
的浓度由大到小的排列顺序是(4)氯化铁溶液蒸干并灼烧的产物是
(5)25℃时,醋酸的电离常数
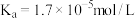 ,则该温度下
,则该温度下 的水解平衡常数
的水解平衡常数
 (保留到小数点后一位)。
(保留到小数点后一位)。
您最近一年使用:0次





