1 . 常温下,已知三种一元弱酸的相对强弱: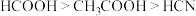 。在浓度均为
。在浓度均为 的
的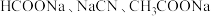 的混合溶液中,通入
的混合溶液中,通入 气体,随着
气体,随着 增大,溶液中的
增大,溶液中的 与
与 (
( 代表三种酸根离子,
代表三种酸根离子, 表示三种弱酸)的分布系数
表示三种弱酸)的分布系数 (平衡时某物种的浓度占各物种浓度之和的分数)变化如图所示。下列说法错误的是
(平衡时某物种的浓度占各物种浓度之和的分数)变化如图所示。下列说法错误的是
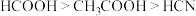 。在浓度均为
。在浓度均为 的
的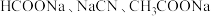 的混合溶液中,通入
的混合溶液中,通入 气体,随着
气体,随着 增大,溶液中的
增大,溶液中的 与
与 (
( 代表三种酸根离子,
代表三种酸根离子, 表示三种弱酸)的分布系数
表示三种弱酸)的分布系数 (平衡时某物种的浓度占各物种浓度之和的分数)变化如图所示。下列说法错误的是
(平衡时某物种的浓度占各物种浓度之和的分数)变化如图所示。下列说法错误的是
A. 的电离常数 的电离常数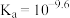 |
B.反应 的平衡常数 的平衡常数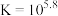 |
C.交点 处的 处的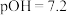 |
D.原混合溶液中: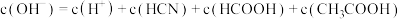 |
您最近一年使用:0次
解题方法
2 . 已知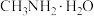 为一元弱碱。常温下,将
为一元弱碱。常温下,将 气体通入
气体通入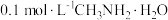 水溶液中,混合溶液的
水溶液中,混合溶液的 与
与 和
和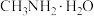 四种微粒浓度对数值(
四种微粒浓度对数值( )的关系如图所示(忽略溶液体积的变化)。下列说法错误的是
)的关系如图所示(忽略溶液体积的变化)。下列说法错误的是
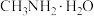 为一元弱碱。常温下,将
为一元弱碱。常温下,将 气体通入
气体通入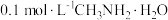 水溶液中,混合溶液的
水溶液中,混合溶液的 与
与 和
和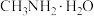 四种微粒浓度对数值(
四种微粒浓度对数值( )的关系如图所示(忽略溶液体积的变化)。下列说法错误的是
)的关系如图所示(忽略溶液体积的变化)。下列说法错误的是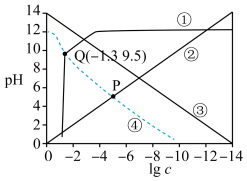
A.①线表示 浓度对数值与溶液 浓度对数值与溶液 的关系 的关系 |
B.常温下, |
C.该体系中, |
D.P点之后,溶液中不可能存在 |
您最近一年使用:0次
2024-04-29更新
|
48次组卷
|
2卷引用:湖北省黄冈市2023-2024学年高二上学期期末调研考试化学试题
解题方法
3 . 由实验操作和现象,可得出相应结论的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 分别测浓度均为 的 的 和 和 溶液的 溶液的 | 后者大于前者 |  |
| B | 向 溶液中先滴加2滴 溶液中先滴加2滴 溶液,再滴加4滴 溶液,再滴加4滴 溶液 溶液 | 先产生白色沉淀再产生黄色沉淀 | 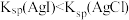 |
| C | 用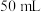 注射器吸入 注射器吸入 和 和 的混合气体,将细管端用橡皮塞封闭。然后将活塞往外拉伸一段距离 的混合气体,将细管端用橡皮塞封闭。然后将活塞往外拉伸一段距离 | 注射器内混合气体的颜色先变浅又逐渐变深 | 其他条件不变,减压,平衡向生成 气体的方向移动 气体的方向移动 |
| D | 加热试管中的聚氯乙烯薄膜碎片 | 试管口润湿的蓝色石蕊试纸变红 | 氯乙烯加聚反应是可逆反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-04-29更新
|
52次组卷
|
2卷引用:湖北省黄冈市2023-2024学年高二上学期期末调研考试化学试题
4 . 溶液中的离子平衡在生产生活中有着广泛的应用,回答下列问题。
I.下表为几种弱酸在常温下的电离平衡常数
(1)CO 水解常数的表达式Kh=
水解常数的表达式Kh=___________
(2)常温下,浓度均为0.1mol/L的下列5种溶液:
①NaHCO3溶液;②NaCN溶液;③NaClO溶液;④CH3COONa溶液;⑤Na2CO3溶液。
它们pH由大到小的顺序是___________ (填序号)。
II.FeCl3溶液通过控制条件,在加热下可获得铁黄(FeOOH)沉淀。
(3)①写出制备铁黄的离子方程式:___________ 。
②制备过程中可以边加热边加水,其目的是___________ 。
(4)向FeCl3溶液中加入NH4HCO3溶液可获得铁黄,该反应的化学方程式为___________ 。
III.某样品为KClO4和KCl混合物,为测定产品含量进行如下实验:准确称取100.1g样品溶于水中,配成250mL溶液。从中取出25.00mL于锥形瓶中,加入适量葡萄糖,加热使ClO4-全部转化为Cl-(反应为 。加入少量
。加入少量 溶液作指示剂,用2.000 mol/L
溶液作指示剂,用2.000 mol/L 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液体积50.00mL。滴定达到终点时,产生砖红色
溶液体积50.00mL。滴定达到终点时,产生砖红色  4沉淀。
4沉淀。
(5)已知 ,若终点时
,若终点时 10-4
10-4  ,则此时c(Cl-)=
,则此时c(Cl-)=___________ mol/L。
(6)样品中KClO4与KCl的物质的量之比为___________ 。
I.下表为几种弱酸在常温下的电离平衡常数
| 物质 | CH3COOH | HCN | HClO | H2CO3 |
| Ka | 1.7×10-5 | 4.9×10-10 | 3×10-8 | Ka1=4.3×10-7 Ka2=5.6×10-11 |
 水解常数的表达式Kh=
水解常数的表达式Kh=(2)常温下,浓度均为0.1mol/L的下列5种溶液:
①NaHCO3溶液;②NaCN溶液;③NaClO溶液;④CH3COONa溶液;⑤Na2CO3溶液。
它们pH由大到小的顺序是
II.FeCl3溶液通过控制条件,在加热下可获得铁黄(FeOOH)沉淀。
(3)①写出制备铁黄的离子方程式:
②制备过程中可以边加热边加水,其目的是
(4)向FeCl3溶液中加入NH4HCO3溶液可获得铁黄,该反应的化学方程式为
III.某样品为KClO4和KCl混合物,为测定产品含量进行如下实验:准确称取100.1g样品溶于水中,配成250mL溶液。从中取出25.00mL于锥形瓶中,加入适量葡萄糖,加热使ClO4-全部转化为Cl-(反应为
 。加入少量
。加入少量 溶液作指示剂,用2.000 mol/L
溶液作指示剂,用2.000 mol/L 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液体积50.00mL。滴定达到终点时,产生砖红色
溶液体积50.00mL。滴定达到终点时,产生砖红色  4沉淀。
4沉淀。(5)已知
 ,若终点时
,若终点时 10-4
10-4  ,则此时c(Cl-)=
,则此时c(Cl-)=(6)样品中KClO4与KCl的物质的量之比为
您最近一年使用:0次
名校
5 . 下列实验不能达到实验目的的是
| A | B | C | D |
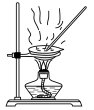 | 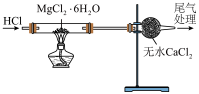 | 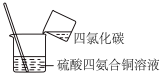 |  |
| 加热融化硫固体 | 制备无水氯化镁 | 制备硫酸四氨合铜晶体 | 制备明矾晶体 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
6 . NA为啊伏伽德罗常数,下列说法正确的是
A.1L1mol/LNa2CO3溶液中, 的数目为NA 的数目为NA |
| B.16gO2和O3的混合物中,含氧原子数目为NA |
| C.1molFe与足量硫粉反应,转移电子数目为3NA |
| D.46g乙醇含共价键的数目为7NA |
您最近一年使用:0次
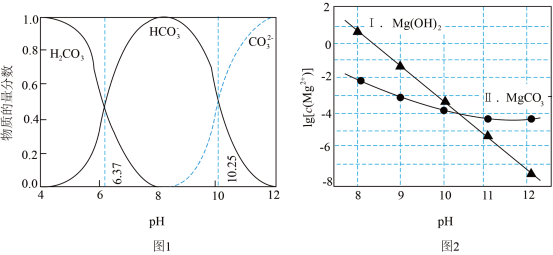
7 . 常温下, 在Na2CO3溶液中发生反应,可能生成
在Na2CO3溶液中发生反应,可能生成 或MgCO3。图1表示Na2CO3溶液中各含碳物种的物质的量分数与溶液pH的关系;图2中曲线Ⅰ的离子浓度关系符合
或MgCO3。图1表示Na2CO3溶液中各含碳物种的物质的量分数与溶液pH的关系;图2中曲线Ⅰ的离子浓度关系符合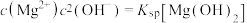 ;曲线Ⅱ的离子浓度关系符合
;曲线Ⅱ的离子浓度关系符合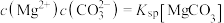 。利用平衡原理分析,下列说法正确的是
。利用平衡原理分析,下列说法正确的是
 在Na2CO3溶液中发生反应,可能生成
在Na2CO3溶液中发生反应,可能生成 或MgCO3。图1表示Na2CO3溶液中各含碳物种的物质的量分数与溶液pH的关系;图2中曲线Ⅰ的离子浓度关系符合
或MgCO3。图1表示Na2CO3溶液中各含碳物种的物质的量分数与溶液pH的关系;图2中曲线Ⅰ的离子浓度关系符合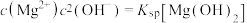 ;曲线Ⅱ的离子浓度关系符合
;曲线Ⅱ的离子浓度关系符合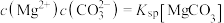 。利用平衡原理分析,下列说法正确的是
。利用平衡原理分析,下列说法正确的是
A.常温时, 的水解常数 的水解常数 |
B.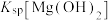 的数量级为 的数量级为 |
C.由图2,当pH=11, 时,有沉淀生成 时,有沉淀生成 |
D.由图1和图2,在pH=8,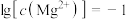 时,溶液中发生反应: 时,溶液中发生反应: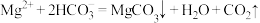 |
您最近一年使用:0次
名校
解题方法
8 . 将磷肥生产形成的副产物石膏( )转化为硫酸钾肥料和氯化钙水合物储热材料,无论从经济效益、资源综合利用还是从环境保护角度看都具有重要意义。石膏转化为硫酸钾和氯化钙的工艺流程示意图如图所示
)转化为硫酸钾肥料和氯化钙水合物储热材料,无论从经济效益、资源综合利用还是从环境保护角度看都具有重要意义。石膏转化为硫酸钾和氯化钙的工艺流程示意图如图所示
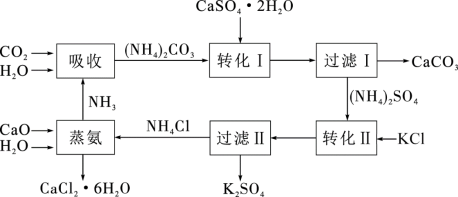
请回答下列问题:
(1)本工艺中所用的原料除 、CaCO3、H2O外,还需要的两种原料是
、CaCO3、H2O外,还需要的两种原料是______ 、______ (填化学式,不考虑损耗)。
(2)室温下, 溶液的pH
溶液的pH______ 7(填“>”、“<”或“=”),该溶液中所有微粒(水分子除外)的物质的量浓度由小到大的顺序为______ 。
(3)转化Ⅰ是将难溶的CaSO4(s)转化为更难溶的CaCO3(s),将一定量的 加入过量的CaSO4悬浊液中,充分反应后,测得溶液中
加入过量的CaSO4悬浊液中,充分反应后,测得溶液中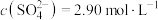 ,此时溶液中的
,此时溶液中的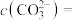
______  。[已知:
。[已知: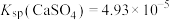 、
、 ]
]
(4)已知不同温度下K2SO4在100 g水中达到饱和时溶解的量如下表:
75℃的K2SO4饱和溶液482 g冷却到20℃,可析出K2SO4晶体______ g。
(5)写出“蒸氨”过程中的化学方程式:____________________ 。
 )转化为硫酸钾肥料和氯化钙水合物储热材料,无论从经济效益、资源综合利用还是从环境保护角度看都具有重要意义。石膏转化为硫酸钾和氯化钙的工艺流程示意图如图所示
)转化为硫酸钾肥料和氯化钙水合物储热材料,无论从经济效益、资源综合利用还是从环境保护角度看都具有重要意义。石膏转化为硫酸钾和氯化钙的工艺流程示意图如图所示
请回答下列问题:
(1)本工艺中所用的原料除
 、CaCO3、H2O外,还需要的两种原料是
、CaCO3、H2O外,还需要的两种原料是(2)室温下,
 溶液的pH
溶液的pH(3)转化Ⅰ是将难溶的CaSO4(s)转化为更难溶的CaCO3(s),将一定量的
 加入过量的CaSO4悬浊液中,充分反应后,测得溶液中
加入过量的CaSO4悬浊液中,充分反应后,测得溶液中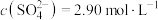 ,此时溶液中的
,此时溶液中的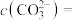
 。[已知:
。[已知: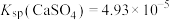 、
、 ]
](4)已知不同温度下K2SO4在100 g水中达到饱和时溶解的量如下表:
温度/℃ | 0 | 20 | 40 | 60 | 75 |
K2SO4溶解的量/g | 7.7 | 11.1 | 14.7 | 18.1 | 20.5 |
(5)写出“蒸氨”过程中的化学方程式:
您最近一年使用:0次
9 . 常温下,0.10 mol/L HCOONH4溶液中部分微粒( 、
、 、HCOOH、
、HCOOH、 )的
)的 (可通入加入NaOH或HCl调节溶液pH)关系如图所示。
(可通入加入NaOH或HCl调节溶液pH)关系如图所示。 ,
,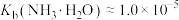 。下列说法正确的是
。下列说法正确的是


 、
、 、HCOOH、
、HCOOH、 )的
)的 (可通入加入NaOH或HCl调节溶液pH)关系如图所示。
(可通入加入NaOH或HCl调节溶液pH)关系如图所示。 ,
,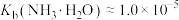 。下列说法正确的是
。下列说法正确的是

A.曲线②和③分别表示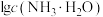 和 和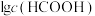 随pH的变化 随pH的变化 |
| B.溶液中M点对应的pH=7 |
C.HCOONH4的水解平衡常数 约为 约为 |
D.原溶液中 |
您最近一年使用:0次
2024-02-25更新
|
146次组卷
|
2卷引用:湖北省鄂西南三校2023-2024学年高二下学期3月联考化学试题
解题方法
10 . 某温度下,向 溶液中滴入
溶液中滴入 的
的 溶液,溶液中
溶液,溶液中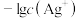 随加入
随加入 溶液体积[
溶液体积[ ]的关系如图所示。下列说法正确的是
]的关系如图所示。下列说法正确的是

已知:该温度下,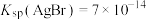 。
。
 溶液中滴入
溶液中滴入 的
的 溶液,溶液中
溶液,溶液中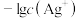 随加入
随加入 溶液体积[
溶液体积[ ]的关系如图所示。下列说法正确的是
]的关系如图所示。下列说法正确的是
已知:该温度下,
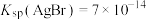 。
。A.该温度下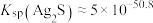 |
B.向b点溶液中加入 的KBr溶液,沉淀转化为AgBr 的KBr溶液,沉淀转化为AgBr |
C.c点溶液中存在: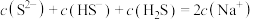 |
D.相同条件下, 在水中和在 在水中和在 溶液中的溶解度相同 溶液中的溶解度相同 |
您最近一年使用:0次



