名校
解题方法
1 . 鼓励日常生活中勤用肥皂水洗手。已知肥㿝的主要成分是硬脂酸且硬脂酸是弱酸。下列叙述错误的是
| A.肥皂水呈中性 | B.肥皂水中 |
| C.肥皂水中存在水解平衡和水的电离平衡 | D.在肥皂水中滴加盐酸会生成硬脂酸 |
您最近一年使用:0次
2 . 碳酸锂可以用作电池的正极材料。在锂离子电池中,正极材料是决定电池性能的关键因素之一,而碳酸锂能够有效提高电池的能量密度和稳定性,从而延长电池的使用寿命。这使得碳酸锂成为制造高性能电动汽车电池和储能系统的重要材料。以电解铝废渣(主要含AlF3、NaF、LiF、CaO)为原料,制备电池级碳酸锂的工艺流程如下: 、
、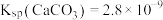 。回答下列问题:
。回答下列问题:
(1)①电解氧化铝生成铝的化学方程式为__________ ,无碳电解铝技术是利用陶瓷材料替代碳作阳极,该技术的优点之一是__________ 。
②已知AlCl3可形成共价分子,AlF3为离子晶体,从电负性的角度解释其原因:__________ 。
(2)“气体1”是______ (填化学式,下同),“滤渣1”的主要成分是______ 。
(3)已知“碱解”同时生成白色沉淀,写出生成“气体2”的离子方程式__________________ 。
(4)Al-Li合金具有低密度、耐腐蚀等特点,已成为航天器的重要结构材料。一种Al3Li合金的晶胞如图所示,其中白球代表的是______ ;若其晶胞参数为apm,则该合金的晶体密度为______ g∙cm-3(列出计算式,阿伏加德罗常数用NA表示)。
 、
、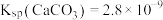 。回答下列问题:
。回答下列问题:(1)①电解氧化铝生成铝的化学方程式为
②已知AlCl3可形成共价分子,AlF3为离子晶体,从电负性的角度解释其原因:
(2)“气体1”是
(3)已知“碱解”同时生成白色沉淀,写出生成“气体2”的离子方程式
(4)Al-Li合金具有低密度、耐腐蚀等特点,已成为航天器的重要结构材料。一种Al3Li合金的晶胞如图所示,其中白球代表的是

您最近一年使用:0次
名校
解题方法
3 . 设 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A.含有7.8 g 的溶液中: 的溶液中: 的数目为 的数目为 |
B.1 L 1 mol⋅L 溴化铵水溶液中 溴化铵水溶液中 与 与 离子数之和大于 离子数之和大于 |
C.标准状况下,11.2 L  含有 含有 键的数目为 键的数目为 |
D.常温下,1 L  的 的 溶液中,由水电离出的 溶液中,由水电离出的 数目为 数目为 |
您最近一年使用:0次
2024-05-02更新
|
78次组卷
|
2卷引用:广西防城港市实验高级中学2023-2024学年高二下学期期中考试化学试题
解题方法
4 . 从海水中可提取多种化工原料,下图是工业上对海水的几项综合利用的示意图。试回答下列问题: 的化学方程式:
的化学方程式:___________ ,___________ ;
(2)以上海水的综合利用过程中,哪一种操作肯定会引起氧化还原反应的发生?___________ ;
(3)电解无水 可制取镁和氯气,其中副产品氯气和烧碱溶液可制得“84”消毒液,制“84”消毒液的离子方程式为
可制取镁和氯气,其中副产品氯气和烧碱溶液可制得“84”消毒液,制“84”消毒液的离子方程式为___________ ;
(4)海边盐碱地(含较多 、
、 )不利于植物生长,盐碱地产生碱性的原因:
)不利于植物生长,盐碱地产生碱性的原因:___________ (用离子方程式表示);农业上用石膏降低其碱性的反应原理:___________ (用化学方程式表示);
(5)用海滩上的贝壳制 ,而不从异地山中开凿石灰石制取,主要考虑到
,而不从异地山中开凿石灰石制取,主要考虑到___________ 问题。

 的化学方程式:
的化学方程式:(2)以上海水的综合利用过程中,哪一种操作肯定会引起氧化还原反应的发生?
(3)电解无水
 可制取镁和氯气,其中副产品氯气和烧碱溶液可制得“84”消毒液,制“84”消毒液的离子方程式为
可制取镁和氯气,其中副产品氯气和烧碱溶液可制得“84”消毒液,制“84”消毒液的离子方程式为(4)海边盐碱地(含较多
 、
、 )不利于植物生长,盐碱地产生碱性的原因:
)不利于植物生长,盐碱地产生碱性的原因:(5)用海滩上的贝壳制
 ,而不从异地山中开凿石灰石制取,主要考虑到
,而不从异地山中开凿石灰石制取,主要考虑到
您最近一年使用:0次
5 . 下列事实不能证明亚硝酸( )是弱电解质的是
)是弱电解质的是
 )是弱电解质的是
)是弱电解质的是A.常温下 溶液的 溶液的 |
B.常温下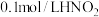 溶液的 溶液的 约为2 约为2 |
| C.亚硝酸溶液中滴加紫色石蕊试液,溶液变红色 |
D.常温下将 的 的 溶液加水稀释至100倍,稀释后溶液的 溶液加水稀释至100倍,稀释后溶液的 约为4.5 约为4.5 |
您最近一年使用:0次
解题方法
6 . 已知:常温下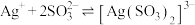 ,
,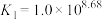 ,
,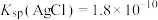 ,某实验小组利用AgCl与Na2SO3反应生成
,某实验小组利用AgCl与Na2SO3反应生成 来“分银”,“分银”时,
来“分银”,“分银”时, 的浓度与溶液pH的关系如图1;
的浓度与溶液pH的关系如图1; 与H+形成的微粒的浓度分数
与H+形成的微粒的浓度分数 随溶液pH变化的关系如图2,下列叙述错误的是
随溶液pH变化的关系如图2,下列叙述错误的是
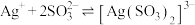 ,
,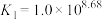 ,
,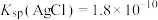 ,某实验小组利用AgCl与Na2SO3反应生成
,某实验小组利用AgCl与Na2SO3反应生成 来“分银”,“分银”时,
来“分银”,“分银”时, 的浓度与溶液pH的关系如图1;
的浓度与溶液pH的关系如图1; 与H+形成的微粒的浓度分数
与H+形成的微粒的浓度分数 随溶液pH变化的关系如图2,下列叙述错误的是
随溶液pH变化的关系如图2,下列叙述错误的是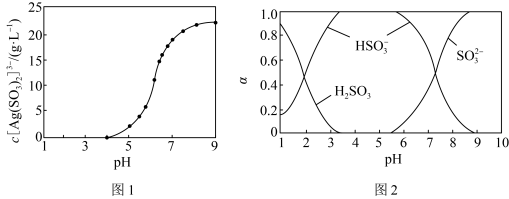
A. 中的∠O—S—O小于 中的∠O—S—O小于 中的∠O—S—O 中的∠O—S—O |
| B.“分银”时,pH需控制的范围大约是8~9 |
C. 溶液中存在 溶液中存在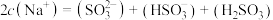 |
D.AgCl与 反应生成 反应生成 和 和 ,该反应的平衡常数 ,该反应的平衡常数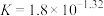 |
您最近一年使用:0次
解题方法
7 . 化学反应在社会发展中运用广泛。下列解释事实的离子方程式正确的是
A.纯碱溶液可以除去油污: |
B.用亚硫酸钠溶液吸收少量氯气: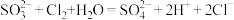 |
C.铅酸蓄电池充电时的阴极电极反应: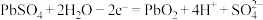 |
D.用醋酸和淀粉—KI溶液检验加碘食盐中所含的碘: |
您最近一年使用:0次
8 . 钛酸亚铁通过以下反应转化为TiCl4: 。设NA为阿伏加德罗常数的值,下列说法正确的是
。设NA为阿伏加德罗常数的值,下列说法正确的是
 。设NA为阿伏加德罗常数的值,下列说法正确的是
。设NA为阿伏加德罗常数的值,下列说法正确的是| A.12g金刚石中含有C—C键数为4 NA |
| B.标准状况下1.12L CO含有质子数为0.7 NA |
| C.每生成2mol TiCl4转移电子数为12 NA |
| D.1L 0.1mol/L的FeCl3溶液中,阳离子数目为0.1 NA |
您最近一年使用:0次
名校
9 . 常温下,向 碱溶液中滴加
碱溶液中滴加 盐酸,溶液的pH及导电能力随滴加盐酸体积的变化曲线如图所示。下列说法正确的是
盐酸,溶液的pH及导电能力随滴加盐酸体积的变化曲线如图所示。下列说法正确的是
 碱溶液中滴加
碱溶液中滴加 盐酸,溶液的pH及导电能力随滴加盐酸体积的变化曲线如图所示。下列说法正确的是
盐酸,溶液的pH及导电能力随滴加盐酸体积的变化曲线如图所示。下列说法正确的是
A. 的电离方程式为 的电离方程式为 |
| B.水的电离程度:b>c>a |
C.b点溶液中 |
D.c点溶液中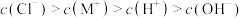 |
您最近一年使用:0次
22-23高二下·云南昆明·期中
10 . 已知常温下溶液中CH3COOH和CH3COO-的物质的量分数与pH的关系如图所示。下列说法正确的是
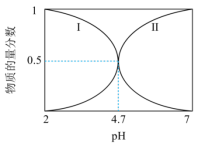
| A.图中曲线I表示的是CH3COO- |
| B.常温下,Ka(CH3COOH)=1×10-4.7 |
| C.0.1mol•L-1CH3COONa溶液中存在等式:c(Na+)+c(CH3COO-)=0.2mol•L-1 |
| D.常温下,浓度均为0.1mol•L-1的CH3COOH和CH3COONa混合溶液中:c(Na+)>c(CH3COOH)>c(CH3COO-)>c(H+)>c(OH-) |
您最近一年使用:0次



