解题方法
1 . 川西地区盐卤浓度较低,为了降低成本,侯德榜对原有的制碱方法——氨碱法(以食盐、氨气、二氧化碳为原料制取碳酸钠)进行改进。下列说法正确的是

| A.二氧化碳为含极性共价键的非极性分子 |
B.实验室可采用如图所示装置来制取 |
| C.工业上常采用电解饱和食盐水的方法来获得金属钠 |
D. 的 的 溶液中, 溶液中, |
您最近一年使用:0次
2 . 河水是主要的饮用水源,污染物通过饮用水可直接毒害人体,也可通过食物链和农田灌溉间接危及人体健康。请回答下列问题。
已知在25℃和T℃时,水的电离平衡曲线如图所示:___________ (填“>”“<”“=”)25℃。
(2)图中四点 间的大小关系:
间的大小关系:___________ (用A、B、C、D表示)。
(3)在新制氯水中加入少量 固体,水的电离平衡移动
固体,水的电离平衡移动___________ (填“向左”“向右”或“不”)。
(4)25℃时,0.1 浓度的
浓度的 溶液与a
溶液与a 醋酸溶液等体积混合后
醋酸溶液等体积混合后 ,醋酸的电离常数为
,醋酸的电离常数为___________ (用含a的式子表示)。
(5)T℃时,将 的
的 溶液与
溶液与 的
的 溶液混合,若所得混合溶液的
溶液混合,若所得混合溶液的 (忽略溶液混合时的体积变化),则
(忽略溶液混合时的体积变化),则 溶液与
溶液与 溶液的体积比为
溶液的体积比为___________ 。
(6) ,25℃时,1.0
,25℃时,1.0
 溶液的
溶液的 约等于
约等于___________ (已知 )。将浓度相等的
)。将浓度相等的 与
与 溶液等体积混合,判断溶液呈
溶液等体积混合,判断溶液呈___________ (填“酸”、“碱”或“中”性,并结合有关数据解释原因:___________ 。
已知在25℃和T℃时,水的电离平衡曲线如图所示:

(2)图中四点
 间的大小关系:
间的大小关系:(3)在新制氯水中加入少量
 固体,水的电离平衡移动
固体,水的电离平衡移动(4)25℃时,0.1
 浓度的
浓度的 溶液与a
溶液与a 醋酸溶液等体积混合后
醋酸溶液等体积混合后 ,醋酸的电离常数为
,醋酸的电离常数为(5)T℃时,将
 的
的 溶液与
溶液与 的
的 溶液混合,若所得混合溶液的
溶液混合,若所得混合溶液的 (忽略溶液混合时的体积变化),则
(忽略溶液混合时的体积变化),则 溶液与
溶液与 溶液的体积比为
溶液的体积比为(6)
 ,25℃时,1.0
,25℃时,1.0
 溶液的
溶液的 约等于
约等于 )。将浓度相等的
)。将浓度相等的 与
与 溶液等体积混合,判断溶液呈
溶液等体积混合,判断溶液呈
您最近一年使用:0次
3 . 常温下,向 溶液中逐滴加入
溶液中逐滴加入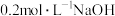 溶液,所得溶液的
溶液,所得溶液的 变化曲线如图所示。下列说法错误的是
变化曲线如图所示。下列说法错误的是
 溶液中逐滴加入
溶液中逐滴加入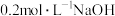 溶液,所得溶液的
溶液,所得溶液的 变化曲线如图所示。下列说法错误的是
变化曲线如图所示。下列说法错误的是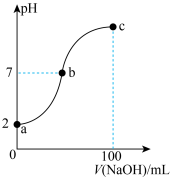
A.a点溶液中,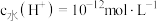 |
B.b点溶液中, |
C.常温下, |
| D.a、b、c三点溶液中,c点溶液中水的电离程度最小 |
您最近一年使用:0次
2024-05-04更新
|
79次组卷
|
2卷引用:河北省保定市部分高中2023-2024学年高二下学期3月月考化学试题
4 . 25℃时,向100mL 0.1
 溶液中滴加0.1
溶液中滴加0.1 KOH溶液,溶液pH与KOH溶液体积的关系曲线如图所示,对图中四个点a、b、c,d的分析中,不正确的是
KOH溶液,溶液pH与KOH溶液体积的关系曲线如图所示,对图中四个点a、b、c,d的分析中,不正确的是

 溶液中滴加0.1
溶液中滴加0.1 KOH溶液,溶液pH与KOH溶液体积的关系曲线如图所示,对图中四个点a、b、c,d的分析中,不正确的是
KOH溶液,溶液pH与KOH溶液体积的关系曲线如图所示,对图中四个点a、b、c,d的分析中,不正确的是
A.a点存在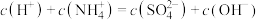 |
B.b点存在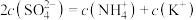 |
C.d点水的电离程度最大,且存在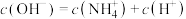 |
D.c点存在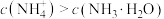 |
您最近一年使用:0次
解题方法
5 . 按要求写出下列离子方程式
(1)(NH4)2SO4水解:_______ 。
(2)NaHCO3水解:_______ 。
(3)Ag2CrO4沉淀溶解平衡:_______ 。
(4)氢氧燃料电池(酸性):已知总电极反应式为H2+ O2=H2O。则负极反应式:
O2=H2O。则负极反应式:_______ 、正极反应式_______ 。
(5)已知AgCl为难溶于水和酸的白色固体,Ag2S为难溶于水和酸的黑色固体。向AgCl和水形成的悬浊液中加入足量的Na2S溶液并振荡,结果白色固体完全转化为黑色固体:
①写出白色固体转化为黑色固体的化学方程式:_______ 。
②简要说明白色固体转化为黑色固体的原因:_______ 。
(1)(NH4)2SO4水解:
(2)NaHCO3水解:
(3)Ag2CrO4沉淀溶解平衡:
(4)氢氧燃料电池(酸性):已知总电极反应式为H2+
 O2=H2O。则负极反应式:
O2=H2O。则负极反应式:(5)已知AgCl为难溶于水和酸的白色固体,Ag2S为难溶于水和酸的黑色固体。向AgCl和水形成的悬浊液中加入足量的Na2S溶液并振荡,结果白色固体完全转化为黑色固体:
①写出白色固体转化为黑色固体的化学方程式:
②简要说明白色固体转化为黑色固体的原因:
您最近一年使用:0次
解题方法
6 . 某学习小组用0.1000mol/LNaOH标准溶液来测定未知物质的量浓度的盐酸时,选择酚酞作指示剂。请回答下列问题:

(1)盛装NaOH标准溶液的仪器名称为______ ,若滴定开始和结束时,该仪器中溶液读数如图所示,所用NaOH标准溶液的体积为______ mL。
(2)某学生根据3次实验分别记录有关数据如表所示:
依据表中数据计算该盐酸的物质的量浓度为______  。
。
(3)下列操作会使所测结果偏高的是______ (填字母)。
A.滴定前用蒸馏水冲洗锥形瓶
B.滴定过程中振荡锥形瓶时不慎将瓶内溶液溅出
C.滴定过程中不慎将数滴碱液滴在锥形瓶外
D.碱式滴定管在滴定前有气泡,滴定后气泡消失
E.读取NaOH体积时,开始仰视读数,滴定结束时俯视读数
(4)用0.1mol/LNaOH溶液分别滴定体积均为20.00mL、浓度均为0.1mol/L的盐酸和醋酸溶液,得到滴定过程中溶液pH随加入NaOH溶液体积而变化的两条滴定曲线。

①滴定醋酸的曲线是______ (填“Ⅰ”或“Ⅱ”)。
② 和
和 的关系:
的关系:
______  (填“>”、“=”或“<”)。
(填“>”、“=”或“<”)。
③M点对应的溶液中,各离子的物质的量浓度由大到小的顺序是______ 。

(1)盛装NaOH标准溶液的仪器名称为
(2)某学生根据3次实验分别记录有关数据如表所示:
| 滴定次数 | 待测盐酸的体积/mL | 标准NaOH溶液体积 | |
| 滴定前的刻度/mL | 滴定后的刻度/mL | ||
| 第一次 | 25.00 | 0.00 | 26.11 |
| 第二次 | 25.00 | 1.56 | 30.30 |
| 第三次 | 25.00 | 0.22 | 26.31 |
 。
。(3)下列操作会使所测结果偏高的是
A.滴定前用蒸馏水冲洗锥形瓶
B.滴定过程中振荡锥形瓶时不慎将瓶内溶液溅出
C.滴定过程中不慎将数滴碱液滴在锥形瓶外
D.碱式滴定管在滴定前有气泡,滴定后气泡消失
E.读取NaOH体积时,开始仰视读数,滴定结束时俯视读数
(4)用0.1mol/LNaOH溶液分别滴定体积均为20.00mL、浓度均为0.1mol/L的盐酸和醋酸溶液,得到滴定过程中溶液pH随加入NaOH溶液体积而变化的两条滴定曲线。

①滴定醋酸的曲线是
②
 和
和 的关系:
的关系:
 (填“>”、“=”或“<”)。
(填“>”、“=”或“<”)。③M点对应的溶液中,各离子的物质的量浓度由大到小的顺序是
您最近一年使用:0次
7 . 盛放NaOH溶液的试剂瓶不能用磨口玻璃塞,原因为 ,生成的Na2SiO3可使玻璃塞与玻璃瓶黏在一起。设NA为阿伏加德罗常数的值,下列说法正确的是
,生成的Na2SiO3可使玻璃塞与玻璃瓶黏在一起。设NA为阿伏加德罗常数的值,下列说法正确的是
 ,生成的Na2SiO3可使玻璃塞与玻璃瓶黏在一起。设NA为阿伏加德罗常数的值,下列说法正确的是
,生成的Na2SiO3可使玻璃塞与玻璃瓶黏在一起。设NA为阿伏加德罗常数的值,下列说法正确的是A. 含有的分子数为NA 含有的分子数为NA |
B.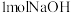 含有的化学键总数目为NA 含有的化学键总数目为NA |
C.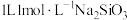 溶液中, 溶液中, 数目为NA 数目为NA |
D.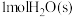 含有的氢键数目为2NA 含有的氢键数目为2NA |
您最近一年使用:0次
8 . 证据推理是化学学科重要核心素养。下列证据能得出相应推论的是
| 选项 | 证据 | 推论 |
| A | 反应2CO2(g)+6H2(g) C2H4(g)+4H2O(g)能自发进行 C2H4(g)+4H2O(g)能自发进行 | 该反应的△H<0 |
| B | 增大压强,化学反应速率加快 | 增大压强,活化分子百分数增多,有效碰撞概率增大 |
| C | 用pH计测定浓度相等的NaClO溶液和Na2CO3溶液的pH,NaClO溶液碱性更强 | 酸性:H2CO3>HClO |
| D | 向双氧水中滴加浓硫酸,产生气体的速率加快 | 浓硫酸对H2O2的分解具有催化作用 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
9 .  是阿伏加德罗常数的值,下列说法不正确的是
是阿伏加德罗常数的值,下列说法不正确的是
 是阿伏加德罗常数的值,下列说法不正确的是
是阿伏加德罗常数的值,下列说法不正确的是A. 中 中 键的个数为 键的个数为 |
B. 碘蒸气和 碘蒸气和 氢气在密闭容器中充分反应,生成的碘化氢分子数小于 氢气在密闭容器中充分反应,生成的碘化氢分子数小于 |
C.电解饱和食盐水时,若阴阳两极产生气体的总质量为 ,则转移电子数为 ,则转移电子数为 |
D.向 溶液中通入氨气至中性,铵根离子数小于 溶液中通入氨气至中性,铵根离子数小于 |
您最近一年使用:0次
名校
10 . 水是最常用的溶剂,许多化学反应都需要在水溶液中进行,用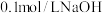 溶液滴定体积均为
溶液滴定体积均为 、浓度均为
、浓度均为 盐酸和醋酸溶液,得到如图所示的滴定曲线,下列说法正确的是
盐酸和醋酸溶液,得到如图所示的滴定曲线,下列说法正确的是

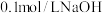 溶液滴定体积均为
溶液滴定体积均为 、浓度均为
、浓度均为 盐酸和醋酸溶液,得到如图所示的滴定曲线,下列说法正确的是
盐酸和醋酸溶液,得到如图所示的滴定曲线,下列说法正确的是
A.用 溶液滴定醋酸溶液通常选择的指示剂为甲基橙,符合其滴定曲线的是Ⅰ 溶液滴定醋酸溶液通常选择的指示剂为甲基橙,符合其滴定曲线的是Ⅰ |
B. 盐酸和醋酸溶液中,由水电离出的 盐酸和醋酸溶液中,由水电离出的 较大的是盐酸 较大的是盐酸 |
C. |
D.曲线Ⅰ中M点对应的溶液中,各离子的浓度由大到小的顺序是 |
您最近一年使用:0次



