名校
1 . 为了除去氯化铜酸性溶液中的 离子,可在加热搅拌下加入一种试剂,过滤后再加入适量盐酸。这种试剂是
离子,可在加热搅拌下加入一种试剂,过滤后再加入适量盐酸。这种试剂是
 离子,可在加热搅拌下加入一种试剂,过滤后再加入适量盐酸。这种试剂是
离子,可在加热搅拌下加入一种试剂,过滤后再加入适量盐酸。这种试剂是| A.氧化铜 | B.氢氧化钠 | C.碳酸钠 | D.氨水 |
您最近一年使用:0次
2 . 常温下,下列各组离子在指定溶液中能大量共存的是
A.使甲基橙呈红色的溶液中: |
B.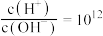 的水溶液中: 的水溶液中: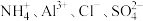 |
C.由水电离出的 的溶液中: 的溶液中: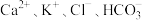 |
D. 的溶液中: 的溶液中: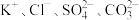 |
您最近一年使用:0次
名校
3 . 室温下,物质的量浓度相同的三种盐 溶液,其
溶液,其 依次为8、9、10。下列有关说法正确的是
依次为8、9、10。下列有关说法正确的是
 溶液,其
溶液,其 依次为8、9、10。下列有关说法正确的是
依次为8、9、10。下列有关说法正确的是A.HX、HY、HZ三种酸的强弱顺序为: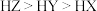 |
B. HX是强酸, 是弱酸,且酸HY强于酸 是弱酸,且酸HY强于酸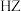 |
C. 三种酸根均能水解,且水解程度 三种酸根均能水解,且水解程度 |
D.三种盐溶液中 的浓度大小顺序为 的浓度大小顺序为 |
您最近一年使用:0次
名校
4 . 溶液中的化学反应大多数是离子反应,根据要求回答问题:
(1)明矾可作净水剂,原理为:_______ (用离子方程式表示)。
(2)完成 溶液粒子浓度关系:
溶液粒子浓度关系:
①离子浓度大小关系_______ 。
②电荷守恒关系_______ 。
③物料守恒关系_______ 。
(3) 的水溶液呈酸性,其原因是
的水溶液呈酸性,其原因是_______ (用离子方程式表示)。
(4)将 溶液蒸干、灼烧,最后得到的主要固体产物是
溶液蒸干、灼烧,最后得到的主要固体产物是_______ 。
(5) 水溶液呈酸性的原因是
水溶液呈酸性的原因是 的水解程度
的水解程度_______ 电离程度(填大于或小于)。
(6)相同温度下,相同物质的量浓度的下列溶液:① 、②
、② 、③
、③ 、④
、④ ⑤
⑤ 、⑥
、⑥ 按
按 由大到小的排列为:
由大到小的排列为:_______ (填序号)
(1)明矾可作净水剂,原理为:
(2)完成
 溶液粒子浓度关系:
溶液粒子浓度关系:①离子浓度大小关系
②电荷守恒关系
③物料守恒关系
(3)
 的水溶液呈酸性,其原因是
的水溶液呈酸性,其原因是(4)将
 溶液蒸干、灼烧,最后得到的主要固体产物是
溶液蒸干、灼烧,最后得到的主要固体产物是(5)
 水溶液呈酸性的原因是
水溶液呈酸性的原因是 的水解程度
的水解程度(6)相同温度下,相同物质的量浓度的下列溶液:①
 、②
、② 、③
、③ 、④
、④ ⑤
⑤ 、⑥
、⑥ 按
按 由大到小的排列为:
由大到小的排列为:
您最近一年使用:0次
名校
5 . 按要求填空
(1)某温度时,测得0.01mol/L的NaOH溶液的pH为11,则该温度下水的离子积常数
___________ ,该温度(填“>”“<”或“=”)___________ 25℃。
(2) 时,
时, 均等于
均等于 的醋酸溶液和氯化铵溶液,醋酸溶液中水电离出的
的醋酸溶液和氯化铵溶液,醋酸溶液中水电离出的 浓度与氯化铵溶液中水电离出的
浓度与氯化铵溶液中水电离出的 浓度之比是
浓度之比是___________ 。
(3)常温下,向10mL浓度均为0.01mol/L的HCl和CH3COOH的混合溶液中加入等体积0.02mol/L的NaOH溶液,充分反应后混合溶液呈___________ (填“酸性”“碱性”或“中性”),混合溶液中离子浓度由大到小的顺序为___________ 。
(4)大量的碘富集在海藻中,用水浸取后浓缩,该浓缩液中主要含有 、
、 等离子。取一定量的浓缩液,向其中滴加
等离子。取一定量的浓缩液,向其中滴加 溶液,当
溶液,当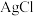 开始沉淀时,溶液中
开始沉淀时,溶液中 为
为___________ 已知 。
。
(1)某温度时,测得0.01mol/L的NaOH溶液的pH为11,则该温度下水的离子积常数

(2)
 时,
时, 均等于
均等于 的醋酸溶液和氯化铵溶液,醋酸溶液中水电离出的
的醋酸溶液和氯化铵溶液,醋酸溶液中水电离出的 浓度与氯化铵溶液中水电离出的
浓度与氯化铵溶液中水电离出的 浓度之比是
浓度之比是(3)常温下,向10mL浓度均为0.01mol/L的HCl和CH3COOH的混合溶液中加入等体积0.02mol/L的NaOH溶液,充分反应后混合溶液呈
(4)大量的碘富集在海藻中,用水浸取后浓缩,该浓缩液中主要含有
 、
、 等离子。取一定量的浓缩液,向其中滴加
等离子。取一定量的浓缩液,向其中滴加 溶液,当
溶液,当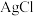 开始沉淀时,溶液中
开始沉淀时,溶液中 为
为 。
。
您最近一年使用:0次
名校
解题方法
6 . 按要求填空
(1)50 mL0.25 mol/LH2SO4溶液与50 mL 0.55 mol/LNaOH溶液充分反应,测得放出1.4 kJ的热量,写出该过程表示中和热的热化学方程式:___________ 。
(2)向纯碱溶液中滴加酚酞,溶液变为___________ ,原因是___________ 、___________ (用离子方程式表示)。
(3)金属焊接时可用NH4Cl溶液做除锈剂的原因是___________ (用离子方程式表示)。
(4)配制FeSO4溶液时,通常向配好的溶液中加入___________ 和___________ 。
(5)泡沫灭火器中的药品是 、
、 ,用离子方程式表示泡沫灭火器的原理
,用离子方程式表示泡沫灭火器的原理___________ 。外筒的材质是铁,内筒是玻璃,则外筒应该盛放___________ 溶液。
(6)常温下,取 溶液与
溶液与 溶液等体积混合,测得混合后溶液的
溶液等体积混合,测得混合后溶液的 ,则
,则 的
的 溶液的浓度
溶液的浓度___________  (填<、>或=)。
(填<、>或=)。
(7)0.1 mol/L的 溶液,测得溶液显碱性。则该溶液中
溶液,测得溶液显碱性。则该溶液中
___________  (填<、>或=)。
(填<、>或=)。
(1)50 mL0.25 mol/LH2SO4溶液与50 mL 0.55 mol/LNaOH溶液充分反应,测得放出1.4 kJ的热量,写出该过程表示中和热的热化学方程式:
(2)向纯碱溶液中滴加酚酞,溶液变为
(3)金属焊接时可用NH4Cl溶液做除锈剂的原因是
(4)配制FeSO4溶液时,通常向配好的溶液中加入
(5)泡沫灭火器中的药品是
 、
、 ,用离子方程式表示泡沫灭火器的原理
,用离子方程式表示泡沫灭火器的原理(6)常温下,取
 溶液与
溶液与 溶液等体积混合,测得混合后溶液的
溶液等体积混合,测得混合后溶液的 ,则
,则 的
的 溶液的浓度
溶液的浓度 (填<、>或=)。
(填<、>或=)。(7)0.1 mol/L的
 溶液,测得溶液显碱性。则该溶液中
溶液,测得溶液显碱性。则该溶液中
 (填<、>或=)。
(填<、>或=)。
您最近一年使用:0次
名校
解题方法
7 . 有溶质的物质的量浓度均为0.1 mol/L的下列八种溶液①HCl ②H2SO4 ③CH3COOH ④(NH4)2SO4 ⑤KOH ⑥NaF ⑦KCl ⑧NH4Cl这些溶液的pH由小到大的顺序是
| A.②①③④⑧⑦⑥⑤ | B.②①③⑥⑦⑧⑤④ |
| C.①②③⑧⑦⑥④⑤ | D.②①⑧③⑥④⑤⑦ |
您最近一年使用:0次
名校
8 . I.常温下,有四种溶液:①0.1mol/LCH3COOH溶液②0.1mol/LCH3COONa溶液③0.1mol/LNaHSO3溶液④0.1mol/LNaHCO3溶液。
(1)溶液①的pH___________ 7(填“>”“<”或“=”),溶液中离子的电荷守恒的关系式是___________ 。
(2)溶液②呈________ (填“酸”“碱”或“中”)性。其原因是_________ (用离子方程式说明)。
(3)下列有关①和②两种溶液的说法不正确的是___________ (填字母)。
a.两种溶液中c(CH3COO-)都等于0.1mol/L
b.两种溶液中c(CH3COO-)都小于0.1mol/L
c.CH3COOH溶液中c(CH3COO-)小于CH3COONa溶液中c(CH3COO-)
(4)NaHSO3溶液的pH<7,NaHCO3溶液的pH>7,则NaHSO3溶液c(H2SO3)___________ c( )(填“>”“<”或“=”,下同),NaHCO3溶液中c(H2CO3)
)(填“>”“<”或“=”,下同),NaHCO3溶液中c(H2CO3)___________ c( )。
)。
Ⅱ.
(5)醋酸(CH3COOH)属于___________ 电解质(填“强”、“弱”或“非”),常温下, 溶液中,
溶液中,
___________  (填“>”“<”或“=”);
(填“>”“<”或“=”); 溶液的
溶液的
___________ 。
(6)常温下,pH=4的醋酸溶液与pH=10的纯碱溶液中,水电离出的c(OH-)之比为________ 。
(7)将 溶液和
溶液和 溶液混合,若混合后溶液呈中性,则溶液中
溶液混合,若混合后溶液呈中性,则溶液中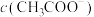
________  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(8)25℃时,H2A的电离常数Ka1=1×10-2,Ka2=6×10-8,则该温度下NaHA水解反应的平衡常数Kh=___________ ,NaHA溶液呈___________ 性。(填“酸”“碱”或“中”)
(1)溶液①的pH
(2)溶液②呈
(3)下列有关①和②两种溶液的说法不正确的是
a.两种溶液中c(CH3COO-)都等于0.1mol/L
b.两种溶液中c(CH3COO-)都小于0.1mol/L
c.CH3COOH溶液中c(CH3COO-)小于CH3COONa溶液中c(CH3COO-)
(4)NaHSO3溶液的pH<7,NaHCO3溶液的pH>7,则NaHSO3溶液c(H2SO3)
 )(填“>”“<”或“=”,下同),NaHCO3溶液中c(H2CO3)
)(填“>”“<”或“=”,下同),NaHCO3溶液中c(H2CO3) )。
)。Ⅱ.
(5)醋酸(CH3COOH)属于
 溶液中,
溶液中,
 (填“>”“<”或“=”);
(填“>”“<”或“=”); 溶液的
溶液的
(6)常温下,pH=4的醋酸溶液与pH=10的纯碱溶液中,水电离出的c(OH-)之比为
(7)将
 溶液和
溶液和 溶液混合,若混合后溶液呈中性,则溶液中
溶液混合,若混合后溶液呈中性,则溶液中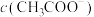
 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。(8)25℃时,H2A的电离常数Ka1=1×10-2,Ka2=6×10-8,则该温度下NaHA水解反应的平衡常数Kh=
您最近一年使用:0次
名校
解题方法
9 . 中山市马拉松赛事中,组委会设置了众多的补水点。研究表明,喝弱碱性水更符合人的机理特征。下列物质能促进水电离,且显碱性的是
| A.KCl | B.NaOH | C.Na2S | D.NH4Cl |
您最近一年使用:0次
名校
解题方法
10 . 下列离子方程式正确的是
A.用KIO3氧化酸性溶液中的KI: 5I-+ IO +3H2O = 3I2 + 6OH- +3H2O = 3I2 + 6OH- |
B.用稀硝酸洗涤试管内壁的银镜: Ag +2H++ NO = Ag++ NO↑+ H2O = Ag++ NO↑+ H2O |
C.NaHS溶液水解:HS-+H2O H3O++S2- H3O++S2- |
D.将 溶液加入到石灰乳中得到氢氧化镁: 溶液加入到石灰乳中得到氢氧化镁: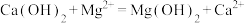 |
您最近一年使用:0次



