1 . 由下列实验事实所得出的结论正确的是
| 选项 | 实验事实 | 结论 |
| A | 密闭容器中发生反应 ,压缩容器体积,气体颜色变深 ,压缩容器体积,气体颜色变深 | 增大压强,平衡向逆反应方向移动 |
| B | 在恒温恒容下发生反应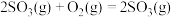 , , 的体积分数不再变化 的体积分数不再变化 | 该反应达到了平衡状态 |
| C | 浓度相同的盐酸和醋酸分别与等质量的形状相同的锌粒反应,前者反应速率快 | 金属与酸的反应中,酸的浓度对反应速率无影响 |
| D | 向含有酚酞的 溶液中加入少量BaCl2固体,溶液红色变浅 溶液中加入少量BaCl2固体,溶液红色变浅 |  溶液中存在水解平衡 溶液中存在水解平衡 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2 . 物质的量浓度相同的 和
和 的溶液,其
的溶液,其 分别为8和9,据此,下列对两种对应酸(
分别为8和9,据此,下列对两种对应酸( 和
和 )在相同温度和浓度下的比较中错误的是
)在相同温度和浓度下的比较中错误的是
 和
和 的溶液,其
的溶液,其 分别为8和9,据此,下列对两种对应酸(
分别为8和9,据此,下列对两种对应酸( 和
和 )在相同温度和浓度下的比较中错误的是
)在相同温度和浓度下的比较中错误的是A.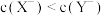 | B.电离程度: |
C.溶液的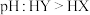 | D.溶液中的 |
您最近一年使用:0次
名校
3 . 下列物质溶解于水时,电离出的阴离子能使水的电离平衡向右移动的是
A. | B. | C. | D. |
您最近一年使用:0次
2024-01-24更新
|
44次组卷
|
8卷引用:湖南省娄底市第一中学2020-2021学年高二上学期期中考试化学(高考班)试题
名校
4 . 常温下,下列各组离子在指定溶液中能大量共存的是
A.能使甲基橙变红的溶液: |
B.澄清透明溶液中: |
C.在新制饱和氯水中: |
D.水电离的 的溶液: 的溶液: |
您最近一年使用:0次
2024-01-21更新
|
305次组卷
|
4卷引用:专题05 盐类的水解-【寒假自学课】2024年高二化学寒假提升学与练(人教版2019)
(已下线)专题05 盐类的水解-【寒假自学课】2024年高二化学寒假提升学与练(人教版2019)广东省汕头市金山中学2023-2024学年高二上学期期中考试 化学试题福建省厦门外国语学校2023-2024学年高二上学期期末模拟考试化学试题宁夏回族自治区石嘴山市第三中学2023-2024学年高二上学期1月期末化学试题
名校
解题方法
5 . 下列有关实验操作、现象和解释或结论都正确的是
| 选项 | 操作 | 现象 | 解释或结论 |
| A | 在 与 与 的混合液中再加入 的混合液中再加入 固体 固体 | 溶液颜色变浅 | 增大生成物浓度,平衡逆向移动 |
| B | 常温下,向等体积、等浓度的 和 和 溶液中分别滴加2滴酚酞 溶液中分别滴加2滴酚酞 | 两份溶液变红, 溶液红色更深 溶液红色更深 | 常温下的水解平衡常数: |
| C | 向重铬酸钾溶液中加水 | 溶液颜色变浅 | 增加反应物 的用量,平衡 的用量,平衡 向右移动 向右移动 |
| D | 向 溶液中加入过量的 溶液中加入过量的 溶液,再加入 溶液,再加入 溶液 溶液 | 产生黄色沉淀 |  |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
6 . 下列有关电解质溶液的说法正确的是
A.室温下,pH=3的 溶液与pH=11的 溶液与pH=11的 溶液等体积混合,溶液pH<7 溶液等体积混合,溶液pH<7 |
B.向盐酸中加入氨水至中性,溶液中 |
C.将 溶液从 溶液从 升温至 升温至 ,溶液中 ,溶液中 增大 增大 |
D.浓度均为 的 的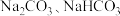 混合溶液中: 混合溶液中: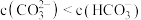 ,且 ,且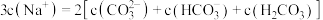 |
您最近一年使用:0次
名校
解题方法
7 . 某同学在实验室探究 的性质:常温下,配制
的性质:常温下,配制 溶液,测其
溶液,测其 为8.4;取少量该溶液滴加
为8.4;取少量该溶液滴加 溶液至
溶液至 ,滴加过程中产生白色沉淀,但无气体放出,下列说法
,滴加过程中产生白色沉淀,但无气体放出,下列说法不正确 的是
 的性质:常温下,配制
的性质:常温下,配制 溶液,测其
溶液,测其 为8.4;取少量该溶液滴加
为8.4;取少量该溶液滴加 溶液至
溶液至 ,滴加过程中产生白色沉淀,但无气体放出,下列说法
,滴加过程中产生白色沉淀,但无气体放出,下列说法A.加入 促进了 促进了 的电离 的电离 |
B. 溶液呈碱性的原因是 溶液呈碱性的原因是 的水解程度大于电离程度 的水解程度大于电离程度 |
C.反应的离子方程式是 |
D.反应后的上层清液中存在: |
您最近一年使用:0次
名校
解题方法
8 . 常温下,下列各组离子在指定溶液中,一定可以大量共存的是
A.无色溶液中: |
B. 的溶液中: 的溶液中: |
C.含 的溶液中: 的溶液中: |
D.在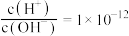 的溶液中: 的溶液中: |
您最近一年使用:0次
名校
9 . 已知常温时HClO和 的电离平衡常数分别为
的电离平衡常数分别为 和
和 。现将pH和体积都相同的两种酸溶液分别加蒸馏水稀释,pH随溶液体积的变化如图所示,下列叙述正确的是
。现将pH和体积都相同的两种酸溶液分别加蒸馏水稀释,pH随溶液体积的变化如图所示,下列叙述正确的是

 的电离平衡常数分别为
的电离平衡常数分别为 和
和 。现将pH和体积都相同的两种酸溶液分别加蒸馏水稀释,pH随溶液体积的变化如图所示,下列叙述正确的是
。现将pH和体积都相同的两种酸溶液分别加蒸馏水稀释,pH随溶液体积的变化如图所示,下列叙述正确的是
A.曲线Ⅱ为 稀释时pH变化曲线 稀释时pH变化曲线 |
| B.b点溶液中水的电离程度比c点溶液中水的电离程度大 |
C.从b点到d点,溶液中 减小(HR代表HClO或 减小(HR代表HClO或 ) ) |
D.取a点的两种酸溶液,中和相同体积、相同浓度的NaOH溶液,消耗 的体积较小 的体积较小 |
您最近一年使用:0次
2024-01-12更新
|
86次组卷
|
6卷引用:【定心卷】3.1.3 电离平衡常数随堂练习-人教版2023-2024学年选择性必修1
名校
10 . 研究化学反应意义重大,请就下列现象和实质回答问题。
(1) 可用作白色颜料和阻燃剂等。在实验室中可利用
可用作白色颜料和阻燃剂等。在实验室中可利用 的水解反应制取
的水解反应制取 (
( 的水解分三步进行,中间产物有
的水解分三步进行,中间产物有 等),写出
等),写出 水解生成
水解生成 的水解反应方程式
的水解反应方程式_________ ; 水解的总反应可表示为:
水解的总反应可表示为: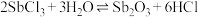 为了得到较多的
为了得到较多的 ,操作时要将
,操作时要将 缓慢加入大量水中的原因是
缓慢加入大量水中的原因是___________ 。
(2)次磷酸 是一种弱酸,
是一种弱酸, 溶液和足量
溶液和足量 溶液混合,所得溶液中阴离子只有
溶液混合,所得溶液中阴离子只有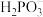 、
、 、
、 三种。写出
三种。写出 溶液与
溶液与 溶液恰好完全中和的溶液中各离子浓度由大到小的顺序为
溶液恰好完全中和的溶液中各离子浓度由大到小的顺序为___________ 。
(3)已知 与
与 溶液反应生成
溶液反应生成 ,与稀硫酸反应生成
,与稀硫酸反应生成 ,写出
,写出 在水中的电离方程式
在水中的电离方程式___________ 、___________ 。
(4)一定温度下,用水吸收 气体时,溶液中水的电离平衡
气体时,溶液中水的电离平衡___________ 移动(填“向左”“向右”或“不”);若得到 的
的 溶液,试计算溶液中
溶液,试计算溶液中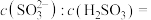
___________ (已知该温度下, 的电离常数:
的电离常数: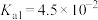 ,
, )。
)。
(5)某温度下, 的盐酸中
的盐酸中 ;该温度下
;该温度下 的
的 溶液与
溶液与 的
的 溶液混合后溶液的
溶液混合后溶液的 ,则
,则 与
与 溶液的体积比为
溶液的体积比为___________ 。
(6)25℃时,若向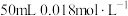 的
的 溶液中加入
溶液中加入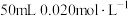 的盐酸,混合后溶液中的
的盐酸,混合后溶液中的 为
为___________  (25℃时,
(25℃时, )。
)。
(1)
 可用作白色颜料和阻燃剂等。在实验室中可利用
可用作白色颜料和阻燃剂等。在实验室中可利用 的水解反应制取
的水解反应制取 (
( 的水解分三步进行,中间产物有
的水解分三步进行,中间产物有 等),写出
等),写出 水解生成
水解生成 的水解反应方程式
的水解反应方程式 水解的总反应可表示为:
水解的总反应可表示为: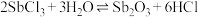 为了得到较多的
为了得到较多的 ,操作时要将
,操作时要将 缓慢加入大量水中的原因是
缓慢加入大量水中的原因是(2)次磷酸
 是一种弱酸,
是一种弱酸, 溶液和足量
溶液和足量 溶液混合,所得溶液中阴离子只有
溶液混合,所得溶液中阴离子只有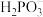 、
、 、
、 三种。写出
三种。写出 溶液与
溶液与 溶液恰好完全中和的溶液中各离子浓度由大到小的顺序为
溶液恰好完全中和的溶液中各离子浓度由大到小的顺序为(3)已知
 与
与 溶液反应生成
溶液反应生成 ,与稀硫酸反应生成
,与稀硫酸反应生成 ,写出
,写出 在水中的电离方程式
在水中的电离方程式(4)一定温度下,用水吸收
 气体时,溶液中水的电离平衡
气体时,溶液中水的电离平衡 的
的 溶液,试计算溶液中
溶液,试计算溶液中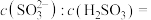
 的电离常数:
的电离常数: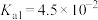 ,
, )。
)。(5)某温度下,
 的盐酸中
的盐酸中 ;该温度下
;该温度下 的
的 溶液与
溶液与 的
的 溶液混合后溶液的
溶液混合后溶液的 ,则
,则 与
与 溶液的体积比为
溶液的体积比为(6)25℃时,若向
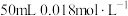 的
的 溶液中加入
溶液中加入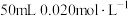 的盐酸,混合后溶液中的
的盐酸,混合后溶液中的 为
为 (25℃时,
(25℃时, )。
)。
您最近一年使用:0次



