1 . 完成下列问题。
(1) 水溶液呈酸性的原因是(用离子方程式表示):
水溶液呈酸性的原因是(用离子方程式表示):________ 。
(2)室温时, 的
的 溶液中由水电离出的
溶液中由水电离出的
______  。
。
(3)室温时, 的Ba(OH)2溶液,
的Ba(OH)2溶液,
________ 。
(4)室温下pH=3的 水溶液水电离的c(H+)
水溶液水电离的c(H+)______  。
。
(5)常温下pH=13的 溶液与pH=11
溶液与pH=11 溶液等体积混合,混合溶液pH=
溶液等体积混合,混合溶液pH=______ 。
(6)常温下0.1 的NH3·H2O,pH=11,则Kb=
的NH3·H2O,pH=11,则Kb=_______ ,常温下0.1 的CH3COOH溶液pH=3 ,则Ka=
的CH3COOH溶液pH=3 ,则Ka=_______ 。
(1)
 水溶液呈酸性的原因是(用离子方程式表示):
水溶液呈酸性的原因是(用离子方程式表示):(2)室温时,
 的
的 溶液中由水电离出的
溶液中由水电离出的
 。
。(3)室温时,
 的Ba(OH)2溶液,
的Ba(OH)2溶液,
(4)室温下pH=3的
 水溶液水电离的c(H+)
水溶液水电离的c(H+) 。
。(5)常温下pH=13的
 溶液与pH=11
溶液与pH=11 溶液等体积混合,混合溶液pH=
溶液等体积混合,混合溶液pH=(6)常温下0.1
 的NH3·H2O,pH=11,则Kb=
的NH3·H2O,pH=11,则Kb= 的CH3COOH溶液pH=3 ,则Ka=
的CH3COOH溶液pH=3 ,则Ka=
您最近一年使用:0次
2 . 部分弱电解质的电离常数如表所示。
下列说法错误的是
| 弱电解质 | HCOOH | HCN | H2CO3 |
| 电离常数(25℃) | Ka=1.8×10-4 | Ka=6.2×10-10 |  =4.5×10-7 =4.5×10-7 =4.7×10-11 =4.7×10-11 |
A.结合H+的能力: >CN-> >CN-> >HCOO- >HCOO- |
B.反应2CN-+H2O+CO2=2HCN+C 能发生 能发生 |
| C.中和等体积、等c(H+)的HCOOH和HCN,消耗NaOH的量前者小于后者 |
D.25℃时,反应HCOOH+CN- HCN+HCOO-的化学平衡常数约为2.9×105 HCN+HCOO-的化学平衡常数约为2.9×105 |
您最近一年使用:0次
3 . 已知常温下部分弱电解质的电离平衡常数如表:
(1)常温下,pH相同的三种溶液①NaF溶液;②NaClO溶液;③Na2CO3溶液,其物质的量浓度由大到小的顺序是_______ 。(填序号)
(2)向足量的次氯酸钠中通入少量的二氧化碳的离子方程式_______ 。
(3)室温下,经测定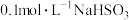 溶液
溶液 ,则
,则
_______  (填“>”、“=”、“<”)。
(填“>”、“=”、“<”)。
(4) 时,将
时,将 的氨水与
的氨水与 的盐酸等体积混合所得溶液中
的盐酸等体积混合所得溶液中 ,则溶液显
,则溶液显_______ (填“酸”“碱”或“中”)性;用含a的代数式表示 的电离平衡常数
的电离平衡常数
_______ 。
(5)将含 的烟气通入该氨水中,当溶液显中性时,溶液中
的烟气通入该氨水中,当溶液显中性时,溶液中
_______ 。
| 化学式 |  |  |  |  |  |
| 电离常数 |  |  |  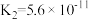 |   |  |
(2)向足量的次氯酸钠中通入少量的二氧化碳的离子方程式
(3)室温下,经测定
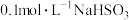 溶液
溶液 ,则
,则
 (填“>”、“=”、“<”)。
(填“>”、“=”、“<”)。(4)
 时,将
时,将 的氨水与
的氨水与 的盐酸等体积混合所得溶液中
的盐酸等体积混合所得溶液中 ,则溶液显
,则溶液显 的电离平衡常数
的电离平衡常数
(5)将含
 的烟气通入该氨水中,当溶液显中性时,溶液中
的烟气通入该氨水中,当溶液显中性时,溶液中
您最近一年使用:0次
4 . 下列叙述正确的是
A.将 溶液从 溶液从 升温至 升温至 ,溶液中 ,溶液中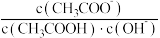 增大 增大 |
B.向盐酸中加入氨水至中性,溶液中 |
C. 时, 时, 的 的 溶液比等浓度的 溶液比等浓度的 溶液的导电能力弱 溶液的导电能力弱 |
D. 时, 时, 一元酸 一元酸 与 与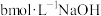 溶液等体积混合后所得溶液的 溶液等体积混合后所得溶液的 为 为 ,则 ,则 |
您最近一年使用:0次
5 . 草酸是植物(特别是草本植物)常具有的成分,有广泛的用途。草酸晶体( )无色,熔点为101℃,易溶于水。常温下草酸的电离常数
)无色,熔点为101℃,易溶于水。常温下草酸的电离常数 ,
, 。
。
(1)写出草酸第一步电离方程式:______
(2)草酸具有很强的还原性,与氧化剂作用易被氧化成二氧化碳和水,可以使酸性高锰酸钾( )溶液褪色,写出发生反应的离子方程式:
)溶液褪色,写出发生反应的离子方程式:______ 。为了探究浓度对化学反应速率的影响,相同温度条件下,分别用2支试管设计了如下实验:
此实验中,加入 溶液的体积应为
溶液的体积应为______ mL。
(3)结合题干所给的电离平衡常数,判断 溶液的酸碱性,应显
溶液的酸碱性,应显______ 性(填“酸”或“碱”)。
(4)设计实验证明草酸为弱酸的方案及其现象均正确的有______(填序号)。
(5)为测定某 溶液的浓度,取20.00mL
溶液的浓度,取20.00mL 溶液于锥形瓶中,滴入2~3滴指示剂,用0.1000mol/L的NaOH溶液进行滴定,并进行3次平行实验,所用NaOH溶液体积分别为19.98mL、20.02mL和22.02mL。
溶液于锥形瓶中,滴入2~3滴指示剂,用0.1000mol/L的NaOH溶液进行滴定,并进行3次平行实验,所用NaOH溶液体积分别为19.98mL、20.02mL和22.02mL。
①若所用指示剂为酚酞,则滴定终点时的现象为______ ;
② 溶液物质的量浓度为
溶液物质的量浓度为______ mol/L;
③下列操作会引起测定结果偏高的是______ (填序号)。
A.滴定管在盛装NaOH溶液前未润洗
B.滴定过程中,锥形瓶震荡的太剧烈,以致部分液体溅出
C.锥形瓶水洗后未干燥
D.滴定前读数正确,滴定终点时仰视读数
 )无色,熔点为101℃,易溶于水。常温下草酸的电离常数
)无色,熔点为101℃,易溶于水。常温下草酸的电离常数 ,
, 。
。(1)写出草酸第一步电离方程式:
(2)草酸具有很强的还原性,与氧化剂作用易被氧化成二氧化碳和水,可以使酸性高锰酸钾(
 )溶液褪色,写出发生反应的离子方程式:
)溶液褪色,写出发生反应的离子方程式:试管 | A | B |
加入试剂 | 4mL 0.01moL/L | ______0.02moL/L |
1mL 0.1moL/L | 1mL 0.1moL/L | |
2mL 0.1moL/L | 2mL 0.1moL/L |
 溶液的体积应为
溶液的体积应为(3)结合题干所给的电离平衡常数,判断
 溶液的酸碱性,应显
溶液的酸碱性,应显(4)设计实验证明草酸为弱酸的方案及其现象均正确的有______(填序号)。
A.室温下,取0.01mol/L 溶液,测其pH=2; 溶液,测其pH=2; |
B.室温下,取0.01mol/L 溶液,测其pH>7; 溶液,测其pH>7; |
C.室温下,取pH=a( )的 )的 溶液稀释100倍后,测其 溶液稀释100倍后,测其 ; ; |
D.标况下,取0.1moL/L的 溶液100mL与足量锌粉反应,收集到 溶液100mL与足量锌粉反应,收集到 体积为224mL; 体积为224mL; |
 溶液的浓度,取20.00mL
溶液的浓度,取20.00mL 溶液于锥形瓶中,滴入2~3滴指示剂,用0.1000mol/L的NaOH溶液进行滴定,并进行3次平行实验,所用NaOH溶液体积分别为19.98mL、20.02mL和22.02mL。
溶液于锥形瓶中,滴入2~3滴指示剂,用0.1000mol/L的NaOH溶液进行滴定,并进行3次平行实验,所用NaOH溶液体积分别为19.98mL、20.02mL和22.02mL。①若所用指示剂为酚酞,则滴定终点时的现象为
②
 溶液物质的量浓度为
溶液物质的量浓度为③下列操作会引起测定结果偏高的是
A.滴定管在盛装NaOH溶液前未润洗
B.滴定过程中,锥形瓶震荡的太剧烈,以致部分液体溅出
C.锥形瓶水洗后未干燥
D.滴定前读数正确,滴定终点时仰视读数
您最近一年使用:0次
名校
解题方法
6 . 常温下,下列有关叙述不正确的是
A.若 溶液的 溶液的 ,则 ,则 |
B.0.2mol/L的亚硫酸氢钠溶液中: |
C. 和 和 混合溶液中: 混合溶液中: |
D.已知 的 的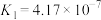 , , ,则NaHA溶液呈碱性 ,则NaHA溶液呈碱性 |
您最近一年使用:0次
名校
7 . 利用Ce(SO4)2溶液处理尾气中的SO2和NO,获得Na2S2O4和NH4NO3的流程如图:

A.“装置I”所得NaHSO3溶液pH<7,则溶液中:c( )>c( )>c( ) ) |
| B.“装置II”中每消耗1molCe4+可吸收22.4LNO |
C.“装置III”为电解槽,阴极反应为2 -2e-= -2e-=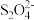 +2OH- +2OH- |
D.“装置IV”所得NH4NO3溶液中存在c( )+c(H+)=c( )+c(H+)=c( ) ) |
您最近一年使用:0次
解题方法
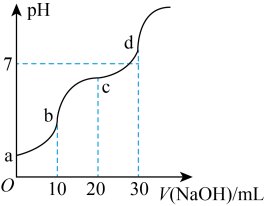
8 . 常温下,向10.00mL0.10mol/LHCl和0.20mol/LCH3COOH的混合溶液中逐滴加入0.10mol/LNaOH溶液时,溶液的pH与所加NaOH溶液体积的关系如图所示(不考虑挥发),且CH3COOH的电离常数Ka=1.0×10-5。已知指示剂变色范围为甲基橙(3.1~4.4),酚酞(8.2~10.0),下列说法不正确的是
| A.测定盐酸浓度时,可选用酚酞或甲基橙作为指示剂 |
| B.点b处c(CH3COOH)+c(CH3COO-)=0.1mol/L |
| C.点b处溶液pH为3 |
| D.点c处溶液中粒子浓度大小关系为c(Na+)>c(Cl-)>c(CH3COOH)>c(H+)>c(OH-) |
您最近一年使用:0次
名校
解题方法
9 . 室温下: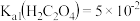 、
、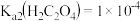 、
、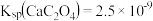 。 通过下列实验探究某些草酸盐的性质。
。 通过下列实验探究某些草酸盐的性质。
实验 :用
:用 计测得
计测得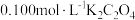 溶液的
溶液的
实验 :向
:向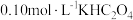 溶液中滴入少量酸性高锰酸钾溶液,振荡后溶液紫色褪去。
溶液中滴入少量酸性高锰酸钾溶液,振荡后溶液紫色褪去。
实验 :向
:向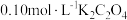 溶液中滴加一定浓度的稀盐酸后,混合溶液的
溶液中滴加一定浓度的稀盐酸后,混合溶液的
实验 :向
:向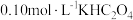 溶液加入一定体积的等浓度
溶液加入一定体积的等浓度 溶液产生白色沉淀,测得上层清液
溶液产生白色沉淀,测得上层清液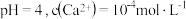 。
。
下列说法不正确的是
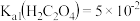 、
、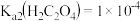 、
、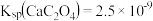 。 通过下列实验探究某些草酸盐的性质。
。 通过下列实验探究某些草酸盐的性质。实验
 :用
:用 计测得
计测得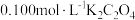 溶液的
溶液的
实验
 :向
:向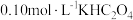 溶液中滴入少量酸性高锰酸钾溶液,振荡后溶液紫色褪去。
溶液中滴入少量酸性高锰酸钾溶液,振荡后溶液紫色褪去。实验
 :向
:向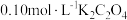 溶液中滴加一定浓度的稀盐酸后,混合溶液的
溶液中滴加一定浓度的稀盐酸后,混合溶液的
实验
 :向
:向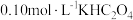 溶液加入一定体积的等浓度
溶液加入一定体积的等浓度 溶液产生白色沉淀,测得上层清液
溶液产生白色沉淀,测得上层清液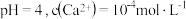 。
。下列说法不正确的是
A.实验 溶液中: 溶液中: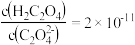 |
B.实验 说明 说明 溶液具有还原性 溶液具有还原性 |
C.实验 所得上层清液中的 所得上层清液中的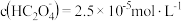 |
D.实验 反应所得溶液中存在: 反应所得溶液中存在: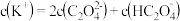 |
您最近一年使用:0次
名校
解题方法
10 . 根据下列实验操作与现象所得出的结论正确的是
| 选项 | 实验操作与现象 | 结论 |
| A | 室温下,用 计测量等浓度的 计测量等浓度的 和 和 溶液的 溶液的 ,前者大于后者 ,前者大于后者 | 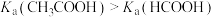 |
| B | 室温下,向浓度均为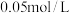 的 的 和 和 的混合溶液中滴加少量 的混合溶液中滴加少量 溶液,有黄色沉淀生成 溶液,有黄色沉淀生成 | 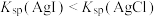 |
| C | 向无水乙醇中加入浓硫酸,加热,将产生的气体通入酸性 溶液,紫红色褪去 溶液,紫红色褪去 | 该气体一定是乙烯 |
| D | 向蔗糖溶液中加入稀硫酸,加热。待溶液冷却后向其中加入少量新制的 ,加热,未产生砖红色沉淀 ,加热,未产生砖红色沉淀 | 蔗糖没有发生水解 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次




