解题方法
1 . 常温下,将 溶液滴加到某二元弱酸
溶液滴加到某二元弱酸 溶液中,混合溶液的pH与离子浓度变化的关系如图所示。下列说法正确的是
溶液中,混合溶液的pH与离子浓度变化的关系如图所示。下列说法正确的是

 溶液滴加到某二元弱酸
溶液滴加到某二元弱酸 溶液中,混合溶液的pH与离子浓度变化的关系如图所示。下列说法正确的是
溶液中,混合溶液的pH与离子浓度变化的关系如图所示。下列说法正确的是
A.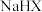 溶液中 溶液中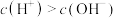 |
B.当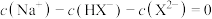 时, 时, |
C.水的电离程度: 上的点大于 上的点大于 上的点 上的点 |
D.a点溶液中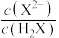 的数量级为 的数量级为 |
您最近一年使用:0次
名校
2 . 25℃时,用 溶液分别滴定一元酸
溶液分别滴定一元酸 溶液和
溶液和 溶液,pM[p表示负对数,M表示
溶液,pM[p表示负对数,M表示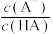 ,
, ]与溶液
]与溶液 的变化关系如图所示。已知:①
的变化关系如图所示。已知:① 易溶于水,②平衡常数
易溶于水,②平衡常数 时反应进行完全。下列说法错误的是
时反应进行完全。下列说法错误的是
 溶液分别滴定一元酸
溶液分别滴定一元酸 溶液和
溶液和 溶液,pM[p表示负对数,M表示
溶液,pM[p表示负对数,M表示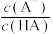 ,
, ]与溶液
]与溶液 的变化关系如图所示。已知:①
的变化关系如图所示。已知:① 易溶于水,②平衡常数
易溶于水,②平衡常数 时反应进行完全。下列说法错误的是
时反应进行完全。下列说法错误的是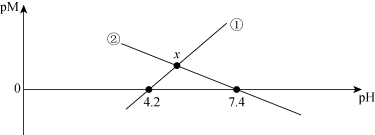
A.该温度下, 的 的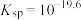 |
B.滴定 溶液至x点时,改为滴加HA溶液,沉淀逐渐完全溶解 溶液至x点时,改为滴加HA溶液,沉淀逐渐完全溶解 |
C.25℃,NaA溶液中, 水解常数的数量级为 水解常数的数量级为 |
D.滴定HA溶液至x点时,溶液中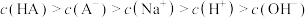 |
您最近一年使用:0次
2024-03-14更新
|
518次组卷
|
3卷引用:四川省成都市石室中学2023-2024学年高二下学期4月月考化学试卷
3 . 已知:连二次硝酸( )是二元酸,可用于制取
)是二元酸,可用于制取 气体。在常温下,用
气体。在常温下,用 溶液滴定
溶液滴定 溶液,测得溶液的
溶液,测得溶液的 与
与 溶液体积的关系如图所示。
溶液体积的关系如图所示。

回答下列问题。
(1)滴定过程中盛装标准 溶液应选用
溶液应选用________ (填字母)仪器。

(2)常温下, 的
的
________ 。
(3)已知常温下 ,
, 与
与 溶液
溶液________ (填“能”或“不能”)反应。
(4)滴定过程中,由水电离出的 大小关系:
大小关系:
________ (填“>”“<”或“=”) 。
。
(5) 点溶液中
点溶液中
________ (填“>”“<”或“=”) 。
。
(6) 点溶液中含氮粒子浓度由大到小的顺序是
点溶液中含氮粒子浓度由大到小的顺序是________ 。
(7) 点溶液和
点溶液和 溶液混合,可得黄色的
溶液混合,可得黄色的 沉淀,再向该体系中滴加
沉淀,再向该体系中滴加 溶液,此时白色和黄色沉淀共存,该体系中
溶液,此时白色和黄色沉淀共存,该体系中
________ 。[已知 ,
, ]
]
 )是二元酸,可用于制取
)是二元酸,可用于制取 气体。在常温下,用
气体。在常温下,用 溶液滴定
溶液滴定 溶液,测得溶液的
溶液,测得溶液的 与
与 溶液体积的关系如图所示。
溶液体积的关系如图所示。
回答下列问题。
(1)滴定过程中盛装标准
 溶液应选用
溶液应选用
(2)常温下,
 的
的
(3)已知常温下
 ,
, 与
与 溶液
溶液(4)滴定过程中,由水电离出的
 大小关系:
大小关系:
 。
。(5)
 点溶液中
点溶液中
 。
。(6)
 点溶液中含氮粒子浓度由大到小的顺序是
点溶液中含氮粒子浓度由大到小的顺序是(7)
 点溶液和
点溶液和 溶液混合,可得黄色的
溶液混合,可得黄色的 沉淀,再向该体系中滴加
沉淀,再向该体系中滴加 溶液,此时白色和黄色沉淀共存,该体系中
溶液,此时白色和黄色沉淀共存,该体系中
 ,
, ]
]
您最近一年使用:0次
名校
4 . 下列方案设计、现象和结论都正确的是
| 实验方案 | 现象 | 结论 | |
 | 向 的 的 溶液中加入等体积浓 溶液中加入等体积浓 溶液,振荡 溶液,振荡 | 分层,下层由紫红色变为浅粉红色,上层呈棕黄色 |  在浓 在浓 溶液中的溶解能力大于在 溶液中的溶解能力大于在 的溶解能力 的溶解能力 |
 | 向 溶液中滴加 溶液中滴加 溶液,再加入少量 溶液,再加入少量 固体 固体 | 溶液先变成血红色后无明显变化 |  与 与 反应不可逆 反应不可逆 |
| C | 向 溶液中先滴加4滴 溶液中先滴加4滴 溶液,再滴加4滴 溶液,再滴加4滴 溶液 溶液 | 先产生白色沉淀,再产生黄色沉淀 |  转化为 转化为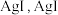 溶解度小于 溶解度小于 溶解度 溶解度 |
 | 向 溶液中滴加 溶液中滴加 溶液 溶液 | 出现黄色沉淀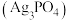 |  发生了水解反应 发生了水解反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
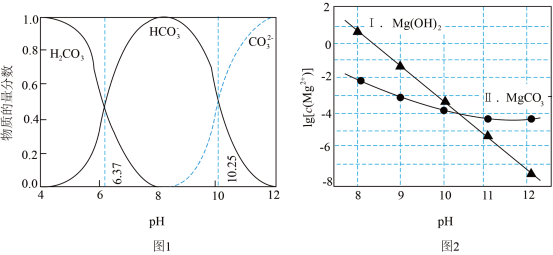
5 . 常温下, 在Na2CO3溶液中发生反应,可能生成
在Na2CO3溶液中发生反应,可能生成 或MgCO3。图1表示Na2CO3溶液中各含碳物种的物质的量分数与溶液pH的关系;图2中曲线Ⅰ的离子浓度关系符合
或MgCO3。图1表示Na2CO3溶液中各含碳物种的物质的量分数与溶液pH的关系;图2中曲线Ⅰ的离子浓度关系符合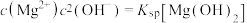 ;曲线Ⅱ的离子浓度关系符合
;曲线Ⅱ的离子浓度关系符合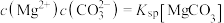 。利用平衡原理分析,下列说法正确的是
。利用平衡原理分析,下列说法正确的是
 在Na2CO3溶液中发生反应,可能生成
在Na2CO3溶液中发生反应,可能生成 或MgCO3。图1表示Na2CO3溶液中各含碳物种的物质的量分数与溶液pH的关系;图2中曲线Ⅰ的离子浓度关系符合
或MgCO3。图1表示Na2CO3溶液中各含碳物种的物质的量分数与溶液pH的关系;图2中曲线Ⅰ的离子浓度关系符合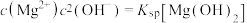 ;曲线Ⅱ的离子浓度关系符合
;曲线Ⅱ的离子浓度关系符合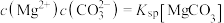 。利用平衡原理分析,下列说法正确的是
。利用平衡原理分析,下列说法正确的是
A.常温时, 的水解常数 的水解常数 |
B.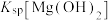 的数量级为 的数量级为 |
C.由图2,当pH=11, 时,有沉淀生成 时,有沉淀生成 |
D.由图1和图2,在pH=8,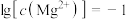 时,溶液中发生反应: 时,溶液中发生反应: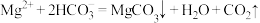 |
您最近一年使用:0次
名校
6 .  排放到空气中会引起酸雨等环境问题,严重危害人类健康,
排放到空气中会引起酸雨等环境问题,严重危害人类健康, 水溶液中存在下列平衡:
水溶液中存在下列平衡:
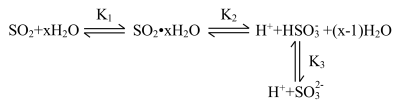
已知: ,
, ,
, 为各步反应的平衡常数,且
为各步反应的平衡常数,且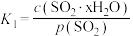 [
[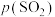 表示
表示 的平衡压强]。下列说法正确的是
的平衡压强]。下列说法正确的是
 排放到空气中会引起酸雨等环境问题,严重危害人类健康,
排放到空气中会引起酸雨等环境问题,严重危害人类健康, 水溶液中存在下列平衡:
水溶液中存在下列平衡: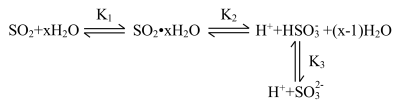
已知:
 ,
, ,
, 为各步反应的平衡常数,且
为各步反应的平衡常数,且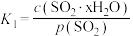 [
[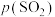 表示
表示 的平衡压强]。下列说法正确的是
的平衡压强]。下列说法正确的是A.由上图平衡可知 溶液和 溶液和 溶液都可以水解,溶液一定呈碱性 溶液都可以水解,溶液一定呈碱性 |
B.氨水也可吸收 ,防止大气污染,同时通入 ,防止大气污染,同时通入 能进一步提高 能进一步提高 去除率 去除率 |
C.当 的平衡压强为p时,测得 的平衡压强为p时,测得 ,则溶液 ,则溶液 |
D.用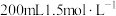 的氢氧化钠溶液吸收0.2mol的 的氢氧化钠溶液吸收0.2mol的 ,则溶液中存在关系式: ,则溶液中存在关系式: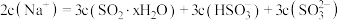 |
您最近一年使用:0次
7 . 常温下,将0.1mol·L-1NaOH溶液滴加到一定浓度的二元酸(H2R)溶液中,混合溶液的pH与离子浓度变化的关系如图所示。下列叙述正确的是
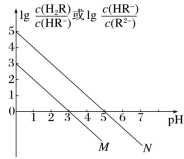

A.线N表示pH与lg 的变化关系 的变化关系 |
| B.当溶液中c(HR-)=c(R2-)时,pH=3 |
| C.NaHR溶液中c(H+)>c(OH-) |
| D.当混合溶液呈中性时,c(Na+)<c(H2R)+c(HR-)+c(R2-) |
您最近一年使用:0次
2024-03-10更新
|
105次组卷
|
2卷引用:云南省玉溪市第二中学2022-2023学年高二下学期期末考试化学试题
名校
解题方法
8 . 将磷肥生产形成的副产物石膏( )转化为硫酸钾肥料和氯化钙水合物储热材料,无论从经济效益、资源综合利用还是从环境保护角度看都具有重要意义。石膏转化为硫酸钾和氯化钙的工艺流程示意图如图所示
)转化为硫酸钾肥料和氯化钙水合物储热材料,无论从经济效益、资源综合利用还是从环境保护角度看都具有重要意义。石膏转化为硫酸钾和氯化钙的工艺流程示意图如图所示
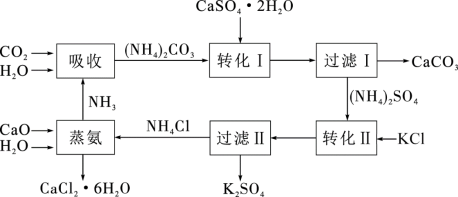
请回答下列问题:
(1)本工艺中所用的原料除 、CaCO3、H2O外,还需要的两种原料是
、CaCO3、H2O外,还需要的两种原料是______ 、______ (填化学式,不考虑损耗)。
(2)室温下, 溶液的pH
溶液的pH______ 7(填“>”、“<”或“=”),该溶液中所有微粒(水分子除外)的物质的量浓度由小到大的顺序为______ 。
(3)转化Ⅰ是将难溶的CaSO4(s)转化为更难溶的CaCO3(s),将一定量的 加入过量的CaSO4悬浊液中,充分反应后,测得溶液中
加入过量的CaSO4悬浊液中,充分反应后,测得溶液中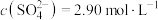 ,此时溶液中的
,此时溶液中的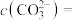
______  。[已知:
。[已知: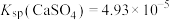 、
、 ]
]
(4)已知不同温度下K2SO4在100 g水中达到饱和时溶解的量如下表:
75℃的K2SO4饱和溶液482 g冷却到20℃,可析出K2SO4晶体______ g。
(5)写出“蒸氨”过程中的化学方程式:____________________ 。
 )转化为硫酸钾肥料和氯化钙水合物储热材料,无论从经济效益、资源综合利用还是从环境保护角度看都具有重要意义。石膏转化为硫酸钾和氯化钙的工艺流程示意图如图所示
)转化为硫酸钾肥料和氯化钙水合物储热材料,无论从经济效益、资源综合利用还是从环境保护角度看都具有重要意义。石膏转化为硫酸钾和氯化钙的工艺流程示意图如图所示
请回答下列问题:
(1)本工艺中所用的原料除
 、CaCO3、H2O外,还需要的两种原料是
、CaCO3、H2O外,还需要的两种原料是(2)室温下,
 溶液的pH
溶液的pH(3)转化Ⅰ是将难溶的CaSO4(s)转化为更难溶的CaCO3(s),将一定量的
 加入过量的CaSO4悬浊液中,充分反应后,测得溶液中
加入过量的CaSO4悬浊液中,充分反应后,测得溶液中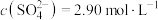 ,此时溶液中的
,此时溶液中的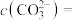
 。[已知:
。[已知: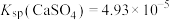 、
、 ]
](4)已知不同温度下K2SO4在100 g水中达到饱和时溶解的量如下表:
温度/℃ | 0 | 20 | 40 | 60 | 75 |
K2SO4溶解的量/g | 7.7 | 11.1 | 14.7 | 18.1 | 20.5 |
(5)写出“蒸氨”过程中的化学方程式:
您最近一年使用:0次
9 . 已知25℃时二元酸 的
的 .下列说法正确的是
.下列说法正确的是
 的
的 .下列说法正确的是
.下列说法正确的是A.在等浓度的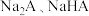 溶液中,水的电离程度前者小于后者 溶液中,水的电离程度前者小于后者 |
B.取 的 的 溶液 溶液 ,加蒸馏水稀释至 ,加蒸馏水稀释至 ,则该溶液 ,则该溶液 |
C.向 溶液中加入 溶液中加入 溶液至 溶液至 ,则 ,则 |
D.向 的 的 溶液中通入HCl气体(忽略溶液体积的变化)至 溶液中通入HCl气体(忽略溶液体积的变化)至 ,则 ,则 的电离度为0.013% 的电离度为0.013% |
您最近一年使用:0次
解题方法
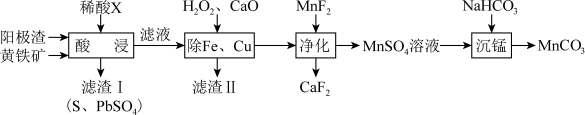
10 . 电解制锰的阳极渣主要成分是 ,还含有少量PbO、CuO及铁的氧化物,以阳极渣和黄铁矿
,还含有少量PbO、CuO及铁的氧化物,以阳极渣和黄铁矿 为原料可制备
为原料可制备 ,其流程如图所示:
,其流程如图所示:
已知常温下,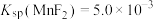 ,
, 。
。
(1)加快“酸浸”速率的措施有___________ (填两条)。稀酸X为___________ (填名称)。“酸浸”时 中的铁元素转化为
中的铁元素转化为 ,则该反应中氧化剂与还原剂的物质的量之比为
,则该反应中氧化剂与还原剂的物质的量之比为___________ 。
(2)滤渣Ⅱ的主要成分为 、
、 、
、___________ (填化学式)。
(3)加入 时发生反应的离子方程式为
时发生反应的离子方程式为___________ 。如果“净化”所得溶液中 的浓度为
的浓度为 ,则溶液中
,则溶液中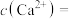
___________  。
。
(4) 溶液中的元素守恒式为
溶液中的元素守恒式为___________ 。加入 溶液进行“沉锰”,写出该反应的离子方程式:
溶液进行“沉锰”,写出该反应的离子方程式:___________ 。
 ,还含有少量PbO、CuO及铁的氧化物,以阳极渣和黄铁矿
,还含有少量PbO、CuO及铁的氧化物,以阳极渣和黄铁矿 为原料可制备
为原料可制备 ,其流程如图所示:
,其流程如图所示:
已知常温下,
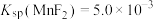 ,
, 。
。(1)加快“酸浸”速率的措施有
 中的铁元素转化为
中的铁元素转化为 ,则该反应中氧化剂与还原剂的物质的量之比为
,则该反应中氧化剂与还原剂的物质的量之比为(2)滤渣Ⅱ的主要成分为
 、
、 、
、(3)加入
 时发生反应的离子方程式为
时发生反应的离子方程式为 的浓度为
的浓度为 ,则溶液中
,则溶液中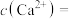
 。
。(4)
 溶液中的元素守恒式为
溶液中的元素守恒式为 溶液进行“沉锰”,写出该反应的离子方程式:
溶液进行“沉锰”,写出该反应的离子方程式:
您最近一年使用:0次



