解题方法
1 . 已知常温下部分弱电解质的电离常数如表:
回答下列问题:
(1)常温下,物质的量浓度相同的三种溶液:① ②HClO③
②HClO③ ,其pH由大到小的顺序是
,其pH由大到小的顺序是_______ (填序号)。
(2)25℃时, 的NaClO溶液中各离子浓度由大到小的顺序为
的NaClO溶液中各离子浓度由大到小的顺序为_______ 。
(3) 溶液中的电荷守恒关系式为
溶液中的电荷守恒关系式为_______ (用离子浓度表示) 。
(4)热的 溶液可以洗涤油污的原因是
溶液可以洗涤油污的原因是_______ °
(5)25℃时,若测得某 和
和 混合溶液的
混合溶液的 ,则溶液中:
,则溶液中: 为
为_______ 。
(6)25℃时,若测得某 和
和 混合溶液的
混合溶液的 ,则溶液中:
,则溶液中: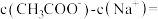
_______ mol/L(列出计算式即可,不需要计算准确值)。
| 弱电解质 | HClO |  |  |  |
| 电离常数 | 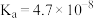 | 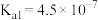 、 、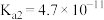 | 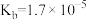 | 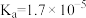 |
(1)常温下,物质的量浓度相同的三种溶液:①
 ②HClO③
②HClO③ ,其pH由大到小的顺序是
,其pH由大到小的顺序是(2)25℃时,
 的NaClO溶液中各离子浓度由大到小的顺序为
的NaClO溶液中各离子浓度由大到小的顺序为(3)
 溶液中的电荷守恒关系式为
溶液中的电荷守恒关系式为(4)热的
 溶液可以洗涤油污的原因是
溶液可以洗涤油污的原因是(5)25℃时,若测得某
 和
和 混合溶液的
混合溶液的 ,则溶液中:
,则溶液中: 为
为(6)25℃时,若测得某
 和
和 混合溶液的
混合溶液的 ,则溶液中:
,则溶液中: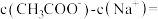
您最近一年使用:0次
名校
解题方法
2 . 已知水在25 ℃和100 ℃时,其电离平衡曲线如图所示。

(1) 25 ℃时,将10 mL pH=a的盐酸与100 mL pH=b的Ba(OH)2溶液混合后恰好中和,则a+b=______ 。
(2) 100℃时,将0.02 mol·L-1的Ba(OH)2溶液与等物质的量浓度的NaHSO4溶液等体积混合(假设溶液的体积变化忽略不计),所得混合液的pH=______ 。
(3) 25 ℃时Ksp(AgCl)=1.8×10-10,若向50 mL 0.018 mol·L-1的AgNO3溶液中加入50 mL 0.020 mol·L-1的盐酸(假设溶液的体积变化忽略不计),混合后溶液中Ag+的浓度为______ mol·L-1,pH为______ 。
(4) 25 ℃时Ksp[Al(OH)3]=1×10-33,Ksp[Fe(OH)3]=1×10-39,pH=7.1时Mn(OH)2开始沉淀。室温下欲除去MnSO4溶液中的Fe3+、Al3+(使其浓度均小于1×10-6 mol·L-1),需调节溶液的pH范围为______ 。
(5) 磷酸是三元弱酸,常温下三级电离常数分别是Ka1=7.1×10-3,Ka2=6.2×10-8,Ka3=4.5×10-13,回答下列问题:
①常温下,NaH2PO4的水溶液pH______ (填“>”“<”或“=”)7。
②常温下,Na2HPO4的水溶液呈______ (填“酸”“碱”或“中”)性,结合Ka与Kh的相对大小,给出判断理由:______ 。

(1) 25 ℃时,将10 mL pH=a的盐酸与100 mL pH=b的Ba(OH)2溶液混合后恰好中和,则a+b=
(2) 100℃时,将0.02 mol·L-1的Ba(OH)2溶液与等物质的量浓度的NaHSO4溶液等体积混合(假设溶液的体积变化忽略不计),所得混合液的pH=
(3) 25 ℃时Ksp(AgCl)=1.8×10-10,若向50 mL 0.018 mol·L-1的AgNO3溶液中加入50 mL 0.020 mol·L-1的盐酸(假设溶液的体积变化忽略不计),混合后溶液中Ag+的浓度为
(4) 25 ℃时Ksp[Al(OH)3]=1×10-33,Ksp[Fe(OH)3]=1×10-39,pH=7.1时Mn(OH)2开始沉淀。室温下欲除去MnSO4溶液中的Fe3+、Al3+(使其浓度均小于1×10-6 mol·L-1),需调节溶液的pH范围为
(5) 磷酸是三元弱酸,常温下三级电离常数分别是Ka1=7.1×10-3,Ka2=6.2×10-8,Ka3=4.5×10-13,回答下列问题:
①常温下,NaH2PO4的水溶液pH
②常温下,Na2HPO4的水溶液呈
您最近一年使用:0次



