1 . 酸碱盐等电解质溶液中存在的电离平衡、水解平衡和沉淀溶解平衡都与生命活动、日常生活、工农业生产和环境保护等息息相关。请回答下列问题:
(1) 水溶液显
水溶液显_______ 性(填“酸”、“碱”或“中”),原因是_______ (用离子方程式表示)。
(2)用离子方程式表示泡沫灭火器的工作原理_______ 。
(3)物质的量浓度相同的下列溶液:① ②
② ③
③ ④
④ ,其中
,其中 由大到小的顺序是
由大到小的顺序是_______ (填序号)。
(4)25℃时, 的盐酸和
的盐酸和 的NaOH溶液混合后溶液
的NaOH溶液混合后溶液 (忽略溶液混合时体积的变化),则
(忽略溶液混合时体积的变化),则
_______ 。
(5)25℃时,某溶液中 白的浓度为
白的浓度为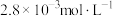 ,使
,使 开始沉淀的
开始沉淀的
_______ 。(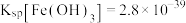 )
)
(6)25℃时,将: 溶液与
溶液与 溶液等体积混合,反应后的溶液中
溶液等体积混合,反应后的溶液中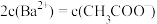 ,用含a和b的代数式表示醋酸的电离常数
,用含a和b的代数式表示醋酸的电离常数
_______ 。
(1)
 水溶液显
水溶液显(2)用离子方程式表示泡沫灭火器的工作原理
(3)物质的量浓度相同的下列溶液:①
 ②
② ③
③ ④
④ ,其中
,其中 由大到小的顺序是
由大到小的顺序是(4)25℃时,
 的盐酸和
的盐酸和 的NaOH溶液混合后溶液
的NaOH溶液混合后溶液 (忽略溶液混合时体积的变化),则
(忽略溶液混合时体积的变化),则
(5)25℃时,某溶液中
 白的浓度为
白的浓度为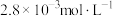 ,使
,使 开始沉淀的
开始沉淀的
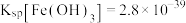 )
)(6)25℃时,将:
 溶液与
溶液与 溶液等体积混合,反应后的溶液中
溶液等体积混合,反应后的溶液中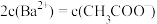 ,用含a和b的代数式表示醋酸的电离常数
,用含a和b的代数式表示醋酸的电离常数
您最近一年使用:0次
2 . 研究电解质在水溶液中的平衡能了解它的存在形式。常温下,向 的溶液中逐滴加入
的溶液中逐滴加入 溶液,所得溶液的
溶液,所得溶液的 随
随 溶液的体积变化如图所示(溶液体积变化忽略不计)。
溶液的体积变化如图所示(溶液体积变化忽略不计)。

(1)温下, 溶液中由水电离出的
溶液中由水电离出的
_______  。
。
(2)X点时,溶液中各离子浓度由大到小的顺序是_______ 。
(3)K点时,溶液中
_______  。
。
 的溶液中逐滴加入
的溶液中逐滴加入 溶液,所得溶液的
溶液,所得溶液的 随
随 溶液的体积变化如图所示(溶液体积变化忽略不计)。
溶液的体积变化如图所示(溶液体积变化忽略不计)。
(1)温下,
 溶液中由水电离出的
溶液中由水电离出的
 。
。(2)X点时,溶液中各离子浓度由大到小的顺序是
(3)K点时,溶液中

 。
。
您最近一年使用:0次
解题方法
3 . (1)某温度(t ℃)时,水的Kw=10-13,将此温度下pH=11的NaOH溶液a L与pH=1的硫酸溶液b L混合,若所得混合液的 pH=2,则a∶b=________
(2)已知25 ℃时,0.1 mol/L醋酸达到平衡时的pH约为3,如果在此溶液中加入等体积的pH=5的盐酸,则电离平衡_______ (填“向左”“向右”或“不”)移动;此温度下的电离平衡常数约为_______________
(3)室温下,测得CH3COONH4溶液的pH=7,则说明CH3COO-的水解程度_______ (填“>”“<”或“=”,下同) NH 的水解程度,CH3COO-与NH
的水解程度,CH3COO-与NH 浓度的大小关系是:c(CH3COO-)
浓度的大小关系是:c(CH3COO-)______ c(NH )
)
(2)已知25 ℃时,0.1 mol/L醋酸达到平衡时的pH约为3,如果在此溶液中加入等体积的pH=5的盐酸,则电离平衡
(3)室温下,测得CH3COONH4溶液的pH=7,则说明CH3COO-的水解程度
 的水解程度,CH3COO-与NH
的水解程度,CH3COO-与NH 浓度的大小关系是:c(CH3COO-)
浓度的大小关系是:c(CH3COO-) )
)
您最近一年使用:0次
解题方法
4 . 按要求填空:
(1)Cr(OH)3在溶液中存在以下沉淀溶解平衡:Cr(OH)3(s)⇌Cr3+(aq)+3OH-(aq)。常温下,Cr(OH)3溶度积Ksp=1.0×10-32,要使c(Cr3+)完全沉淀,溶液的pH应调至______ 。
(2)25℃时,向水的电离平衡体系中加入少量碳酸钠固体,得到pH为11的溶液,其水解方程式为_________ ,由水电离出的c(OH-)=________ mol·L-1。
(3)在100℃下,将pH=3的硫酸溶液和pH=10的NaOH溶液混合,若要使混合后溶液的pH=7,则硫酸溶液和NaOH溶液的体积比约为_____ 。
(1)Cr(OH)3在溶液中存在以下沉淀溶解平衡:Cr(OH)3(s)⇌Cr3+(aq)+3OH-(aq)。常温下,Cr(OH)3溶度积Ksp=1.0×10-32,要使c(Cr3+)完全沉淀,溶液的pH应调至
(2)25℃时,向水的电离平衡体系中加入少量碳酸钠固体,得到pH为11的溶液,其水解方程式为
(3)在100℃下,将pH=3的硫酸溶液和pH=10的NaOH溶液混合,若要使混合后溶液的pH=7,则硫酸溶液和NaOH溶液的体积比约为
您最近一年使用:0次
5 . (1)在25°C时,纯水中C(H+)·C(OH-)=_________________ ;
(2)在NH4Cl溶液中C(H+)______ 10-7mol/L(大于、小于或等于),pH______ 7(大于、小于或等于);
(3)在Na2CO3溶液中C(H+)______ 10-7mol/L (大于、小于或等于),pH______ 7(大于、小于或等于)
(4)在NaCl溶液中C(H+)______ 10-7mol/L (大于、小于或等于),pH______ 7(大于、小于或等于).
(2)在NH4Cl溶液中C(H+)
(3)在Na2CO3溶液中C(H+)
(4)在NaCl溶液中C(H+)
您最近一年使用:0次
2016-12-09更新
|
169次组卷
|
3卷引用:黑龙江省鸡西市密山市第四中学2021-2022学年高二上学期期末考试化学试题
黑龙江省鸡西市密山市第四中学2021-2022学年高二上学期期末考试化学试题2014-2015四川省雅安中学高二上学期期末模拟化学试卷(已下线)第三章 检测-2020-2021学年上学期高二化学同步精品课堂(新教材人教版选择性必修1)
11-12高二上·黑龙江双鸭山·期中
6 . (1)25 ℃时,将pH=11的NaOH溶液与pH=4的硫酸溶液混合,若所得混合溶液pH=9,则NaOH溶液与硫酸溶液的体积比为
已知25 ℃时,0.1 L 0.1 mol·L-1的NaA溶液的pH=10,溶液中各离子的物质的量浓度由大到小的顺序为 。
(2))若100 ℃时,KW=10-12,则100 ℃时pH=11的Ba(OH)2溶液与pH=2的硫酸按体积比1:9混合充分反应后pH= ;若该温度下10体积的pH=a的某强酸溶液与1体积pH=b的某强碱溶液混合后溶液呈中性,则混合之前,a与b之间应满足的关系为 。
(3)某温度下的水溶液中,c(H+)=10x mol/L,c(OH-)=10y mol/L。x与y的关系如图所示。

该温度下水的离子积为 。该温度下氯化钠溶液的pH为
该温度下0.01 mol/L NaOH溶液的pH为 。
已知25 ℃时,0.1 L 0.1 mol·L-1的NaA溶液的pH=10,溶液中各离子的物质的量浓度由大到小的顺序为 。
(2))若100 ℃时,KW=10-12,则100 ℃时pH=11的Ba(OH)2溶液与pH=2的硫酸按体积比1:9混合充分反应后pH= ;若该温度下10体积的pH=a的某强酸溶液与1体积pH=b的某强碱溶液混合后溶液呈中性,则混合之前,a与b之间应满足的关系为 。
(3)某温度下的水溶液中,c(H+)=10x mol/L,c(OH-)=10y mol/L。x与y的关系如图所示。

该温度下水的离子积为 。该温度下氯化钠溶液的pH为
该温度下0.01 mol/L NaOH溶液的pH为 。
您最近一年使用:0次



