1 . 判断下列选项正确的是
| A.NaHCO3属于碱式盐,其水溶液显碱性 |
| B.NaHSO3属于酸式盐,其水溶液显酸性 |
C.NaHSO4属于正盐,水溶液显酸性的原因是HSO 的电离程度大于HSO 的电离程度大于HSO 的水解程度 的水解程度 |
D.NaHC2O4水溶液显酸性的原因是H2C2O4 的电离程度大于HC2O 的水解程度 的水解程度 |
您最近一年使用:0次
2022-08-25更新
|
77次组卷
|
2卷引用:宁夏石嘴山第三中学2021-2022学年高二下学期期末考试化学试题
名校
解题方法
2 . 下列方案设计、现象和结论都正确的是
| 实验目的 | 方案设计 | 现象和结论 | |
| A | 探究NO2生成N2O4反应的吸放热 | 将充有NO2的密闭烧瓶放入热水中 | 烧瓶内气体颜色变浅,NO2生成N2O4的反应为吸热反应 |
| B | 比较CH3COOH和HF的酸性强弱 | 相同条件下,分别用pH试纸测定0.lmol·L-1CH3COONa溶液、1.0mol·L-1NaF溶液的pH | NaF溶液的pH>CH3COONa溶液的pH,证明CH3COOH的酸性比HF的酸性强 |
| C | 比较氢氧化铜和氢氧化镁Ksp的大小 | 向浓度均为0.1mol·L-1的MgCl2、CuCl2混合溶液中逐滴加入NaOH溶液 | 先出现蓝色沉淀,Ksp[Mg(OH)2]>Ksp[Cu(OH)2] |
| D | 镀锌铁皮锌镀层厚度的测定 | 装有镀锌铁皮的烧杯中加入足量稀硫酸 | 产生气泡的速率突然减小,证明镀锌层完全反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-04-09更新
|
2677次组卷
|
10卷引用:宁夏石嘴山市光明中学2024届高三第一次模拟考试理综化学试题
宁夏石嘴山市光明中学2024届高三第一次模拟考试理综化学试题重庆市2022届高三模拟调研卷(三)化学试题(已下线)化学-2022年高考押题预测卷01(辽宁卷)(已下线)押江苏卷第11题 化学实验综合选择题 -备战2022年高考化学临考题号押题(江苏卷)(已下线)2022年全国甲卷高考真题变式题(选择题)(已下线)2022年全国乙卷高考变式题(选择题)(已下线)2022年浙江1月高考真题变式题(21-25)湖南省株洲市第四中学2023届高三第六次月考化学试题江苏省泰州中学2023-2024学年高三上学期期初调研考试化学试题(已下线)FHgkyldyjhx09
名校
3 . 为探究温度对盐类水解的影响,利用手持技术测定0.1mol•L-1Na2CO3溶液温度由20℃升高到60℃过程的pH,130s后的曲线如图所示(已知pKw=pH+pOH)。下列说法正确的是


| A.加热升温时,溶液中的c(OH-)降低 |
B.加热过程中,n(H2CO3)+n(HCO )+n(CO )+n(CO )逐渐增大 )逐渐增大 |
C.常温下,Kh1(CO )为10-4.6 )为10-4.6 |
D.Kw受温度的影响程度大于Kh1(CO ) ) |
您最近一年使用:0次
2022-01-15更新
|
443次组卷
|
4卷引用:宁夏回族自治区银川一中2022-2023学年高二上学期期中考试化学试题
宁夏回族自治区银川一中2022-2023学年高二上学期期中考试化学试题福建省泉州市2021-2022学年高三上学期1月普通高中毕业班质量监测(二)化学试题(已下线)考点28 盐类的水解-备战2023年高考化学一轮复习考点帮(全国通用)云南省腾冲市第八中学2022-2023学年高二下学期第三次月考化学试题
名校
4 . 下列实验操作、实验现象及解释或结论都正确且有因果关系的是
| 选项 | 实验操作 | 实验现象 | 解释或结论 |
| A |  在平衡体系中加入KCl晶体 在平衡体系中加入KCl晶体 | 溶液颜色变浅 | 加入生成物该化学平衡向逆反应方向移动 |
| B | 常温下,用pH计测定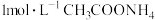 溶液 溶液 | 测得pH=7 |  溶液对水的电离程度无影响 溶液对水的电离程度无影响 |
| C | 将硫酸铝溶液加入到天然淡水中,搅拌,静置 | 水变澄清,絮状沉淀下沉到底部 |  的水解与天然水中 的水解与天然水中 的水解互相促进,生成 的水解互相促进,生成 胶体 胶体 |
| D | 用pH试纸测得相同浓度的pH NaClO溶液、 溶液的pH 溶液的pH | NaClO溶液的pH约为9, 溶液的pH约为8 溶液的pH约为8 |  的酸性比HClO强 的酸性比HClO强 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-11-18更新
|
268次组卷
|
6卷引用:宁夏青铜峡市高级中学2021-2022学年高二下学期开学考试化学试题
名校
5 . 化学与人类生产、生活密切相关。下列描述中不涉及盐类水解原理的是
| A.明矾净水 | B.氯化铵溶液除铁锈 |
| C.用食盐腌制肉制品 | D.用草木灰去除油污 |
您最近一年使用:0次
2021-08-06更新
|
452次组卷
|
6卷引用:宁夏永宁县永宁中学2021-2022学年高二上学期期末考试化学试题
宁夏永宁县永宁中学2021-2022学年高二上学期期末考试化学试题重庆市南开中学2020-2021学年二上学期期末考试化学试题(已下线)3.3.3 盐类水解的应用-2021-2022学年高二化学课后培优练(人教版选修4)陕西省西安中学2021-2022学年高二上学期期末考试化学试题河北省保定市徐水综合高级中学2021-2022学年高二上学期第二次月考化学试题重庆市第七中学校2021-2022学年高二上学期第二次月考化学试题
名校
6 . 设NA为阿伏加德罗常数的值。下列说法正确的是
| A.标准状况下,0.1molCl2溶于水,转移的电子数目为0.1NA |
| B.1.8gH2O所含分子数为6.02×1023 |
C.100mL 1.0mol/L的碳酸钠溶液中,CO 数目为0.1×6.02×1023 数目为0.1×6.02×1023 |
| D.1mol OH-中含有10NA个电子 |
您最近一年使用:0次
7 . 根据下列实验操作和现象所得出的结论正确的是
| 选项 | 实验操作和现象 | 结 论 |
| A | 向20mL0.2mol·L-1硝酸银溶液中滴加5滴0.2mol·L-1氯化钠溶液出现白色沉淀,再在浊液中滴加几滴0.2mol·L-1碘化钾溶液出现黄色沉淀 | 不能证明碘化银比氯化银难溶 |
| B | 常温下,测得0.1mol/LNaA溶液的pH小于0.1mol/LNa2CO3溶液的pH | 酸性:HA>H2CO3 |
| C | 将铝与氧化铁发生铝热反应后的熔融物在稀盐酸中充分溶解,再滴加几滴KSCN溶液,溶液未变红 | 熔融物中不含有正三价铁 |
| D | 向2支均盛有2mL1.0mol·L-1KOH溶液的试管中分别加入2滴浓度均为0.1mol·L-1的AlCl3和MgCl2溶液,一支试管出现白色沉淀,另一支无明显现象 | Ksp[Al(OH)3]>Ksp[Mg(OH)2] |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-01-20更新
|
105次组卷
|
2卷引用:宁夏银川市景博中学2021-2022学年高二上学期第二次月考化学试题
20-21高二上·全国·假期作业
8 . pH=4的醋酸和pH=4的氯化铵溶液相比,水的电离程度较大的是( )
| A.前者 | B.后者 |
| C.等于 | D.无法确定 |
您最近一年使用:0次
名校
9 . 在室温下,下列五种溶液:
①0.1 mol·L-1 NH4Cl ②0.1 mol·L-1 CH3COONH4 ③0.1 mol·L-1 NH4HSO4
④0.1 mol·L-1 NH3·H2O和0.1 mol·L-1 NH4Cl混合液 ⑤0.1 mol·L-1 NH3·H2O
请根据要求填写下列空白:
(1)溶液①呈___________ (填“酸”“碱”或“中”)性,其原因是___________ (用离子方程式表示)。
(2)比较溶液②③中c(NH )的大小关系是②
)的大小关系是②___________ (填“>”“<”或“=”)③。
(3)在溶液④中,___________ 离子的浓度为0.1 mol·L-1;NH3·H2O和___________ 离子的浓度之和为0.2 mol·L-1。
(4)室温下,测得溶液②的pH=7,则说明CH3COO-的水解程度___________ (填“>”“<”或“=”)NH 的水解程度,CH3COO-与NH
的水解程度,CH3COO-与NH 浓度的大小关系是:c(CH3COO-)
浓度的大小关系是:c(CH3COO-)___________ (填“>”“<”或“=”)c(NH )。
)。
①0.1 mol·L-1 NH4Cl ②0.1 mol·L-1 CH3COONH4 ③0.1 mol·L-1 NH4HSO4
④0.1 mol·L-1 NH3·H2O和0.1 mol·L-1 NH4Cl混合液 ⑤0.1 mol·L-1 NH3·H2O
请根据要求填写下列空白:
(1)溶液①呈
(2)比较溶液②③中c(NH
 )的大小关系是②
)的大小关系是②(3)在溶液④中,
(4)室温下,测得溶液②的pH=7,则说明CH3COO-的水解程度
 的水解程度,CH3COO-与NH
的水解程度,CH3COO-与NH 浓度的大小关系是:c(CH3COO-)
浓度的大小关系是:c(CH3COO-) )。
)。
您最近一年使用:0次
2021-01-06更新
|
120次组卷
|
2卷引用:宁夏银川市长庆高级中学2020-2021学年高二上学期期末考试化学试题
名校
解题方法
10 . 草酸是二元弱酸,草酸氢钾溶液呈酸性。在0.1 mol∙L−1 KHC2O4溶液中,下列关系正确的是
A.c(K+)+c(H+)=c(HC2O )+c(OH-)+c(C2O )+c(OH-)+c(C2O ) ) |
B.c(HC2O )+ c(C2O )+ c(C2O )=0.1 mol∙L−1 )=0.1 mol∙L−1 |
C.c(C2O )>c(H2C2O4) )>c(H2C2O4) |
D.c(K+)= c(H2C2O4)+ c(HC2O )+2 c(C2O )+2 c(C2O ) ) |
您最近一年使用:0次
2020-12-28更新
|
786次组卷
|
12卷引用:宁夏吴忠中学2020-2021学年高二上学期期末考试化学试题
宁夏吴忠中学2020-2021学年高二上学期期末考试化学试题鲁科版(2019)选择性必修1第3章 物质在水溶液中的行为 第2节 弱电解质的电离 盐类的水解 课时4 溶液中粒子浓度的大小关系高中必刷题高二选择性必修1第三章 水溶液中的离子反应与平衡 第三节 盐类的水解 课时3 溶液中粒子浓度的大小关系人教版(2019)高二选择性必修第一册 第三章 水溶液中的离子反应与平衡 第三节 盐类的水解 教材帮内蒙古呼和浩特市第十六中学2020-2021学年高二上学期第一次质量检测化学试题吉林省汪清县汪清第四中学2020-2021学年高二上学期第二阶段考试化学试题安徽省泗县第一中学2020-2021学年高二上学期第二次月考化学试题吉林省延边朝鲜族自治州汪清县第四中学2020-2021学年高二上学期期末考试化学试题甘肃省民勤县第四中学2020-2021学年高二下学期开学考试化学试题选择性必修1 专题3 第三单元 突破4 溶液中粒子浓度的数量关系(已下线)3.3.1 盐溶液的酸碱性及其原因(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)四川省广安代市中学校2021-2022学年上学期高二第三次月考化学试题



