解题方法
1 . 按要求写出下列离子方程式
(1)(NH4)2SO4水解:_______ 。
(2)NaHCO3水解:_______ 。
(3)Ag2CrO4沉淀溶解平衡:_______ 。
(4)氢氧燃料电池(酸性):已知总电极反应式为H2+ O2=H2O。则负极反应式:
O2=H2O。则负极反应式:_______ 、正极反应式_______ 。
(5)已知AgCl为难溶于水和酸的白色固体,Ag2S为难溶于水和酸的黑色固体。向AgCl和水形成的悬浊液中加入足量的Na2S溶液并振荡,结果白色固体完全转化为黑色固体:
①写出白色固体转化为黑色固体的化学方程式:_______ 。
②简要说明白色固体转化为黑色固体的原因:_______ 。
(1)(NH4)2SO4水解:
(2)NaHCO3水解:
(3)Ag2CrO4沉淀溶解平衡:
(4)氢氧燃料电池(酸性):已知总电极反应式为H2+
 O2=H2O。则负极反应式:
O2=H2O。则负极反应式:(5)已知AgCl为难溶于水和酸的白色固体,Ag2S为难溶于水和酸的黑色固体。向AgCl和水形成的悬浊液中加入足量的Na2S溶液并振荡,结果白色固体完全转化为黑色固体:
①写出白色固体转化为黑色固体的化学方程式:
②简要说明白色固体转化为黑色固体的原因:
您最近一年使用:0次
2 . 下列物质在常温下发生水解时,对应的水解方程式正确的是
A.Na2CO3: +H2O +H2O 2OH-+CO2↑ 2OH-+CO2↑ |
B.NH4NO3: +H2O +H2O NH3·H2O+OH- NH3·H2O+OH- |
C.CuSO4:Cu2++2H2O Cu(OH)2↓+2H+ Cu(OH)2↓+2H+ |
D.KF:F-+H2O HF+OH- HF+OH- |
您最近一年使用:0次
名校
解题方法
3 . 下列有关电极方程式或离子方程式书写正确的是
A. 溶液与稀硫酸混合: 溶液与稀硫酸混合: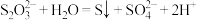 |
B.碱性条件下 燃料电池的负极反应: 燃料电池的负极反应: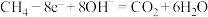 |
C.泡沫灭火器的反应原理: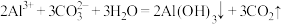 |
D.酸性 溶液与草酸溶液混合: 溶液与草酸溶液混合: |
您最近一年使用:0次
名校
解题方法
4 . 氮的氧化物是造成大气污染的主要物质,以乙烯(C2H4)作为还原剂的脱硝(NO)机理如图所示,下列说法正确的是
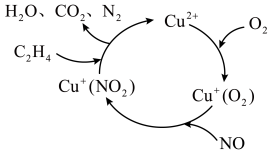

A.H2CO3的电离方程式为H2CO3 2H+ + 2H+ + |
| B.该机理图中,Cu2+、Cu+ (O2)和Cu+(NO2)均为催化剂 |
C.Cu2+与水反应的离子方程式为Cu2++2H2O Cu(OH)2↓+2H+ Cu(OH)2↓+2H+ |
| D.该反应的化学方程式可能为C2H4+2NO+2O2=2H2O+2CO2+N2 |
您最近一年使用:0次
2024-01-14更新
|
97次组卷
|
3卷引用:河北省保定市定州市第二中学2023-2024学年高二上学期12月月考化学试题
名校
5 . 化学用语可以表达化学过程,下列化学用语表达正确的是
A. 的价电子轨道表示式: 的价电子轨道表示式: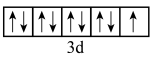 |
B.将氢硫酸滴加到硫酸铁溶液中: |
C. 溶液显碱性的原因: 溶液显碱性的原因: |
D.用电子式表示 的形成过程: 的形成过程: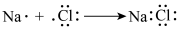 |
您最近一年使用:0次
名校
解题方法
6 . 已知25℃时电离常数: :
: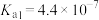
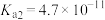 ;HClO:
;HClO: ,下列化学用语正确的是
,下列化学用语正确的是
 :
: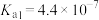
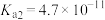 ;HClO:
;HClO: ,下列化学用语正确的是
,下列化学用语正确的是A.少量 通入 通入 溶液,体系中存在: 溶液,体系中存在: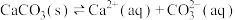 |
B. 溶液存在水解平衡: 溶液存在水解平衡: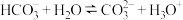 |
C.向NaClO溶液中通入少量 : :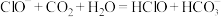 |
D.将 溶液和 溶液和 混合: 混合: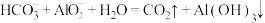 |
您最近一年使用:0次
名校
7 . 微粒观和变化观是中学生需要具备的核心素养。下列式子属于水解反应方程式的是
A. | B.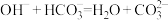 |
C.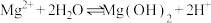 | D.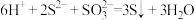 |
您最近一年使用:0次
2023-10-26更新
|
488次组卷
|
6卷引用:河北省邢台市五岳联盟2023-2024学年高二上学期11月期中考试化学试题
名校
8 . 向100 mL 0.01 mol·L-1Ba(OH)2溶液中滴加0.1 mol·L-1NaHCO3溶液,测得溶液的电导率变化如图。下列说法正确的是
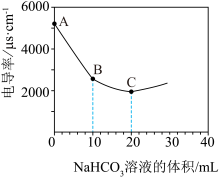

A.NaHCO3在水中的电离方程式为 |
B.A→B的过程中,溶液中 的浓度在逐渐增大 的浓度在逐渐增大 |
C.B→C的过程中,发生反应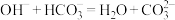 |
| D.B、C两点的阴离子浓度相等 |
您最近一年使用:0次
2023-09-23更新
|
279次组卷
|
7卷引用:河北省部分学校2023-2024学年高三一轮复习联考(一)化学试题
9 . 下列离子方程式,不能正确解释相应现象的是
A.长期放置的 溶液中含有 溶液中含有 : : |
B. 溶液中 溶液中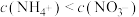 : :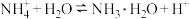 |
C.向 溶液中加入适量 溶液中加入适量 得到蓝色沉淀: 得到蓝色沉淀: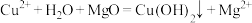 |
D.长期放置的 溶液中出现红棕色固体: 溶液中出现红棕色固体: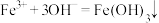 |
您最近一年使用:0次
解题方法
10 . I.某化学兴趣小组探究铁粉与硫酸铜溶液反应时溶液pH变化。
(1)甲同学提出硫酸铜溶液显酸性,理由是_______ (写离子方程式),加入铁粉消耗了 和
和 ,溶液pH会
,溶液pH会_______ (填“增大”、“不变”或“减小”;已知相同条件下, 的水解程度强于
的水解程度强于 )。
)。
Ⅱ.乙同学用pH传感器测铁粉和 溶液反应时溶液pH的变化。
溶液反应时溶液pH的变化。
【实验用品】仪器:pH传感器、笔记本电脑、带橡皮塞的 三颈烧瓶、铁架台、分液漏斗等。
三颈烧瓶、铁架台、分液漏斗等。
试剂: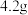 铁粉、
铁粉、 溶液。
溶液。
【实验步骤】向三颈烧瓶中加入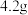 铁粉,将
铁粉,将 溶液滴入铁粉中,同时插入pH传感器检测溶液pH的变化,实验装置(夹持装置已省略)及测得的pH变化曲线如图所示。
溶液滴入铁粉中,同时插入pH传感器检测溶液pH的变化,实验装置(夹持装置已省略)及测得的pH变化曲线如图所示。
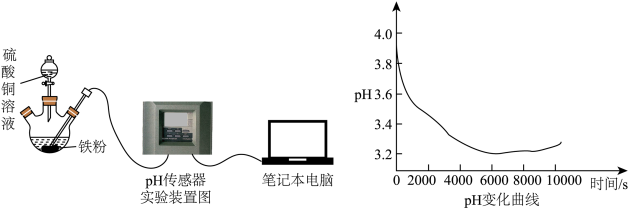
(2)乙同学猜想反应过程中pH下降与亚铁离子和溶液中氧气反应有关,理由是_______ (写离子方程式;常温下, 在
在 时完全沉淀)。
时完全沉淀)。
(3)为了验证猜想,乙同学用煮沸后冷却的蒸馏水新配制 溶液,重新进行实验。
溶液,重新进行实验。
①配制 溶液所用的蒸馏水需提前煮沸、冷却的目的是
溶液所用的蒸馏水需提前煮沸、冷却的目的是_______ ,配制 溶液需要称量
溶液需要称量_______ (保留小数点后一位)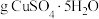 。
。
②下列实验操作会使所配制的溶液浓度偏高的是_______ (填标号)。
a.所称量的 失去部分结晶水
失去部分结晶水
b.容量瓶洗净后刻度线下残留少量水未处理
c.移液后未洗涤烧杯和玻璃棒
d.未用 溶液润洗容量瓶
溶液润洗容量瓶
③改进之后测得溶液pH的变化趋势为_______ ,证明乙同学的猜想正确(忽略容器内空气对实验的影响)。
(1)甲同学提出硫酸铜溶液显酸性,理由是
 和
和 ,溶液pH会
,溶液pH会 的水解程度强于
的水解程度强于 )。
)。Ⅱ.乙同学用pH传感器测铁粉和
 溶液反应时溶液pH的变化。
溶液反应时溶液pH的变化。【实验用品】仪器:pH传感器、笔记本电脑、带橡皮塞的
 三颈烧瓶、铁架台、分液漏斗等。
三颈烧瓶、铁架台、分液漏斗等。试剂:
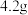 铁粉、
铁粉、 溶液。
溶液。【实验步骤】向三颈烧瓶中加入
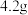 铁粉,将
铁粉,将 溶液滴入铁粉中,同时插入pH传感器检测溶液pH的变化,实验装置(夹持装置已省略)及测得的pH变化曲线如图所示。
溶液滴入铁粉中,同时插入pH传感器检测溶液pH的变化,实验装置(夹持装置已省略)及测得的pH变化曲线如图所示。
(2)乙同学猜想反应过程中pH下降与亚铁离子和溶液中氧气反应有关,理由是
 在
在 时完全沉淀)。
时完全沉淀)。(3)为了验证猜想,乙同学用煮沸后冷却的蒸馏水新配制
 溶液,重新进行实验。
溶液,重新进行实验。①配制
 溶液所用的蒸馏水需提前煮沸、冷却的目的是
溶液所用的蒸馏水需提前煮沸、冷却的目的是 溶液需要称量
溶液需要称量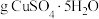 。
。②下列实验操作会使所配制的溶液浓度偏高的是
a.所称量的
 失去部分结晶水
失去部分结晶水b.容量瓶洗净后刻度线下残留少量水未处理
c.移液后未洗涤烧杯和玻璃棒
d.未用
 溶液润洗容量瓶
溶液润洗容量瓶③改进之后测得溶液pH的变化趋势为
您最近一年使用:0次



