名校
解题方法
1 . 下列表示水解反应的离子方程式正确的是
A.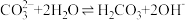 | B.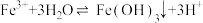 |
C. | D. |
您最近一年使用:0次
2 . 水是生命之源,下列改善水质的相关事实与方程式不相符 的是
A.用 溶液除去废水中的 溶液除去废水中的 : : |
B.用食醋处理水垢中的 : :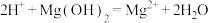 |
C.用明矾净化水: |
D.用碳酸钠溶液处理水垢中的硫酸钙: |
您最近一年使用:0次
3 . 下列用于解释事实的化学用语书写不正确 的是
| A.钢铁发生吸氧腐蚀的正极反应:O2+2H2O+4e-=4OH− |
B.Na2CO3溶液显碱性从而清洗油污的原理:CO +2H2O +2H2O H2CO3+2OH− H2CO3+2OH− |
C.Na2CO3溶液处理水垢中CaSO4:CaSO4(s)+CO (aq) (aq) CaCO3(s)+SO CaCO3(s)+SO (aq) (aq) |
| D.TiCl4水解制备TiO2的反应原理:TiCl4+(x+2)H2O=TiO2•xH2O↓+4HCl |
您最近一年使用:0次
解题方法
4 . 实验小组对Mg与NH4Cl溶液的反应进行探究。
(1)用pH计测定1.0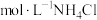 溶液约为4.6,分析NH4Cl溶液呈酸性的原因
溶液约为4.6,分析NH4Cl溶液呈酸性的原因______ (用化学用语表示)。
(2)探究镁与NH4Cl溶液的反应:实验Ⅰ、Ⅱ所取镁粉质量均为0.5g,分别加入选取的实验试剂中。
①实验Ⅰ中发生反应的化学方程式为______ 。
②经检验实验Ⅱ中刺激性气味气体为NH3和H2的混合气体,用平衡移动原理解释产生NH3的原因______ 。
③已知灰白色沉淀中含有Mg2+、OH-。为研究固体成分,进行实验:将生成的灰白色固体洗涤数次,至洗涤液中滴加AgNO3溶液后无明显浑浊。将洗涤后的固体溶于稀HNO3,再滴加AgNO3溶液,出现白色沉淀。推测沉淀中含有______ ,灰白色固体可能是______ (填化学式)。
④针对实验Ⅱ比实验Ⅰ反应剧烈的原因,小组同学提出了两种假设:
假设l:NH4Cl溶液中的H+溶解了Mg(OH)2;
假设2:NH4Cl溶液中的 溶解了Mg(OH)2。
溶解了Mg(OH)2。
为证明假设的合理性.小组同学做了如下对比实验:
实验结论是______ 。
(3)甲同学通过深入思考,认为Mg与NH4Cl溶液反应剧烈.可能还与 有关.并通过设计实验,证明了猜想的正确性.他设计的实验方案和实验证据为
有关.并通过设计实验,证明了猜想的正确性.他设计的实验方案和实验证据为______ 。
(4)由上述实验得出的结论是______ 。
(1)用pH计测定1.0
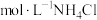 溶液约为4.6,分析NH4Cl溶液呈酸性的原因
溶液约为4.6,分析NH4Cl溶液呈酸性的原因(2)探究镁与NH4Cl溶液的反应:实验Ⅰ、Ⅱ所取镁粉质量均为0.5g,分别加入选取的实验试剂中。
实验 | 实验试剂 | 实验现象 |
Ⅰ | 5mL蒸馏水 | 反应缓慢,有少量气泡产生(经检验为H2) |
Ⅱ | 5mL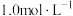 NH4Cl溶液(pH=4.6) | 剧烈反应,产生刺激性气味气体和灰白色难溶固体 |
②经检验实验Ⅱ中刺激性气味气体为NH3和H2的混合气体,用平衡移动原理解释产生NH3的原因
③已知灰白色沉淀中含有Mg2+、OH-。为研究固体成分,进行实验:将生成的灰白色固体洗涤数次,至洗涤液中滴加AgNO3溶液后无明显浑浊。将洗涤后的固体溶于稀HNO3,再滴加AgNO3溶液,出现白色沉淀。推测沉淀中含有
④针对实验Ⅱ比实验Ⅰ反应剧烈的原因,小组同学提出了两种假设:
假设l:NH4Cl溶液中的H+溶解了Mg(OH)2;
假设2:NH4Cl溶液中的
 溶解了Mg(OH)2。
溶解了Mg(OH)2。为证明假设的合理性.小组同学做了如下对比实验:
实验 | 实验方案 | 实验现象 |
Ⅲ | 取2根覆盖了Mg(OH)2的Mg条,分别同时放入相同体积相同pH的盐酸和饱和NH4Cl溶液中。 | 饱和NH4Cl溶液中反应更剧烈。 |
Ⅳ | 向饱和NH4Cl溶液中滴加浓氨水,使溶液呈中性或略显碱性,再放入覆盖了Mg(OH)2的镁条。 | 剧烈反应,但是比实验Ⅲ饱和NH4Cl溶液略慢,产生刺激性气味气体和灰白色难溶固体。 |
(3)甲同学通过深入思考,认为Mg与NH4Cl溶液反应剧烈.可能还与
 有关.并通过设计实验,证明了猜想的正确性.他设计的实验方案和实验证据为
有关.并通过设计实验,证明了猜想的正确性.他设计的实验方案和实验证据为(4)由上述实验得出的结论是
您最近一年使用:0次
2024-01-24更新
|
85次组卷
|
2卷引用:北京市顺义区2023-2024学年高二上学期期末质量监测化学试题
名校
5 . 下列化学用语对事实的表述正确 的是
A.常温时,饱和 溶液的 溶液的 约为11: 约为11: |
B.电解饱和食盐水: |
C.向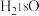 中投入 中投入 固体: 固体: |
D.苯酚和甲醛在一定条件下反应能生成酚醛树脂:n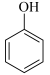 +nHCHO +nHCHO 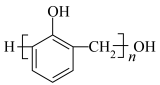 +(n-1)H2O +(n-1)H2O |
您最近一年使用:0次
名校
解题方法
6 . ①醋酸、②盐酸、③一水合氨、④碳酸氢钠、⑤氯化钙、⑥氯化铵是实验室中的常见物质。
(1)写出一水合氨的电离方程式___________ 。
(2)碳酸氢钠溶液显碱性,结合化学用语解释原因:___________ 。
(3)有关0.1mol·L-1 CH3COOH溶液的叙述正确的是___________ 。
a.CH3COOH溶液中离子浓度关系满足:c(CH3COO-)>c(OH-)>c(H+)
b.常温下,等物质的量浓度、等体积CH3COOH溶液与NaOH溶液混合后溶液pH=7
c.向CH3COOH溶液中加少量CH3COONa固体,c(H+)减小
d.向CH3COOH溶液中加少量Na2CO3固体,c(CH3COO-)增大
e.与同浓度盐酸溶液的导电性相同
(4)25℃时,pH均等于4的醋酸溶液和氯化铵溶液,醋酸溶液中水电离出的c(H+)与氯化铵溶液中水电离出的c(H+)之比是___________ 。
(5)向饱和NaHCO3溶液中滴加饱和CaCl2溶液,可观察到先产生白色沉淀,后产生大量无色气泡,结合化学用语,从平衡移动角度解释原因___________ 。
(1)写出一水合氨的电离方程式
(2)碳酸氢钠溶液显碱性,结合化学用语解释原因:
(3)有关0.1mol·L-1 CH3COOH溶液的叙述正确的是
a.CH3COOH溶液中离子浓度关系满足:c(CH3COO-)>c(OH-)>c(H+)
b.常温下,等物质的量浓度、等体积CH3COOH溶液与NaOH溶液混合后溶液pH=7
c.向CH3COOH溶液中加少量CH3COONa固体,c(H+)减小
d.向CH3COOH溶液中加少量Na2CO3固体,c(CH3COO-)增大
e.与同浓度盐酸溶液的导电性相同
(4)25℃时,pH均等于4的醋酸溶液和氯化铵溶液,醋酸溶液中水电离出的c(H+)与氯化铵溶液中水电离出的c(H+)之比是
(5)向饱和NaHCO3溶液中滴加饱和CaCl2溶液,可观察到先产生白色沉淀,后产生大量无色气泡,结合化学用语,从平衡移动角度解释原因
您最近一年使用:0次
名校
解题方法
7 . 下列化学用语表达正确的是
A.纯碱溶液显碱性:CO +2H2O +2H2O H2CO3+2OH- H2CO3+2OH- |
B.向碳酸氢钠溶液中加入醋酸溶液:HCO +H+=H2O+CO2↑ +H+=H2O+CO2↑ |
C.硫酸铜溶液显酸性:Cu2++2H2O Cu(OH)2↓+2H+ Cu(OH)2↓+2H+ |
D.硫酸铝和碳酸氢钠互相促进水解:Al3++3HCO =Al(OH)3↓+3CO2↑ =Al(OH)3↓+3CO2↑ |
您最近一年使用:0次
名校
解题方法
8 . 下列对生产生活中的原理描述不准确的是
| 选项 | 事 实 | 解 释 |
| A | 用纯碱去除厨房油污 |  ,碱性条件有利 于油脂水解 ,碱性条件有利 于油脂水解 |
| B | FeCl3 溶液蒸干后得到 Fe(OH)3 | 升温以及生成的 HCl 挥发,使得 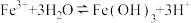 正向移动 正向移动 |
| C | 用 Al2(SO4)3 作净水剂 | Al3+ 和天然水中 的水解相互促进,生成 Al(OH)3 胶体,吸附水中悬浮物,加速其沉降 的水解相互促进,生成 Al(OH)3 胶体,吸附水中悬浮物,加速其沉降 |
| D | 用 BaSO4 作内服造影剂 | 胃液中高浓度的H+对BaSO4 的沉淀溶解平衡基本 没有影响,Ba2+可以保持在安全浓度范围内 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-01-14更新
|
116次组卷
|
2卷引用:北京市第十一中学2022-2023学年高二上学期期末考试化学试题
名校
9 . 下列实验“实验结论”与“操作及现象”不相符的一组是
实验操作及现象 | 实验结论 | |
A | 碳酸钠溶液中滴加酚酞,溶液变红 | CO |
B | 相同条件下,测得相同体积的0.1mol/L的稀盐酸导电能力大于稀醋酸的导电能力 | 说明稀盐酸中一定不存在HCl分子 |
C | 将充满NO2的密闭玻璃球浸泡在热水中,玻璃球中红棕色加深 | 说明反应:2NO2(g) |
D | 锌与稀硫酸反应制取氢气,加入少量CuSO4溶液,产生氢气速率明显加快 | 形成了铜锌原电池加快反应速率 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-01-12更新
|
45次组卷
|
2卷引用:北京市八一学校2023-2024学年高二上学期12月月考化学试题
10 . 印刷电路板废液主要含(CuCl2、FeCl2以及少量的FeCl3等物质, 以废液为原料制备CuSO4,实现资源回收再利用,流程如下图所示。
(1)粗CuSO4溶液的制备
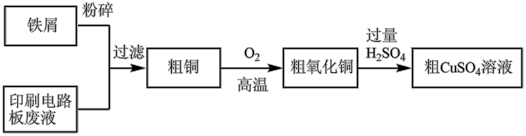
① 上述流程中能加快反应速率的措施有___________ 。
② 加入铁屑后,印刷电路板废液中发生的离子反应有___________ 。
(2)CuSO4溶液的精制
i.经检验,粗CuSO4溶液含有Fe2+
ii.向粗CuSO4溶液滴加 3%的H2O2溶液,当溶液中Fe2+完全氧化后,加 A物质的粉末调节溶液的 pH=4。
iii.将溶液加热至沸,趁热减压过滤,得到精制CuSO4溶液。
① ii中,用离子方程式说明加入H2O2溶液的作用___________ ;A物质是___________ 。
② 25℃时,Ksp[Cu(OH)2]=2.2×10-20,Ksp[Fe(OH)3]=2.8×10-39 。pH=4 时,c(Fe3+)________ mol∙L−1。 判断Cu2+此时尚未开始沉淀,依据是___________ 。 (25℃时,CuSO4饱和溶液中Cu2+的物质的量浓度约为 1.4mol·L⁻¹)
③ 精制CuSO4溶液显酸性,原因是___________ (用离子方程式表示)
(3)制备CuSO4∙5H2O晶体
向精制的CuSO4溶液中加一定量硫酸,________ ,过滤,洗涤干燥,得到CuSO4∙5H2O晶体。
(1)粗CuSO4溶液的制备

① 上述流程中能加快反应速率的措施有
② 加入铁屑后,印刷电路板废液中发生的离子反应有
(2)CuSO4溶液的精制
i.经检验,粗CuSO4溶液含有Fe2+

ii.向粗CuSO4溶液滴加 3%的H2O2溶液,当溶液中Fe2+完全氧化后,加 A物质的粉末调节溶液的 pH=4。
iii.将溶液加热至沸,趁热减压过滤,得到精制CuSO4溶液。
① ii中,用离子方程式说明加入H2O2溶液的作用
② 25℃时,Ksp[Cu(OH)2]=2.2×10-20,Ksp[Fe(OH)3]=2.8×10-39 。pH=4 时,c(Fe3+)
③ 精制CuSO4溶液显酸性,原因是
(3)制备CuSO4∙5H2O晶体
向精制的CuSO4溶液中加一定量硫酸,
您最近一年使用:0次



