1 . 盐与碱的反应是水溶液中常见的反应,某学习小组展开相关探究。
Ⅰ.NH4Cl抗碱容量(σ)的测定
(1)某小组同学测定NH4Cl固体抗碱容量的实验步骤如下:
a.配置100mL0.2mol·L-1NaOH溶液;
b.称取xgNH4Cl固体,溶于20mL水中,用上述NaOH溶液滴定至pH=11.
已知:氯化铵的抗碱容量是指用NaOH溶液滴定NH4Cl溶液至pH=11时,单位质量的NH4Cl所消耗NaOH的物质的量,即σ=
①步骤a需要称量NaOH固体为______ g(保留一位小数)
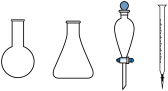
②步骤b需要用到下图所示仪器中的______ (填名称)。______ mol·g-1
Ⅱ.NH4Cl-NH3混合溶液抗碱能力的探究
NH4Cl-NH3混合溶液具有抗碱能力。向该溶液中加入少量NaOH,溶液的pH变化不大。
已知:i.25℃时,NH3·H2O的Kb=1.75×10-5=10-4.8
ii.NH4Cl-NH3混合溶液的抗碱能力与 、[c(
、[c( )+c(NH3)]有关
)+c(NH3)]有关
(2)NH4Cl溶液显酸性,用离子方程式解释原因:______ 。
(3)小组同学设计实验探究[c )+c(NH3)]一定时,
)+c(NH3)]一定时, 对混合溶液抗碱能力的影响。分别向溶液1、溶液2、溶液3、溶液4中滴加0.1mol·L-1NaOH溶液,溶液的pH随加入NaOH的变化情况如下图所示
对混合溶液抗碱能力的影响。分别向溶液1、溶液2、溶液3、溶液4中滴加0.1mol·L-1NaOH溶液,溶液的pH随加入NaOH的变化情况如下图所示
①实验结果显示,NaCl溶液不具备抗碱能力,即曲线______ (填曲线标号)表示溶液1.
②实验结果显示,当[c( )+c(NH3)]相同时,
)+c(NH3)]相同时, 越大,混合溶液的抗碱能力越强,则曲线b表示溶液
越大,混合溶液的抗碱能力越强,则曲线b表示溶液______ (填溶液组号)
③已知A点时,c(NH4+)=c(NH3·H2O),则此时溶液的pH=______ (精确至小数点后1位)。
Ⅰ.NH4Cl抗碱容量(σ)的测定
(1)某小组同学测定NH4Cl固体抗碱容量的实验步骤如下:
a.配置100mL0.2mol·L-1NaOH溶液;
b.称取xgNH4Cl固体,溶于20mL水中,用上述NaOH溶液滴定至pH=11.
已知:氯化铵的抗碱容量是指用NaOH溶液滴定NH4Cl溶液至pH=11时,单位质量的NH4Cl所消耗NaOH的物质的量,即σ=

①步骤a需要称量NaOH固体为
②步骤b需要用到下图所示仪器中的
Ⅱ.NH4Cl-NH3混合溶液抗碱能力的探究
NH4Cl-NH3混合溶液具有抗碱能力。向该溶液中加入少量NaOH,溶液的pH变化不大。
已知:i.25℃时,NH3·H2O的Kb=1.75×10-5=10-4.8
ii.NH4Cl-NH3混合溶液的抗碱能力与
 、[c(
、[c( )+c(NH3)]有关
)+c(NH3)]有关(2)NH4Cl溶液显酸性,用离子方程式解释原因:
(3)小组同学设计实验探究[c
 )+c(NH3)]一定时,
)+c(NH3)]一定时, 对混合溶液抗碱能力的影响。分别向溶液1、溶液2、溶液3、溶液4中滴加0.1mol·L-1NaOH溶液,溶液的pH随加入NaOH的变化情况如下图所示
对混合溶液抗碱能力的影响。分别向溶液1、溶液2、溶液3、溶液4中滴加0.1mol·L-1NaOH溶液,溶液的pH随加入NaOH的变化情况如下图所示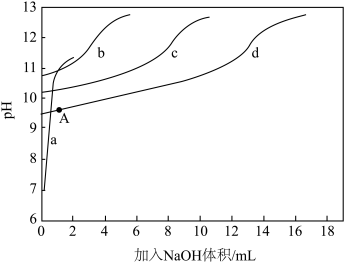
| 溶液组号 | 组成 | 体积/mL |
| 1 | 0.2mol·L-1NaCl溶液 | 15 |
| 2 | 0.1mol·L-1NH4Cl | 3 |
| 0.1mol·L-1氨水 | 12 | |
| 3 | 0.1mol·L-1NH4Cl | 7.5 |
| 0.1mol·L-1氨水 | 7.5 | |
| 4 | 0.1mol·L-1NH4Cl | 12 |
| 0.1mol·L-1氨水 | 3 |
②实验结果显示,当[c(
 )+c(NH3)]相同时,
)+c(NH3)]相同时, 越大,混合溶液的抗碱能力越强,则曲线b表示溶液
越大,混合溶液的抗碱能力越强,则曲线b表示溶液③已知A点时,c(NH4+)=c(NH3·H2O),则此时溶液的pH=
您最近一年使用:0次
名校
解题方法
2 . 室温下,向亚硫酸溶液中滴加 溶液,各含硫微粒分布系数(平衡时某微粒的物质的量占各微粒物质的量之和的分数)与溶液
溶液,各含硫微粒分布系数(平衡时某微粒的物质的量占各微粒物质的量之和的分数)与溶液 的关系如图所示。下列说法不正确的是
的关系如图所示。下列说法不正确的是
 溶液,各含硫微粒分布系数(平衡时某微粒的物质的量占各微粒物质的量之和的分数)与溶液
溶液,各含硫微粒分布系数(平衡时某微粒的物质的量占各微粒物质的量之和的分数)与溶液 的关系如图所示。下列说法不正确的是
的关系如图所示。下列说法不正确的是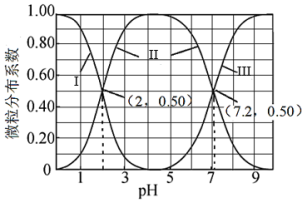
A.曲线Ⅱ表示 的分布系数随 的分布系数随 的变化 的变化 |
B. 的二级电离平衡常数( 的二级电离平衡常数(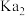 )的数量级为 )的数量级为 |
C. 时, 时,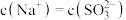 |
D. 溶液中水电离出的 溶液中水电离出的 |
您最近一年使用:0次
2024-01-17更新
|
402次组卷
|
5卷引用:广东省惠州市第一中学2023-2024学年高二下学期4月月考化学试题
广东省惠州市第一中学2023-2024学年高二下学期4月月考化学试题福建省厦门市松柏中学2023-2024学年高三上学期第三次月考化学试卷(已下线)化学(九省联考考后提升卷,江西卷)-2024年1月“九省联考”真题完全解读与考后提升湖南省宁乡市第一高级中学2021届高三第三次模拟考试化学试卷宁夏回族自治区银川一中2024届高三下学期三模理综试题-高中化学
名校
3 .  时,有
时,有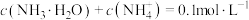 的一组
的一组 、
、 混合溶液,溶液中
混合溶液,溶液中 和
和 与溶液pH的关系如图所示。下列说法错误的是
与溶液pH的关系如图所示。下列说法错误的是
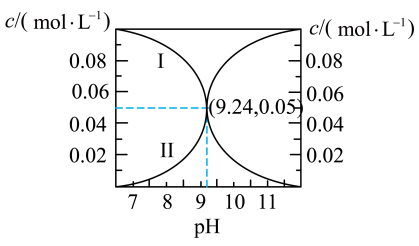
 时,有
时,有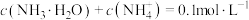 的一组
的一组 、
、 混合溶液,溶液中
混合溶液,溶液中 和
和 与溶液pH的关系如图所示。下列说法错误的是
与溶液pH的关系如图所示。下列说法错误的是
A.曲线Ⅰ表示 |
B. |
C. 时, 时,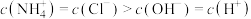 |
D.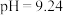 时, 时, |
您最近一年使用:0次
2023-06-24更新
|
75次组卷
|
2卷引用:广东省惠州市龙门县高级中学2021-2022学年高二下学期开学测试化学试题
名校
解题方法
4 .  是一种弱碱,可与盐酸反应生成
是一种弱碱,可与盐酸反应生成 。下列叙述正确的是
。下列叙述正确的是
 是一种弱碱,可与盐酸反应生成
是一种弱碱,可与盐酸反应生成 。下列叙述正确的是
。下列叙述正确的是A.常温时,0.1mol/L 水溶液的 水溶液的 |
B.0.1mol/L 水溶液加水稀释, 水溶液加水稀释, 升高 升高 |
C.0.1mol/L 水溶液中: 水溶液中: |
D. 水溶液中: 水溶液中: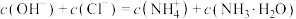 |
您最近一年使用:0次
2023-06-22更新
|
791次组卷
|
4卷引用:广东省惠州市2024届高三第一次调研考试化学试题
广东省惠州市2024届高三第一次调研考试化学试题(已下线)第九章单元测试卷(已下线)考点3 盐类水解(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)广东省深圳市福田区福田中学2023-2024学年高三上学期12月月考化学考试
名校
5 . 常温下,体积和浓度一定的 溶液中各微粒浓度的负对数(
溶液中各微粒浓度的负对数(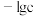 )随溶液pH的变化关系如图所示。下列叙述正确的是
)随溶液pH的变化关系如图所示。下列叙述正确的是
 溶液中各微粒浓度的负对数(
溶液中各微粒浓度的负对数(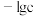 )随溶液pH的变化关系如图所示。下列叙述正确的是
)随溶液pH的变化关系如图所示。下列叙述正确的是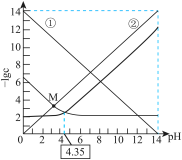
A.曲线②表示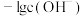 随溶液pH的变化情况 随溶液pH的变化情况 |
B.等物质的量浓度 和 和 混合溶液: 混合溶液: |
C. 的 的 的数量级为 的数量级为 |
D.常温下,将M点对应溶液加水稀释,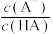 不变 不变 |
您最近一年使用:0次
2023-04-01更新
|
782次组卷
|
7卷引用:广东省惠州市第一中学 珠海市第一中学2023-2024学年高二上学期12月期中联考化学试题
6 . 下列说法不正确的是
| A.热的纯碱溶液去油污洗涤效果更好 |
B.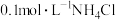 溶液中电荷守恒为 溶液中电荷守恒为 |
C.配制 溶液时,直接将 溶液时,直接将 晶体溶于水即可制得 晶体溶于水即可制得 |
D.已知常温下 , ,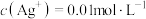 时,当 时,当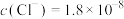 开始沉淀 开始沉淀 |
您最近一年使用:0次
2023-03-02更新
|
237次组卷
|
2卷引用:广东省惠州市2022-2023学年高二上学期期末质量检测化学试题
解题方法
7 . 烟气脱硫脱硝技术是环境科学研究的热点。某小组模拟 氧化结合溶液吸收法同时脱除
氧化结合溶液吸收法同时脱除 和
和 ,主要反应原理及相关数据如下表。
,主要反应原理及相关数据如下表。
回答下列问题:
(1)①已知: 则
则
_______ 。 时
时
_______ 。
②其他条件不变, 和
和 初始的物质的量浓度相等时,经检测发现,在相同时间内,
初始的物质的量浓度相等时,经检测发现,在相同时间内, 和
和 的转化率随
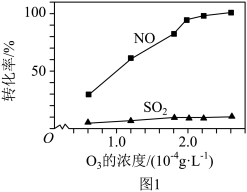
的转化率随 的浓度的变化如图1,结合数据分析
的浓度的变化如图1,结合数据分析 的转化率高于
的转化率高于 的原因:
的原因:_______ 。
③ 与
与 反应生成的
反应生成的 的平衡
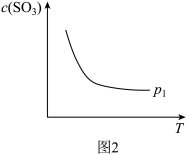
的平衡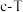 (浓度—温度)如图2所示,请画出其他条件不变,压强
(浓度—温度)如图2所示,请画出其他条件不变,压强 (
(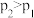 )下的
)下的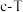 图像。
图像。_______
(2)① 溶液显碱性,用化学平衡原理解释:
溶液显碱性,用化学平衡原理解释:_______ 。
②下列有关该溶液的说法正确的是_______ (填标号)。
A.加入少量水,溶液中离子总数增加
B.溶液中存在: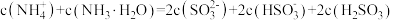
C.常温下 时,
时,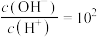
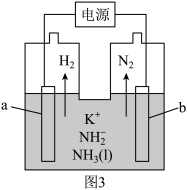
③液氨中存在平衡: 。如图3所示为电解池装置,以
。如图3所示为电解池装置,以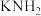 的液氨溶液为电解液,电解过程中a、b两个惰性电极上都有气泡产生。请写出阴极的电极反应式:
的液氨溶液为电解液,电解过程中a、b两个惰性电极上都有气泡产生。请写出阴极的电极反应式:_______ 。
 氧化结合溶液吸收法同时脱除
氧化结合溶液吸收法同时脱除 和
和 ,主要反应原理及相关数据如下表。
,主要反应原理及相关数据如下表。| 反应 | 平衡常数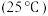 | 活化能/ |
反应a: | 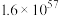 | 24.6 |
反应b: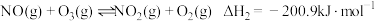 | 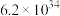 | 3.17 |
反应c: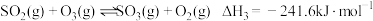 | 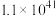 | 58.17 |
回答下列问题:
(1)①已知:
 则
则
 时
时
②其他条件不变,
 和
和 初始的物质的量浓度相等时,经检测发现,在相同时间内,
初始的物质的量浓度相等时,经检测发现,在相同时间内, 和
和 的转化率随
的转化率随 的浓度的变化如图1,结合数据分析
的浓度的变化如图1,结合数据分析 的转化率高于
的转化率高于 的原因:
的原因:
③
 与
与 反应生成的
反应生成的 的平衡
的平衡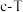 (浓度—温度)如图2所示,请画出其他条件不变,压强
(浓度—温度)如图2所示,请画出其他条件不变,压强 (
(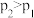 )下的
)下的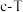 图像。
图像。
(2)①
 溶液显碱性,用化学平衡原理解释:
溶液显碱性,用化学平衡原理解释:②下列有关该溶液的说法正确的是
A.加入少量水,溶液中离子总数增加
B.溶液中存在:
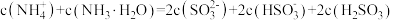
C.常温下
 时,
时,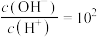
③液氨中存在平衡:
 。如图3所示为电解池装置,以
。如图3所示为电解池装置,以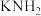 的液氨溶液为电解液,电解过程中a、b两个惰性电极上都有气泡产生。请写出阴极的电极反应式:
的液氨溶液为电解液,电解过程中a、b两个惰性电极上都有气泡产生。请写出阴极的电极反应式:
您最近一年使用:0次
8 . 常温下,向 溶液中滴加
溶液中滴加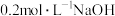 溶液。有关微粒 (
溶液。有关微粒 ( )物质的量变化如图。下列各粒子浓度之间关系正确的是
)物质的量变化如图。下列各粒子浓度之间关系正确的是
 溶液中滴加
溶液中滴加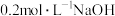 溶液。有关微粒 (
溶液。有关微粒 ( )物质的量变化如图。下列各粒子浓度之间关系正确的是
)物质的量变化如图。下列各粒子浓度之间关系正确的是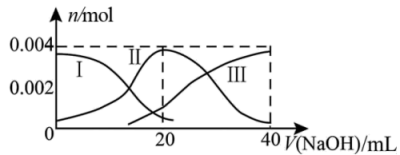
A. 的第一步电离平衡常数 的第一步电离平衡常数 |
B.当加入 体积为 体积为 时,溶液中: 时,溶液中: |
C.当加入 体积为 体积为 时,溶液中: 时,溶液中: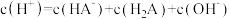 |
D.图中的Ⅱ线,代表 的变化 的变化 |
您最近一年使用:0次
2022-12-10更新
|
297次组卷
|
4卷引用:广东省惠州市四校2022-2023学年高二上学期联考化学试卷
名校
9 .  时,在
时,在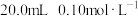 氨水中滴入
氨水中滴入 的盐酸,溶液
的盐酸,溶液 与所加盐酸的体积关系如图所示。
与所加盐酸的体积关系如图所示。
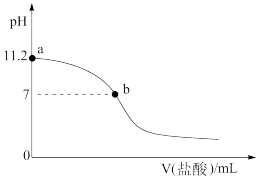
下列有关叙述不正确的是
 时,在
时,在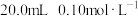 氨水中滴入
氨水中滴入 的盐酸,溶液
的盐酸,溶液 与所加盐酸的体积关系如图所示。
与所加盐酸的体积关系如图所示。
下列有关叙述不正确的是
A.a点对应溶液中已电离的 为 为 |
B.b点对应盐酸的体积等于 |
C.b点对应溶液中: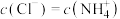 |
D.滴加入 盐酸时: 盐酸时: |
您最近一年使用:0次
2022-01-21更新
|
403次组卷
|
3卷引用:广东省惠州市2022-2023学年高二上学期期末质量检测化学试题
10 . 下列说法不正确 的是
| A.pH<7的溶液不一定显酸性 |
| B.中和pH和体积均相等的CH3COOH溶液与盐酸,所需NaOH的物质的量相同 |
| C.相同温度下,pH相等的盐酸、CH3COOH溶液中,c(OH−)相等 |
D.氨水和盐酸反应后的溶液,若溶液呈中性,则c(Cl−)=c(NH ) ) |
您最近一年使用:0次



