名校
解题方法
1 . Ka、Kw、Kh、Ksp分别表示电离常数、水的离子积常数、水解常数、溶度积常数,下列判断不正确的是
A.室温下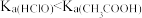 , , 的电离度一定比HClO的大 的电离度一定比HClO的大 |
B.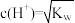 的溶液任何温度下均为中性 的溶液任何温度下均为中性 |
| C.已知25℃时,AgCl和砖红色沉淀Ag2CrO4的Ksp分别为1.8×10-10和2.0×10-12,则用AgNO3标准溶液滴定Cl-时,可采用K2CrO4为指示剂 |
| D.某温度下,一元弱酸HA的Ka越小,则NaA的Kh越大 |
您最近一年使用:0次
2023-12-25更新
|
489次组卷
|
8卷引用:河南省商丘市第一高级中学2022-2023学年高二下学期3月份考试化学试题
名校
2 . 利用平衡移动原理,分析常温下Ni2+在不同pH的Na2CO3体系中的可能产物。
已知:图1中曲线表示Na2CO3体系中各含碳粒子的物质的量分数与pH的关系;图2中曲线I的离子浓度关系符合 ;曲线Ⅱ的离子浓度关系符合
;曲线Ⅱ的离子浓度关系符合 ;[注:起始Na2CO3体系中
;[注:起始Na2CO3体系中 ;不同pH下c(CO
;不同pH下c(CO )由图1得到]。下列说法错误的是
)由图1得到]。下列说法错误的是
已知:图1中曲线表示Na2CO3体系中各含碳粒子的物质的量分数与pH的关系;图2中曲线I的离子浓度关系符合
 ;曲线Ⅱ的离子浓度关系符合
;曲线Ⅱ的离子浓度关系符合 ;[注:起始Na2CO3体系中
;[注:起始Na2CO3体系中 ;不同pH下c(CO
;不同pH下c(CO )由图1得到]。下列说法错误的是
)由图1得到]。下列说法错误的是
A.pH=7时,碳酸钠溶液体系中存在:c( )>c(H2CO3)>c( )>c(H2CO3)>c( ) ) |
B.M点时,溶液中存在c( )=c(OH-) )=c(OH-) |
C.初始状态pH=9、 ,平衡后存在 ,平衡后存在 |
D.沉淀Ni2+制备NiCO3时,选用0.1 NaHCO3溶液比0.1 NaHCO3溶液比0.1 Na2CO3溶液效果好 Na2CO3溶液效果好 |
您最近一年使用:0次
2023-10-07更新
|
1101次组卷
|
8卷引用:河南省信阳高级中学2023-2024学年高三上学期第八次月考理综试题
3 . 已知H2C2O4为二元弱酸,常温下将0.1mol·L-1的NaOH溶液滴入20mL0.1mol·L-1的NaHC2O4溶液中,溶液中 (或
(或 )的分布系数δ、NaOH溶液体积V与pH的关系如图所示[已知:
)的分布系数δ、NaOH溶液体积V与pH的关系如图所示[已知: ]。下列叙述正确的是
]。下列叙述正确的是
 (或
(或 )的分布系数δ、NaOH溶液体积V与pH的关系如图所示[已知:
)的分布系数δ、NaOH溶液体积V与pH的关系如图所示[已知: ]。下列叙述正确的是
]。下列叙述正确的是
A.曲线a表示的是 的分布系数变化曲线 的分布系数变化曲线 |
B.n点对应的溶液中, |
| C.Na2C2O4的水解平衡常数的数量级为10-9 |
| D.在n、p、q三点中,水的电离程度最大的是p点 |
您最近一年使用:0次
2023-08-22更新
|
247次组卷
|
3卷引用:河南省南阳市第八中学校2022-2023学年高三下学期第七次调研考试理科综合试卷-高中化学
名校
解题方法
4 . 下列说法不正确的是
| A.在一定条件下,Na2S溶液加入CuSO4固体,HS-浓度减小 |
| B.加水稀释,水解常数Kh增大,pH减小 |
| C.25℃时,Ka(HCOOH)=1.0×10-4,该温度下HCOO-的水解常数为1.0×10-10 |
| D.某温度下,一元弱酸HA的Ka越小,则NaA的Kh越大 |
您最近一年使用:0次
2023-08-14更新
|
691次组卷
|
4卷引用:河南省宜阳县第一高级中学2023-2024学年高二上学期能力达标测试化学试题
解题方法
5 . 丙二酸( )是二元弱酸。298K时,向一定浓度的
)是二元弱酸。298K时,向一定浓度的 溶液中滴加盐酸,混合溶液中含碳粒子浓度pX与pH的关系如图所示。已知:
溶液中滴加盐酸,混合溶液中含碳粒子浓度pX与pH的关系如图所示。已知: ,
, 或
或 )下列叙述正确的是
)下列叙述正确的是

 )是二元弱酸。298K时,向一定浓度的
)是二元弱酸。298K时,向一定浓度的 溶液中滴加盐酸,混合溶液中含碳粒子浓度pX与pH的关系如图所示。已知:
溶液中滴加盐酸,混合溶液中含碳粒子浓度pX与pH的关系如图所示。已知: ,
, 或
或 )下列叙述正确的是
)下列叙述正确的是
A.直线 表示pH与 表示pH与 的关系 的关系 |
B. 稀溶液与等体积、等浓度的盐酸混合后, 稀溶液与等体积、等浓度的盐酸混合后, |
C.当 时,溶液pH=3.26 时,溶液pH=3.26 |
D. 的溶液中的溶质可能是 的溶液中的溶质可能是 和 和 |
您最近一年使用:0次
6 . 食用磷酸钾(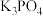 )可用作食品乳化剂,工业制备原理为:
)可用作食品乳化剂,工业制备原理为:
ⅰ. ,控制
,控制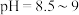 左右;
左右;
ⅱ.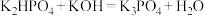 ,控制pH=14左右。
,控制pH=14左右。
已知常温下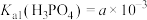 、
、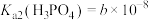 、
、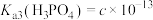 。
。
常温下,下列说法正确的是
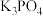 )可用作食品乳化剂,工业制备原理为:
)可用作食品乳化剂,工业制备原理为:ⅰ.
 ,控制
,控制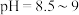 左右;
左右;ⅱ.
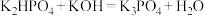 ,控制pH=14左右。
,控制pH=14左右。已知常温下
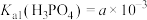 、
、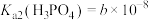 、
、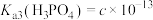 。
。常温下,下列说法正确的是
A. 溶液中由水电离出的氢离子浓度一定大于 溶液中由水电离出的氢离子浓度一定大于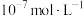 |
B.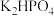 溶液中 溶液中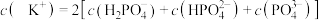 |
C.向 溶液中滴加少量KOH溶液,反应的离子方程式为 溶液中滴加少量KOH溶液,反应的离子方程式为 |
D.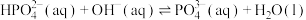 的化学平衡常数为10c 的化学平衡常数为10c |
您最近一年使用:0次
2023-06-21更新
|
65次组卷
|
2卷引用:河南省大联考2022-2023学年高二下学期阶段性测试(五)化学试题
名校
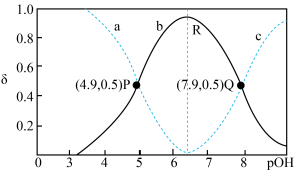
7 . 乙二胺 ( )是二元弱碱,在溶液中分步电离。25℃时,向一定浓度的乙二胺溶液中滴加稀盐酸,溶液中各含氮微粒的分布分数
)是二元弱碱,在溶液中分步电离。25℃时,向一定浓度的乙二胺溶液中滴加稀盐酸,溶液中各含氮微粒的分布分数 (平衡时某含氮微粒的浓度占各含氮微粒浓度之和的分数)随溶液
(平衡时某含氮微粒的浓度占各含氮微粒浓度之和的分数)随溶液 的变化如图所示。下列说法错误的是
的变化如图所示。下列说法错误的是
 )是二元弱碱,在溶液中分步电离。25℃时,向一定浓度的乙二胺溶液中滴加稀盐酸,溶液中各含氮微粒的分布分数
)是二元弱碱,在溶液中分步电离。25℃时,向一定浓度的乙二胺溶液中滴加稀盐酸,溶液中各含氮微粒的分布分数 (平衡时某含氮微粒的浓度占各含氮微粒浓度之和的分数)随溶液
(平衡时某含氮微粒的浓度占各含氮微粒浓度之和的分数)随溶液 的变化如图所示。下列说法错误的是
的变化如图所示。下列说法错误的是
A.曲线 表示 表示 微粒的分布分数 微粒的分布分数 随溶液 随溶液 的变化关系 的变化关系 |
B.常温下,R点溶液中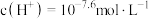 |
C.Q点溶液中的离子浓度关系: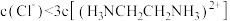 |
D.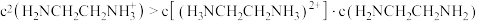 |
您最近一年使用:0次
2023-05-19更新
|
308次组卷
|
4卷引用:河南省开封市2022-2023学年高三下学期5月月考理综化学试题
8 .  溶液中存在多个平衡。本题条件下仅需考虑如下平衡:
溶液中存在多个平衡。本题条件下仅需考虑如下平衡:
(i)
(ii)
 时,
时, 溶液中
溶液中 随
随 的变化关系如图。
的变化关系如图。

下列有关 溶液的说法正确的是
溶液的说法正确的是
 溶液中存在多个平衡。本题条件下仅需考虑如下平衡:
溶液中存在多个平衡。本题条件下仅需考虑如下平衡:(i)

(ii)

 时,
时, 溶液中
溶液中 随
随 的变化关系如图。
的变化关系如图。
下列有关
 溶液的说法正确的是
溶液的说法正确的是A.加入少量 溶液,反应(i)的平衡逆向移动 溶液,反应(i)的平衡逆向移动 |
B.溶液中 |
C.加入少量 固体,则平衡时 固体,则平衡时 的比值减小 的比值减小 |
D.当pH=9.0时,溶液中 的平衡浓度约为 的平衡浓度约为 |
您最近一年使用:0次
2023-05-16更新
|
330次组卷
|
4卷引用:河南省郑州市等3地2023届高三下学期6月理综化学试题
河南省郑州市等3地2023届高三下学期6月理综化学试题河北省秦皇岛市青龙满族自治县2023届高三三模联考化学试题(已下线)不定项选择题(已下线)考点2 化学平衡 (核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)
名校
9 . HA是一元弱酸,微溶性盐 的饱和溶液中
的饱和溶液中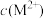 随
随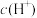 而变化,
而变化, 不发生水解。定义如下关系:
不发生水解。定义如下关系: ,
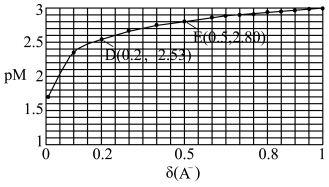
,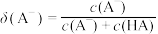 。25℃时,实验测得pM与
。25℃时,实验测得pM与 的关系如图所示,其中D点对应的
的关系如图所示,其中D点对应的 。已知
。已知 ,则下列说法不正确的是
,则下列说法不正确的是
 的饱和溶液中
的饱和溶液中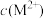 随
随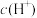 而变化,
而变化, 不发生水解。定义如下关系:
不发生水解。定义如下关系: ,
,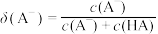 。25℃时,实验测得pM与
。25℃时,实验测得pM与 的关系如图所示,其中D点对应的
的关系如图所示,其中D点对应的 。已知
。已知 ,则下列说法不正确的是
,则下列说法不正确的是
A.25℃时,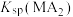 的数量级为 的数量级为 |
B.E点的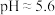 |
C.D点存在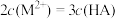 |
D.25℃时,HA的电离常数 为 为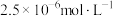 |
您最近一年使用:0次
解题方法
10 . 25℃时,苯胺(C6H5NH2)的电离平衡常数Kb=4×10-10。下列说法正确的是
A.苯胺的电离方程式为C6H5NH2+H2O=C6H5NH +OH- +OH- |
| B.分别加热浓度均为0.01mol•L-1的C6H5NH3Cl溶液和HCl溶液,两者的pH均增大 |
C.浓度为0.01mol•L-1的C6H5NH2溶液中,c(C6H5NH )>c(OH-)>c(H+) )>c(OH-)>c(H+) |
| D.等体积、等浓度的C6H5NH3Cl溶液和C6H5NH2溶液混合后,溶液呈酸性 |
您最近一年使用:0次



