1 . 碲(Te)是重要的稀有元素,被誉为“现代高新技术材料的维生素”。一种从碲化镉废料中(主要成分为CdTe、CdS、SiO2)回收Te和Cd的工艺流程如图所示。

已知:室温下,饱和H2S溶液的浓度为0.01mol·L-1, ,
, ;
; ;
; 。
。
回答下列问题:
(1)“氧化浸出”时,温度控制在80℃的原因是___________ 。“氧化浸出”过程中CdTe反应的离子方程式为___________ 。其他条件不变,双氧水与物料质量比对碲回收率的影响如图所示。质量比高于0.6时,碲回收率降低的原因是___________ 。

(2)“溶浸”过程中,若H2O2过量,将增加___________ (填化学式)的用量。“浸渣”中含有的一种单质是___________ 。
(3)“沉镉”需在酸性环境中进行的原因是___________ 。Cd2+完全沉淀时,为防止H2S气体逸出,溶液中 应控制在
应控制在___________ mol·L-1以下(离子浓度低于10-5mol·L-1视为完全沉淀)。

已知:室温下,饱和H2S溶液的浓度为0.01mol·L-1,
 ,
, ;
; ;
; 。
。回答下列问题:
(1)“氧化浸出”时,温度控制在80℃的原因是

(2)“溶浸”过程中,若H2O2过量,将增加
(3)“沉镉”需在酸性环境中进行的原因是
 应控制在
应控制在
您最近一年使用:0次
名校
解题方法
2 . 下列现象和结论均正确的是
| 选项 | 操作 | 现象 | 结论 |
| A | 等体积等浓度的MgCl2和NaOH溶液混合后,再滴加几滴FeCl3 | 先产生白色沉淀,后沉淀消失 | Fe3+水解出H+造成Mg(OH)2溶解 |
| B | 将通过灼热碎瓷片后的石蜡油蒸气通入到溴水中 | 溴水褪色 | 产物中一定含乙烯 |
| C | SO2分别通入石蕊、品红溶液 | 前者变红,后者褪色 | SO2漂白具有选择性 |
| D | 向5mL0.1mol/LK2Cr2O7溶液滴加5滴浓硫酸 | 溶液颜色由橙色变黄色 | 浓硫酸溶于水放热使平衡移动 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-12-09更新
|
540次组卷
|
4卷引用:山东省青岛市莱西市2022-2023学年高三上学期期末考试化学试题
名校
3 . 用如图所示装置(夹持装置均已省略)进行实验能达到目的的是


| A.甲装置可检验溶液中是否有K+ | B.乙装置可验证浓硫酸的脱水性 |
C.丙装置可制备无水 | D.丁装置可制取并收集干燥、纯净的NO |
您最近一年使用:0次
2022-10-12更新
|
142次组卷
|
2卷引用:山东省潍坊五县市2022-2023学年高三上学期10月质量检测联考化学试题
4 . 下列由实验现象所得结论正确的是
A.取补铁口服液的上层清液,滴加酸性 溶液,溶液紫色褪去,证明口服液中含有 溶液,溶液紫色褪去,证明口服液中含有 |
B.向盛有 的 的 溶液的小试管中滴加酚酞溶液,溶液变红,再加入少量 溶液的小试管中滴加酚酞溶液,溶液变红,再加入少量 固体,溶液红色加深,证明 固体,溶液红色加深,证明 水解程度增大 水解程度增大 |
C.向滴有酚酞的NaOH溶液中加入 ,溶液红色褪去,可证明 ,溶液红色褪去,可证明 具有酸性 具有酸性 |
D.向 溶液中通入 溶液中通入 ,再通入X气体,有白色沉淀生成,则X可能为碱性气体 ,再通入X气体,有白色沉淀生成,则X可能为碱性气体 |
您最近一年使用:0次
2022-06-07更新
|
417次组卷
|
3卷引用:山东省德州市2022届高考三模化学试题
解题方法
5 . 由下列实验操作及现象所得结论或解释正确的是
| 选项 | 实验操作 | 现象 | 结论或解释 |
| A | 将丙烯醛滴入酸性 | 紫红色变浅 | 溶液丙烯醛中含有碳碳双键 |
| B | 常温下,测定等浓度 溶液和 溶液和 溶液的pH 溶液的pH | 前者大于后者 | 得电子能力S>C |
| C | 向 固体中加入蒸馏水至固体溶解,继续加水稀释 固体中加入蒸馏水至固体溶解,继续加水稀释 | 溶液由黄绿色逐渐变为蓝色 | 溶液中存在平衡: |
| D | 向5mL  溶液中加入10mL 溶液中加入10mL  溶液,充分反应后滴加 溶液,充分反应后滴加 溶液 溶液 | 溶液变红 |  与 与 的反应是可逆反应 的反应是可逆反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
20-21高三下·山东·阶段练习
名校
解题方法
6 . 下列实验操作、实验现象及解释或结论都正确且有因果关系的是
| 选项 | 实验操作 | 实验现象 | 解释或结论 |
| A | 工业上用SiO2与焦炭在高温条件制备粗硅 | 生成可燃性气体,得到固体粗硅 | 非金属性:C>Si |
| B | 常温下,用pH计分别测定等体积1mol·L−1 CH3COONH4溶液和0.1mol·L−1 CH3COONH4溶液的pH | 测得pH都等于7 | 同温下,不同浓度的CH3COONH4溶液中水的电离程度相同 |
| C | 向两支试管中各加入4mL 0.01mol·L−1 KMnO4溶液和4mL 0.1mol·L−1 KMnO4溶液,再分别通入足量SO2,分别记录溶液褪色所需的时间 | 0.1mol·L−1 KMnO4溶液褪色所需时间更短 | 其他条件相同时,增大反应物浓度,反应速率增大 |
| D | 往烧杯中加入约20g研细的Ba(OH)2·8H2O晶体和10gNH4Cl晶体,并将烧杯放在滴有水的玻璃片上,用玻璃棒迅速搅拌 | 有刺激性气味气体生成,烧杯底部结冰,与玻璃片粘在一起 | 吸热反应不一定需要加热才能进行 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-11-16更新
|
600次组卷
|
5卷引用:学科网2021年高三3月大联考(山东卷)
(已下线)学科网2021年高三3月大联考(山东卷)山东省青岛第五十八中学2021-2022学年高三上学期期中考试化学试题河北省武邑中学2021届高三二模化学试题河北省石家庄市第二中学2021-2022学年高三上学期10月联考化学试题(已下线)第七单元 化学反应速率与化学平衡(B卷 真题滚动练)-2022年高考化学一轮复习单元滚动双测卷(新高考地区专用)
解题方法
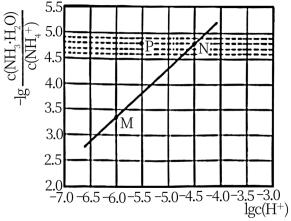
7 . 常温下,将0.1mol·L-1的 溶液加水稀释,混合溶液中
溶液加水稀释,混合溶液中 与
与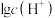 的关系如图所示。下列说法正确的是
的关系如图所示。下列说法正确的是
 溶液加水稀释,混合溶液中
溶液加水稀释,混合溶液中 与
与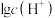 的关系如图所示。下列说法正确的是
的关系如图所示。下列说法正确的是
A.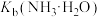 的值为10-4.7 的值为10-4.7 |
| B.M、N两点对应的溶液稀释程度N>M |
C.向溶液中加入 固体可使N点移动到P点 固体可使N点移动到P点 |
D.将溶液稀释1000倍后,溶液中 |
您最近一年使用:0次
名校
8 . 下列说法正确的是
| A.P的第一电离能与电负性均大于S |
| B.电解精炼铜时,若阳极质量减少64g,则阴极得到电子的数目为2mol |
| C.高温下,TiO2(s)+2Cl2(g)=TiCl4(g)+O2(g)∆H>0能自发进行,其原因是∆S>0 |
D.向0.1mol·L-1CH3COONa溶液中加入少量水,溶液中 减小 减小 |
您最近一年使用:0次
2021-04-30更新
|
290次组卷
|
4卷引用:山东省日照市2021届高三第二次模拟考试化学试题
山东省日照市2021届高三第二次模拟考试化学试题(已下线)押山东卷第14题 化学反应速率和平衡-备战2021年高考化学临考题号押题(山东卷)(已下线)必刷卷01-2022年高考化学考前信息必刷卷(山东专用)江苏省南京市中华中学2021届高三第二次适应性训练(选修)化学试题
10-11高三上·山东济南·阶段练习
名校
9 . 下列关于FeCl3水解的说法错误的是
| A.在FeCl3稀溶液中,水解达到平衡时,无论加FeCl3饱和溶液还是加水稀释,平衡均向右移动 |
| B.浓度为5 mol·L-1和0.5 mol·L-1的两种FeCl3溶液,其他条件相同时,Fe3+的水解程度前者小于后者 |
| C.为抑制Fe3+的水解,更好地保存FeCl3溶液,应加少量盐酸 |
| D.其他条件相同时,同浓度的FeCl3溶液在50℃和20 ℃时发生水解,50℃时Fe3+的水解程度比20℃时的小 |
您最近一年使用:0次
2021-03-10更新
|
1017次组卷
|
17卷引用:2010年山东省济南外国语学校高三上学期第二次质量检测化学卷
(已下线)2010年山东省济南外国语学校高三上学期第二次质量检测化学卷2014-2015山东省淄博市沂源一中高二12月月考化学试卷2014-2015山东省淄博市沂源县第一中学高二12月月考化学试卷(已下线)考点28 盐类的水解(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)2010年江西省新余一中 宜春中学 高安中学高二上学期第三次段考化学试卷步步为赢高二化学寒假作业 :作业九 盐类水解的应用江苏苏州市第四中学2019-2020学年高二下学期5月自学能力测试化学试题2020年北京高二下学期 复习模拟试题二(选修4人教版)人教版(2019)高二选择性必修第一册 第三章 水溶液中的离子反应与平衡 第三节 盐类的水解 教材帮陕西省宝鸡市宝鸡中学2020-2021学年高二上学期阶段考试(一)化学试题(已下线)练习11 盐类的水解-2020-2021学年【补习教材·寒假作业】高二化学(人教版)吉林省长春外国语学校2020-2021学年高二下学期期初考试化学试题(已下线)作业09 盐类的水解-2021年高二化学暑假作业(人教版2019)(已下线)3.3.2 影响盐类水解的主要因素(素养提优B练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)第三节 盐类的水解 第2课时 盐类水解的影响因素及应用吉林省乾安县第七中学2021-2022学年高二上学期第三次质量检测化学试题作业(十八) 影响盐类水解的主要因素 盐类水解的应用
解题方法
10 . 三氧化二镍(Ni2O3)是一种重要的电子元件材料和蓄电池材料。工业上利用含镍废料(镍、铁、钙、镁合金为主)制取草酸镍(NiC2O4·2H2O),再高温煅烧草酸镍制取三氧化二镍。已知草酸的钙、镁、镍盐均难溶于水,工艺流程图如图所示:
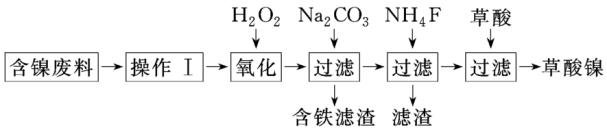
下列说法错误的是

下列说法错误的是
| A.加入H2O2发生反应的离子方程式为2Fe2++H2O2+2H+= 2Fe3++2H2O |
| B.加入碳酸钠溶液调pH至4.0~5.0,其目的为促进Fe3+水解沉淀完全 |
| C.加入NH4F得到的滤渣成分为CaF2、MgF2 |
| D.草酸镍(NiC2O4·2H2O)受热分解的产物为Ni2O3、CO2、H2O |
您最近一年使用:0次



