名校
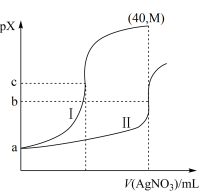
1 . 某温度下,向体积均为20.00 mL、浓度均为0.1 mol·L-1的NaCl、Na2CrO4溶液中分别滴加0.1 mol·L-1的AgNO3溶液,滴定过程中的pX(pX=-lgX,X=Cl-、CrO )与滴加AgNO3溶液体积关系如图所示(lg3=0.47)。下列说法错误的是
)与滴加AgNO3溶液体积关系如图所示(lg3=0.47)。下列说法错误的是
 )与滴加AgNO3溶液体积关系如图所示(lg3=0.47)。下列说法错误的是
)与滴加AgNO3溶液体积关系如图所示(lg3=0.47)。下列说法错误的是
| A.a=1 | B.曲线I表示NaCl溶液 |
| C.Ksp(Ag2CrO4)=1.0×10-2b | D.M约为2c-1.47 |
您最近一年使用:0次
2021-05-24更新
|
484次组卷
|
5卷引用:四川省眉山市2021届高三下学期第三次诊断性考试(5月) 化学试题
四川省眉山市2021届高三下学期第三次诊断性考试(5月) 化学试题(已下线)考点26 难溶电解质的溶解平衡-备战2022年高考化学一轮复习考点帮(全国通用)安徽省六安市第一中学2021-2022学年高三上学期第四次月考化学试题福建省厦外石狮分校、泉港一中两校联考2022-2023学年高三上学期第二次月考化学试题(已下线)题型28 沉淀溶解平衡常数及其应用图像
2 . 往含 和
和 的稀溶液中滴入
的稀溶液中滴入 溶液,产生沉淀的质量
溶液,产生沉淀的质量 (沉淀)与加入
(沉淀)与加入 溶液体积的关系如图所示。已知:
溶液体积的关系如图所示。已知: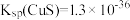 ,
,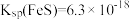 。则原溶液中
。则原溶液中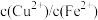 比值为
比值为
 和
和 的稀溶液中滴入
的稀溶液中滴入 溶液,产生沉淀的质量
溶液,产生沉淀的质量 (沉淀)与加入
(沉淀)与加入 溶液体积的关系如图所示。已知:
溶液体积的关系如图所示。已知: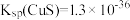 ,
,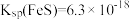 。则原溶液中
。则原溶液中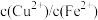 比值为
比值为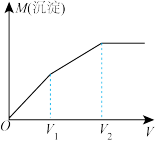
A.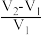 | B.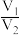 | C.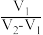 | D.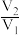 |
您最近一年使用:0次
解题方法
3 . 室温下向100mL蒸馏水中加入1gCaCO3,一段时间后再向其中加入10mL蒸馏水,一段时间后继续加入10mL蒸馏水。该过程中电导率的变化如下图:
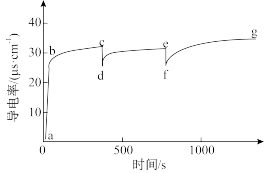
已知:室温下,CaCO3的溶解度为0.0013g。
下列说法不正确 的是

已知:室温下,CaCO3的溶解度为0.0013g。
下列说法
| A.a→b电导率上升是由于CaCO3固体部分溶解于水中 |
| B.c和e对应的时刻分别加入了10mL蒸馏水 |
| C.c→d、e→f,电导率下降,说明CaCO3的溶解平衡逆向移动 |
| D.g后的电导率几乎不再改变,说明CaCO3的溶解达到平衡状态 |
您最近一年使用:0次
2021-05-10更新
|
1128次组卷
|
8卷引用:北京市西城区2021届高三化学第二次模拟考试
北京市西城区2021届高三化学第二次模拟考试(已下线)2021年高考化学押题预测卷(北京卷)(02)广东省华附、省实、广雅、深中四校2020-2021学年高二下学期期末联考化学试题(已下线)考点26 难溶电解质的溶解平衡-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)3.4.1 沉淀溶解平衡-2021-2022学年高二化学课后培优练(人教版选修4)(已下线)专题12 水溶液中的离子平衡-备战2022年高考化学学霸纠错(全国通用)北京市师范大学亚太实验学校2021-2022学年高二上学期期中考试化学试题(已下线)第八章 水溶液中的离子反应与平衡 第52讲 难溶电解质的溶解平衡
名校
4 . 具有十八面体结构的Ag3PO4晶体是一种高效光催化剂,可用于实现“碳中和”,也可用于降解有机污染物。
Ⅰ.配位-沉淀法制备 高效光催化剂
高效光催化剂

已知:i.Ag3PO4难溶于水,可溶于硝酸;
ii.Ag3PO4沉淀的生成速率会影响其结构和形貌,从而影响其光催化性能;
iii.银氨溶液中存在: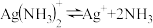
(1)配制银氨溶液时的反应现象是___________ 。
(2)加入 溶液时,发生以下反应,请将离子方程式补充完整:
溶液时,发生以下反应,请将离子方程式补充完整:
□ +□ +□ =□NH3+□ +□
+□ +□ =□NH3+□ +□ ___________
(3) 和
和 在溶液中反应也可制得Ag3PO4固体,但制得的Ag3PO4固体光催化性能极差。从速率角度解释其原因:
在溶液中反应也可制得Ag3PO4固体,但制得的Ag3PO4固体光催化性能极差。从速率角度解释其原因:___________ 。
Ⅱ.Ag3PO4光催化剂的使用和再生
已知:Ag3PO4晶体在光照条件下发挥催化作用时,首先引发反应。a.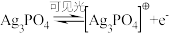
(4)Ag3PO4光催化CO2制备甲醇可实现“碳中和”,a的后续反应: ,
,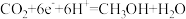 ,则由CO2制备甲醇的总反应的化学方程式为
,则由CO2制备甲醇的总反应的化学方程式为___________ 。
(5)Ag3PO4光催化降解RhB(代表有机污染物),RhB被氧化成CO2和H2O。a的后续反应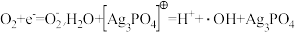
注:Ag3PO4在该催化过程中可能发生光腐蚀,生成单质银,影响其光催化性能。
用Ag3PO4依次降解三份相同的废水,测得3次降解过程中RhB的残留率(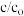 :即时浓度与起始浓度之比)随时间变化的曲线如图。
:即时浓度与起始浓度之比)随时间变化的曲线如图。

①下列说法正确的是___________ (填字母序号)。
a. 和
和 是降解RhB的重要氧化剂
是降解RhB的重要氧化剂
b.第1次使用后Ag3PO4的光催化性能降低
c.该实验条件下,Ag3PO4使用两次即基本失效
②第1次光降解时,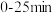 内的反应速率为
内的反应速率为___________ 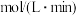 (废水中RhB初始浓度
(废水中RhB初始浓度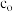 为
为 ,RhB的摩尔质量为
,RhB的摩尔质量为 )
)
Ⅰ.配位-沉淀法制备
 高效光催化剂
高效光催化剂
已知:i.Ag3PO4难溶于水,可溶于硝酸;
ii.Ag3PO4沉淀的生成速率会影响其结构和形貌,从而影响其光催化性能;
iii.银氨溶液中存在:
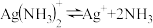
(1)配制银氨溶液时的反应现象是
(2)加入
 溶液时,发生以下反应,请将离子方程式补充完整:
溶液时,发生以下反应,请将离子方程式补充完整:□
 +□ +□ =□NH3+□ +□
+□ +□ =□NH3+□ +□ (3)
 和
和 在溶液中反应也可制得Ag3PO4固体,但制得的Ag3PO4固体光催化性能极差。从速率角度解释其原因:
在溶液中反应也可制得Ag3PO4固体,但制得的Ag3PO4固体光催化性能极差。从速率角度解释其原因:Ⅱ.Ag3PO4光催化剂的使用和再生
已知:Ag3PO4晶体在光照条件下发挥催化作用时,首先引发反应。a.
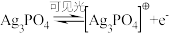
(4)Ag3PO4光催化CO2制备甲醇可实现“碳中和”,a的后续反应:
 ,
,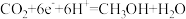 ,则由CO2制备甲醇的总反应的化学方程式为
,则由CO2制备甲醇的总反应的化学方程式为(5)Ag3PO4光催化降解RhB(代表有机污染物),RhB被氧化成CO2和H2O。a的后续反应
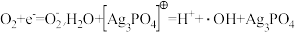
注:Ag3PO4在该催化过程中可能发生光腐蚀,生成单质银,影响其光催化性能。
用Ag3PO4依次降解三份相同的废水,测得3次降解过程中RhB的残留率(
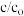 :即时浓度与起始浓度之比)随时间变化的曲线如图。
:即时浓度与起始浓度之比)随时间变化的曲线如图。
①下列说法正确的是
a.
 和
和 是降解RhB的重要氧化剂
是降解RhB的重要氧化剂b.第1次使用后Ag3PO4的光催化性能降低
c.该实验条件下,Ag3PO4使用两次即基本失效
②第1次光降解时,
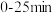 内的反应速率为
内的反应速率为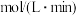 (废水中RhB初始浓度
(废水中RhB初始浓度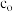 为
为 ,RhB的摩尔质量为
,RhB的摩尔质量为 )
)
您最近一年使用:0次
2021-05-10更新
|
577次组卷
|
3卷引用:北京市海淀区2021届高三二模化学试题
5 . 某品牌牙膏的成分含水、丙三醇、二氧化硅、苯甲酸钠、十二烷基硫酸钠和氟化钠等。已知:牙釉质中含有羟基磷酸钙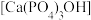 ,是牙齿的保护层。在牙齿表面存在平衡:
,是牙齿的保护层。在牙齿表面存在平衡:

下列说法不正确 的是
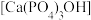 ,是牙齿的保护层。在牙齿表面存在平衡:
,是牙齿的保护层。在牙齿表面存在平衡:

下列说法
| A.若使牙膏呈弱酸性,更有利于保护牙釉质 |
| B.丙三醇的俗称是甘油 |
C. 是摩擦剂,有助于去除牙齿表面的污垢 是摩擦剂,有助于去除牙齿表面的污垢 |
D.NaF能将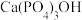 转化为更难溶的 转化为更难溶的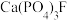 ,减少龋齿的发生 ,减少龋齿的发生 |
您最近一年使用:0次
6 . T℃时,CdCO3和Cd(OH)2的沉淀溶解平衡曲线如图所示。已知:pCd2+为Cd2+浓度的负对数,pN为阴离子浓度的负对数。下列说法正确的是
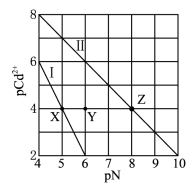

| A.溶度积的负对数:pKsp(CdCO3)< pKsp[Cd(OH)2] |
B.X点:c(Cd2+)>c(OH-),Z点:c(Cd2+)<c(CO ) ) |
| C.Y点对应的CdCO3溶液为不饱和溶液,可以继续溶解 CdCO3 |
D.T℃时,Cd(OH)2(s)+ (aq) (aq)  CdCO3(s)+2OH-(aq)的平衡常数K为103 CdCO3(s)+2OH-(aq)的平衡常数K为103 |
您最近一年使用:0次
7 . 下列化学用语正确的是
| A.氢氧化铝电离:Al(OH)3=Al3++3OH- |
| B.氯气溶于水:Cl2+H2O=2H++Cl-+ClO- |
| C.氯气与石灰乳反应制漂白粉:2Cl2+Ca2++2OH-=2Cl-+Ca(ClO)2+2H2O |
D.向Mg(OH)2悬浊液中滴酚酞后溶液变红:Mg(OH)2(s) Mg2+(aq)+2OH-(aq) Mg2+(aq)+2OH-(aq) |
您最近一年使用:0次
2021-05-03更新
|
376次组卷
|
2卷引用:北京市丰台区2021届高三第二次模拟考试化学试题
2021·辽宁·模拟预测
解题方法
8 . 向等体积pH不同的盐酸和NH4Cl溶液中加入过量镁条,溶液pH和温度随时间变化曲线如图。下列有关说法错误的是


A.在NH4Cl溶液中,P点存在:2c(Mg2+)+c(NH )>c(Cl-) )>c(Cl-) |
| B.Ksp[Mg(OH)2]=5×10-10.39 |
| C.在NH4Cl溶液中,2000~4000s温度上升是因为Mg与H2O发生反应 |
| D.在盐酸中,Q点后pH上升是因为Mg与HCl发生反应 |
您最近一年使用:0次
9 . 常温下,用AgNO3溶液分别滴定浓度均为0.01mol/L的KCl、K2C2O4溶液,所得的沉淀溶解平衡图象如图所示(不考虑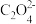 的水解)。下列叙述错误的是
的水解)。下列叙述错误的是

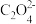 的水解)。下列叙述错误的是
的水解)。下列叙述错误的是
| A.Ksp(Ag2C2O4)的数量级等于10-11 |
| B.a点表示Ag2C2O4的不饱和溶液 |
C.向c(Cl-)=c(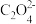 )的混合液中滴入AgNO3溶液时,先生成Ag2C2O4沉淀 )的混合液中滴入AgNO3溶液时,先生成Ag2C2O4沉淀 |
D.Ag2C2O4(s)+2Cl-(aq) ⇌2AgCl(s)+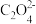 (aq)的平衡常数K=109.04 (aq)的平衡常数K=109.04 |
您最近一年使用:0次
2021-04-24更新
|
624次组卷
|
5卷引用:河南省六市(南阳市、驻马店市、信阳市、漯河市、周口市、三门峡市)2021届高三4月第二次联合调研检测理综化学试题
河南省六市(南阳市、驻马店市、信阳市、漯河市、周口市、三门峡市)2021届高三4月第二次联合调研检测理综化学试题(已下线)押全国卷理综第12题 水溶液中的离子平衡-备战2021年高考化学临考题号押题(课标全国卷)(已下线)难点6 水溶液中的四大平衡常数-2021年高考化学专练【热点·重点·难点】(已下线)专题27 难溶电解质的溶解平衡(限时精炼)-2022年高三毕业班化学常考点归纳与变式演练新疆岳普湖县2021-2022学年高二下学期第一次学情调研测试化学试题
解题方法
10 . 常温下,向20mL0.1mol·L-1BaCl2溶液中滴加0.2mol·L-1Na2CO3溶液的滴定曲线如图所示。已知:pBa=-lgc(Ba2+),pKa=-lgKa;常温下H2CO3:pKa1=6.4,pKa2=10.3。下列说法正确的是
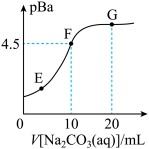

| A.常温下,Na2CO3溶液的pKh1=3.7(Kh1为一级水解常数) |
| B.常温下,Ksp(BaCO3)≈1.0×10-9 |
| C.E、F、G三点的Ksp从大到小的顺序为:G>F>E |
| D.其他条件相同,用MgCl2溶液替代BaCl2溶液,F点向G点迁移 |
您最近一年使用:0次



