1 . 已知: ,
, 均难溶于水,
均难溶于水, ,离子浓度
,离子浓度 时认为其沉淀完全。
时认为其沉淀完全。 时,
时, ,
, 的沉淀溶解平衡曲线如图所示,其中
的沉淀溶解平衡曲线如图所示,其中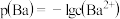 ,
,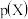
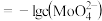 或
或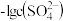 。下列叙述正确的是
。下列叙述正确的是

 ,
, 均难溶于水,
均难溶于水, ,离子浓度
,离子浓度 时认为其沉淀完全。
时认为其沉淀完全。 时,
时, ,
, 的沉淀溶解平衡曲线如图所示,其中
的沉淀溶解平衡曲线如图所示,其中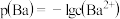 ,
,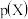
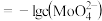 或
或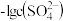 。下列叙述正确的是
。下列叙述正确的是
A. 时, 时,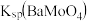 的数量级为 的数量级为 |
B. 时, 时, 点对应为 点对应为 的饱和溶液 的饱和溶液 |
C. 时, 时,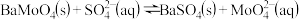 的平衡常数 的平衡常数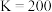 |
D. 时,向浓度均为 时,向浓度均为 的 的 和 和 的混合溶液中加入 的混合溶液中加入 溶液,当 溶液,当 恰好完全沉淀时,溶液中 恰好完全沉淀时,溶液中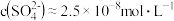 |
您最近一年使用:0次
2021-09-10更新
|
2129次组卷
|
10卷引用:江西省南昌大学附属中学2021-2022学年高二上学期期末考试化学试题
江西省南昌大学附属中学2021-2022学年高二上学期期末考试化学试题山西省运城市2022届高三上学期入学摸底测试化学试题辽宁省沈阳市第二十中学2021-2022学年高二上学期期初考试化学试题(已下线)2021年高考全国甲卷化学试题变式题2022届重庆市缙云教育联盟高三第〇次诊断性检测化学试题(已下线)专题07 电解质溶液—2022年高考化学二轮复习讲练测(全国版)-练习(已下线)押江苏卷第13题 水溶液中的离子平衡 -备战2022年高考化学临考题号押题(江苏卷)(已下线)专题22 沉淀溶解平衡及图像分析-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)巩固训练5(已下线)易错点10对沉淀溶解平衡的原理或应用理解不清而出错
名校
解题方法
2 . 利用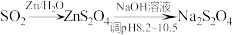 转化制取连二亚硫酸钠(
转化制取连二亚硫酸钠( )的装置如图。下列说法不正确的是
)的装置如图。下列说法不正确的是
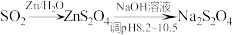 转化制取连二亚硫酸钠(
转化制取连二亚硫酸钠( )的装置如图。下列说法不正确的是
)的装置如图。下列说法不正确的是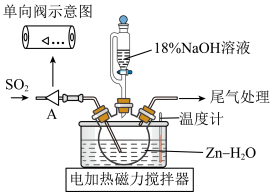
| A.单向阀的作用是防倒吸 |
B.先通入 至悬浊液变澄清,再打开滴液漏斗旋塞 至悬浊液变澄清,再打开滴液漏斗旋塞 |
C.NaOH溶液不宜加入过多的原因是防止 水解 水解 |
| D.上述反应液经过滤,在冷却搅拌下加入一定量NaCl的作用是提高产率 |
您最近一年使用:0次
2023-08-14更新
|
834次组卷
|
4卷引用:江西省赣州地区2023-2024学年十大教学能手选拔赛高中化学试题
名校
解题方法
3 . 下列实验目的、方案设计和现象、结论都正确的是
| 实验目的 | 方案设计和现象 | 结论 | |
| A | 比较KMnO4、Cl2和Fe3+的氧化性 | 向酸性KMnO4溶液中滴入FeCl2溶液,紫红色溶液变浅并伴有黄绿色气体产生 | 氧化性:KMnO4>Cl2>Fe3+ |
| B | 检验某溶液中是否含有Fe2+ | 取少量待检液于试管中,先滴加KSCN溶液,无明显变化,再滴加新制氯水,变为红色溶液 | 该溶液一定含有Fe2+ |
| C | 比较Ksp(AgCl)、Ksp(AgI)的大小 | 向NaCl、NaI混合溶液中滴入少量AgNO3溶液,有黄色沉淀生成 | Ksp(AgCl)大于Ksp(AgI) |
| D | 检验某有机物(如图)中含有醛基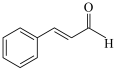 | 取少量待检液于试管中,滴加酸性KMnO4溶液,紫红色褪去 | 该有机物中含有醛基 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-09-17更新
|
1195次组卷
|
3卷引用:江西省上饶市2024届高三下学期第一次高考模拟考试化学试题
江西省上饶市2024届高三下学期第一次高考模拟考试化学试题广西壮族自治区南宁三中、柳州高中2023-2024学年高三上学期第一次适应性考试化学试题(已下线)专题03 化学实验基础-【好题汇编】2024年高考化学一模试题分类汇编(全国通用)
名校
解题方法
4 . 下列指定反应的离子方程式正确的是
A.向Ba(OH)2溶液中加入过量NH4HSO4溶液:Ba2++2OH-+NH +H++SO +H++SO =BaSO4↓+NH3·H2O+H2O =BaSO4↓+NH3·H2O+H2O |
B.向PbS固体中滴加硫酸铜溶液:Cu2++SO +PbS=CuS+PbSO4 +PbS=CuS+PbSO4 |
| C.将Fe(OH)3固体溶于氢碘酸:Fe(OH)3+3H+=Fe3++3H2O |
D.苯酚钠溶液中通入少量CO2:CO2+H2O+2C6H5O-→2C6H5OH+CO |
您最近一年使用:0次
2022-05-05更新
|
940次组卷
|
7卷引用:江西省重点中学盟校2022届高三下学期5月第二次联考理综化学试题
江西省重点中学盟校2022届高三下学期5月第二次联考理综化学试题东北育才学校超常教育实验部(少32届)2022届高三第十次模拟考试化学试题(已下线)专题03离子反应-2022年高考真题+模拟题汇编(全国卷)(已下线)专题03离子反应-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题03离子反应-五年(2018~2022)高考真题汇编(全国卷)(已下线)专题03 离子反应-三年(2020-2022)高考真题分项汇编湖南省永州市第一中学2023届高三下学期第五次月考化学试题
名校
解题方法
5 . 下列实验操作、现象和结论均正确的是
| 选项 | 操作 | 现象 | 结论 |
| A | 两块相同的未经打磨的铝片,相同温度下分别投入5.0mL等浓度的 溶液和 溶液和 溶液中 溶液中 | 前者无明显现象,后者剧烈反应 |  能加速破坏铝片表面的氧化膜 能加速破坏铝片表面的氧化膜 |
| B | 向 溶液中加入足量NaCl后再加入少量NaI溶液 溶液中加入足量NaCl后再加入少量NaI溶液 | 白色沉淀转化为淡黄色沉淀 | 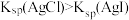 |
| C | 取少量溶液于试管中,先加入KSCN溶液,再滴加过量酸性高锰酸钾溶液 | 溶液变红色 | 溶液中含Fe2+ |
| D | 向铜与浓硫酸反应后的溶液中加入适量水稀释 | 溶液呈蓝色 | 溶液中存在 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-01-21更新
|
895次组卷
|
2卷引用:江西省宜春市丰城市2022-2023学年高二上学期期中考试化学试题
名校
解题方法
6 . 下列实验方案设计、现象和结论都正确的是
| 选项 | 实验目的 | 方案设计 | 现象和结论 |
| A | 探究反应物浓度对化学反应速率的影响 | 分别取10mL 0.1mol·Lˉ1 Na2S2O3溶液和5mL 0.1mol·Lˉ1 Na2S2O3溶液、5mL蒸馏水于两支试管中,然后同时加入10mL 0.1mol·Lˉ1H2SO4溶液 | 前者出现浑浊的时间更短,说明增大Na2S2O3浓度,可以加快反应速率 |
| B | 探究压强对化学反应速率的影响 | 在容积不变的密闭容器中发生反应:N2(g)+3H2(g) 2NH3(g),向其中通入氩气,反应速率不变 2NH3(g),向其中通入氩气,反应速率不变 | 化学反应速率不受压强影响 |
| C | 探究生成物浓度对化学平衡的影响 | 向2mL 0.1mol·L-1 FeCl3溶液加入1滴KSCN溶液,再加入少量KCl溶液 | 若溶液先变血红色,加入KCl溶液后血红色变浅,说明增大生成物浓度,平衡逆向移动 |
| D | 探究溶度积常数的大小关系 | 向盛有2mL 0.1mol/L NaOH溶液的试管中滴加4~5滴0.1mol/L MgSO4溶液,再向其中滴加0.1mol/L CuSO4溶液 | 先生成白色沉淀,后生成蓝色沉淀,说明Ksp[Mg(OH)2]>Ksp[Cu(OH)2] |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
7 . 某些难溶性铅盐可用作涂料,如秦俑彩绘中使用的铅白(PbCO3)和黄金雨中黄色的PbI2。室温下,PbCO3和PbI2在水溶液中分别达到溶解平衡时-lgc(Pb2+)与-lgc(CO )或-lgc(I-)的关系如图所示。下列说法不正确的是
)或-lgc(I-)的关系如图所示。下列说法不正确的是

 )或-lgc(I-)的关系如图所示。下列说法不正确的是
)或-lgc(I-)的关系如图所示。下列说法不正确的是
| A.室温下,Ksp(PbI2)的数量级为10-8 |
| B.P点对应的是PbI2饱和溶液 |
C.L2对应的是-lgc(Pb2+)与-lgc(CO )的关系变化 )的关系变化 |
| D.向浓度相同的Na2CO3、NaI混合溶液中逐滴加入Pb(NO3)2溶液,先产生白色沉淀 |
您最近一年使用:0次
名校
解题方法
8 . 下列实验方案合理,且能达到实验目的的是
| 选项 | 实验方案 | 实验目的 |
| A | 将乙醇与浓硫酸的混合物加热至170℃,并将产生的气体干燥后通入少量溴的四氯化碳溶液中,观察溴的四氯化碳溶液颜色的变化 | 验证乙醇发生了消去反应 |
| B | 将混有HCl杂质气体的 通入饱和食盐水中 通入饱和食盐水中 | 除去杂质HCl气体 |
| C | 分别测定相同浓度的 溶液和 溶液和 溶液的pH 溶液的pH | 比较 溶液和 溶液和 的酸性 的酸性 |
| D | 向2mL0.1mol/L 溶液中滴入几滴0.1mol/LKCl溶液,生成白色沉淀,再滴加几滴0.1mol/LKI溶液,观察沉淀颜色的变化 溶液中滴入几滴0.1mol/LKCl溶液,生成白色沉淀,再滴加几滴0.1mol/LKI溶液,观察沉淀颜色的变化 | 证明Ksp(AgCl)>Ksp(AgI) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-03-19更新
|
875次组卷
|
6卷引用:江西省南昌市2024届高三第一次模拟测试化学试卷
江西省南昌市2024届高三第一次模拟测试化学试卷江西省南昌市2024届高三下学期第一次模拟测试化学试题江西省宜春市宜丰中学2023-2024学年高三下学期3月月考化学试题2024届河南省焦作市博爱县第一中学高三下学期二模化学试题(已下线)通关练03 常考化学实验基础知识-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)(已下线)压轴题09?微型化学实验设计与评价(5大题型+方法总结+压轴题速练)-2024年高考化学压轴题专项训练(新高考通用)
名校
解题方法
9 . 下列实验操作、现象、实验结论均正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向两支盛有等浓度等体积 的试管中分别加入等浓度等体积的 的试管中分别加入等浓度等体积的 溶液和 溶液和 溶液 溶液 | 前者产生气泡速率快 |  的催化效果比 的催化效果比 好 好 |
| B | 取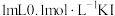 于试管中,加入 于试管中,加入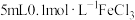 溶液,充分反应后滴入5滴15%的 溶液,充分反应后滴入5滴15%的 溶液 溶液 | 溶液变红 |  与 与 的反应有一定限度 的反应有一定限度 |
| C | 取A、B两试管,各加入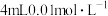 的 的 ,向A中加 ,向A中加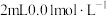 酸性高锰酸钾溶液,同时向B中加入 酸性高锰酸钾溶液,同时向B中加入 酸性高锰酸钾溶液 酸性高锰酸钾溶液 | B试管先褪为无色 | 其他条件不变时,增大反应物的浓度,反应速率加快 |
| D | 向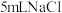 溶液中滴加2滴等浓度的 溶液中滴加2滴等浓度的 出现白色沉淀,过滤后取上层清 液又加入2滴 出现白色沉淀,过滤后取上层清 液又加入2滴 溶液 溶液 | 有黄色沉淀生成 |  |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-02-24更新
|
634次组卷
|
7卷引用:江西省抚州市临川第二中学2023-2024学年高二下学期6月月考化学试题
名校
解题方法
10 . 铊(Tl)在工业中的用途非常广泛,其中铊锡合金可作超导材料:铊镉合金是原子能工业中的重要材料。铊主要从铅精矿焙烧产生的富铊灰(主要成分PbO、ZnO、Fe2O3、 FeO、Tl2O等)中提炼,具体工艺流程如图。
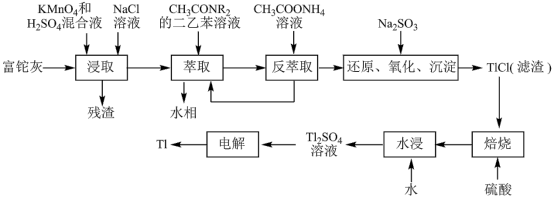
已知:萃取剂选用对铊有很高选择性的酰胺类萃取剂CH3CONR2的二乙苯溶液,萃取过程的反应原理为H+ +CH3CONR2+TlCl
 [CH3CONR2H]TlCl4。
[CH3CONR2H]TlCl4。
回答下列问题:
(1)浸取过程中硫酸的作用除了酸化提供H+,另一作用为_______ 。
(2)在实验室中,“萃取”过程使用的玻璃仪器有_______ ,用平衡移动解释“反萃取”过程的原理和目的_______ 。
(3)“还原、氧化、沉淀”过程中生成TlCl,该反应的离子方程式为_______ ,为提高经济效益充分利用原料,该反应的滤液可加入_______ 步骤循环使用最合适。
(4)Tl+对人体毒性很大,难溶盐KFe[Fe(CN)6]可通过离子交换治疗Tl2SO4中毒,将其转化为沉淀同时生成K2SO4溶液,写出治疗Tl2SO4中毒的离子方程式:_______ 。
(5)电解Tl2SO4溶液制备金属Tl的装置如图所示。石墨(C)上电极反应式为_______ 。


已知:萃取剂选用对铊有很高选择性的酰胺类萃取剂CH3CONR2的二乙苯溶液,萃取过程的反应原理为H+ +CH3CONR2+TlCl

 [CH3CONR2H]TlCl4。
[CH3CONR2H]TlCl4。回答下列问题:
(1)浸取过程中硫酸的作用除了酸化提供H+,另一作用为
(2)在实验室中,“萃取”过程使用的玻璃仪器有
(3)“还原、氧化、沉淀”过程中生成TlCl,该反应的离子方程式为
(4)Tl+对人体毒性很大,难溶盐KFe[Fe(CN)6]可通过离子交换治疗Tl2SO4中毒,将其转化为沉淀同时生成K2SO4溶液,写出治疗Tl2SO4中毒的离子方程式:
(5)电解Tl2SO4溶液制备金属Tl的装置如图所示。石墨(C)上电极反应式为

您最近一年使用:0次
2022-04-10更新
|
768次组卷
|
2卷引用:江西省八所重点中学2022届高三联考理科综合化学试题



