名校
1 . 下列对有关事实的解释正确的是
| 事实 | 解释 | |
| A | 某些金属盐灼烧呈现不同焰色 | 金属盐灼烧时发生了化学反应 |
| B | CH4与NH3分子的空间构型不同 | 二者中心原子杂化轨道类型不同 |
| C | 苯可以使溴水褪色 | 苯与溴水发生加成反应 |
| D | 向2.0mL浓度均为0.1mol/L的KCl、KI混合溶液中滴加1-2滴0.01mol/LAgNO3溶液,振荡,沉淀呈黄色 | Ksp:AgCl>AgI |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2 . 我国是世界上稀土资源最丰富的国家,冶炼提纯技术位于世界前茅。从某种磷精矿(主要成分为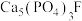 ,含少量
,含少量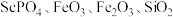 )分离稀土元素钪(
)分离稀土元素钪( )的工业流程如下:
)的工业流程如下:_______ 。
(2)“萃取”的目的是富集 ,但其余元素也会按一定比例进入萃取剂中。
,但其余元素也会按一定比例进入萃取剂中。
①通过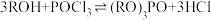 制得有机磷萃取剂
制得有机磷萃取剂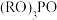 ,其中
,其中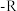 代表烃基,
代表烃基,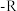 对
对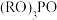 产率的影响如下表。
产率的影响如下表。
由表可知:随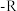 中碳原子数增加,
中碳原子数增加,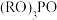 产率降低,请从结构的角度分析原因
产率降低,请从结构的角度分析原因_______ 。
②“反萃取”的目的是分离 和
和 元素。向“萃取液”中通入
元素。向“萃取液”中通入 ,
,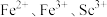 的沉淀率随
的沉淀率随 的变化如图。试剂X为
的变化如图。试剂X为_______ (填“ ”或“
”或“ ”),应调节
”),应调节 为
为_______ 。 得到
得到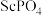 沉淀的过程为:
沉淀的过程为:
i.
ii._______ (写出该过程的化学方程式)。
(3)草酸钪晶体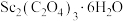 在空气中加热,
在空气中加热, 随温度的变化情况如图所示。250℃晶体主要成分是
随温度的变化情况如图所示。250℃晶体主要成分是_______ (填化学式),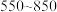 ℃反应的化学方程式为
℃反应的化学方程式为_______ 。 的一种氢化物晶胞结构如图,晶体中H周围与其最近的
的一种氢化物晶胞结构如图,晶体中H周围与其最近的 的个数为
的个数为_______ 。 为阿伏伽德罗常数的值,晶胞参数为
为阿伏伽德罗常数的值,晶胞参数为 ,则该晶胞的密度为
,则该晶胞的密度为_______  。
。
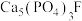 ,含少量
,含少量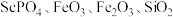 )分离稀土元素钪(
)分离稀土元素钪( )的工业流程如下:
)的工业流程如下: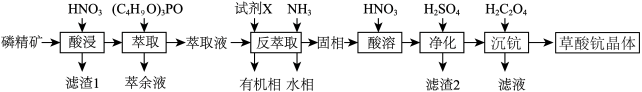
(2)“萃取”的目的是富集
 ,但其余元素也会按一定比例进入萃取剂中。
,但其余元素也会按一定比例进入萃取剂中。①通过
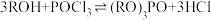 制得有机磷萃取剂
制得有机磷萃取剂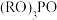 ,其中
,其中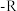 代表烃基,
代表烃基,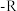 对
对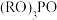 产率的影响如下表。
产率的影响如下表。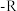 | 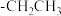 | 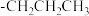 | 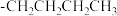 |
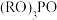 产率/ 产率/ | 82 | 62 | 20 |
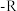 中碳原子数增加,
中碳原子数增加,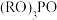 产率降低,请从结构的角度分析原因
产率降低,请从结构的角度分析原因②“反萃取”的目的是分离
 和
和 元素。向“萃取液”中通入
元素。向“萃取液”中通入 ,
, 的沉淀率随
的沉淀率随 的变化如图。试剂X为
的变化如图。试剂X为 ”或“
”或“ ”),应调节
”),应调节 为
为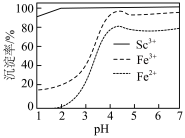
 得到
得到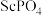 沉淀的过程为:
沉淀的过程为:i.

ii.
(3)草酸钪晶体
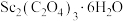 在空气中加热,
在空气中加热, 随温度的变化情况如图所示。250℃晶体主要成分是
随温度的变化情况如图所示。250℃晶体主要成分是 ℃反应的化学方程式为
℃反应的化学方程式为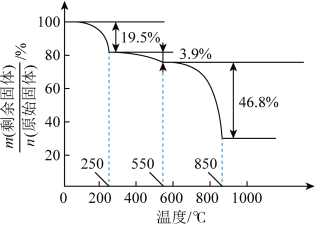
 的一种氢化物晶胞结构如图,晶体中H周围与其最近的
的一种氢化物晶胞结构如图,晶体中H周围与其最近的 的个数为
的个数为 为阿伏伽德罗常数的值,晶胞参数为
为阿伏伽德罗常数的值,晶胞参数为 ,则该晶胞的密度为
,则该晶胞的密度为 。
。
您最近一年使用:0次
2024-03-31更新
|
1083次组卷
|
4卷引用:广东省广州市天河区普通高中2023-2024学年高三毕业班综合测试(二)化学试题
广东省广州市天河区普通高中2023-2024学年高三毕业班综合测试(二)化学试题广东省佛山市三水区三水中学2024届高三下学期全真模拟考试化学试题(已下线)题型10 工艺流程题(25题)-2024年高考化学常考点必杀300题(新高考通用)(已下线)压轴题11?无机化工流程综合分析(6大题型+方法总结+压轴题速练)-2024年高考化学压轴题专项训练(新高考通用)
3 . 探究硫及其化合物的性质,下列实验操作、现象和结论都正确的是
序号 | 实验操作 | 现象 | 结论 |
A | 往装有适量蔗糖的烧杯中滴加几滴水,加入适量浓硫酸,迅速搅拌 | 蔗糖逐渐变黑,体积膨胀,并产生有刺激性气味的气体 | 浓硫酸在此过程中仅体现吸水性 |
B | 已知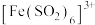 呈红棕色,往 呈红棕色,往 溶液中通入 溶液中通入 | 溶液先变红棕色,后逐渐变为浅绿色 |  与 与 反应生成 反应生成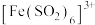 的速率比发生氧化还原反应的速率快,但氧化还原反应的平衡常数更大 的速率比发生氧化还原反应的速率快,但氧化还原反应的平衡常数更大 |
C | 往 溶液中滴加少量稀硫酸 溶液中滴加少量稀硫酸 | 产生刺激性气味的气体和黄色沉淀 | 稀硫酸在此过程中体现氧化性 |
D | 向盛有少量 溶液的试管中滴加几滴 溶液的试管中滴加几滴 溶液 溶液 | 产生黑色沉淀 |
|
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
4 . 下列实验操作能达到实验目的的是
选项 | 实验目的 | 实验操作 |
A | 比较 和 和 的水解程度 的水解程度 | 常温下,分别测浓度均为 的 的 和 和 溶液的 溶液的 |
B | 比较 与 与 的 的 即大小 即大小 | 向 溶液中滴入过量 溶液中滴入过量 溶液,再滴加 溶液,再滴加 溶液 溶液 |
C | 探究 与 与 反应是否为可逆反应 反应是否为可逆反应 | 向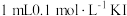 溶液中加入 溶液中加入  溶液,充分反应后滴入 溶液,充分反应后滴入 溶液 溶液 |
D | 探究 的吸氧腐蚀产物是否有 的吸氧腐蚀产物是否有 | 取少量铁电极附近溶液于试管中,滴加几滴 溶液 溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
5 . 银作为催化剂,主要用于乙烯氧化制环氧乙烷、甲醇氧化制甲醛等,通过亚硫酸钠-甲醛还原法或氨浸-水合肼还原法可回收失效的银催化剂。
回答下列问题:
(1)向银催化剂中加入稀硝酸溶解的化学方程式为____________ 。
(2)用氯化钠溶液沉淀银离子可发生下列反应:
Ⅰ.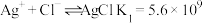
Ⅱ.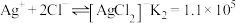
Ⅲ.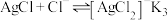
①计算
____________ (列出计算式即可)。
②根据上述平衡信息,为了使 沉淀完全,应注意控制的条件是
沉淀完全,应注意控制的条件是____________ 。
(3)亚硫酸钠-甲醛还原法浸取 的主要反应为
的主要反应为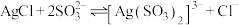 。
。
①该反应在敞口容器中进行,其他条件不变时,浸出时间过长会使银的浸出率降低,原因可能是____________ (用离子方程式表示)。
②浸出液中含银微粒总浓度随含硫微粒总浓度及浸出液 的关系如图所示:
的关系如图所示: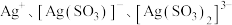 、
、 和
和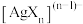 (X为
(X为 或
或 ),则含硫微粒的总浓度
),则含硫微粒的总浓度 +
+_____ +________ + ;
; 时,含银微粒总浓度随含硫微粒总浓度的变化不大,
时,含银微粒总浓度随含硫微粒总浓度的变化不大, 时,含银微粒总浓度随含硫微粒总浓度的变化较大,原因是
时,含银微粒总浓度随含硫微粒总浓度的变化较大,原因是____________ 。
(4)常温下用氨浸-水合肼还原法浸取 ,已知:
,已知: ,
, ,写出
,写出 溶于氨水发生反应的离子方程式:
溶于氨水发生反应的离子方程式:____________ ,计算该反应的平衡常数
______ (保留3位有效数字)。
回答下列问题:
(1)向银催化剂中加入稀硝酸溶解的化学方程式为
(2)用氯化钠溶液沉淀银离子可发生下列反应:
Ⅰ.
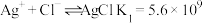
Ⅱ.
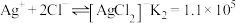
Ⅲ.
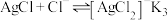
①计算

②根据上述平衡信息,为了使
 沉淀完全,应注意控制的条件是
沉淀完全,应注意控制的条件是(3)亚硫酸钠-甲醛还原法浸取
 的主要反应为
的主要反应为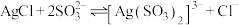 。
。①该反应在敞口容器中进行,其他条件不变时,浸出时间过长会使银的浸出率降低,原因可能是
②浸出液中含银微粒总浓度随含硫微粒总浓度及浸出液
 的关系如图所示:
的关系如图所示: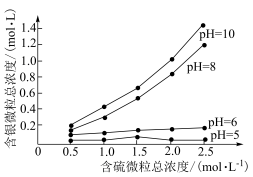
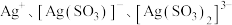 、
、 和
和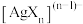 (X为
(X为 或
或 ),则含硫微粒的总浓度
),则含硫微粒的总浓度 +
+ ;
; 时,含银微粒总浓度随含硫微粒总浓度的变化不大,
时,含银微粒总浓度随含硫微粒总浓度的变化不大, 时,含银微粒总浓度随含硫微粒总浓度的变化较大,原因是
时,含银微粒总浓度随含硫微粒总浓度的变化较大,原因是(4)常温下用氨浸-水合肼还原法浸取
 ,已知:
,已知: ,
, ,写出
,写出 溶于氨水发生反应的离子方程式:
溶于氨水发生反应的离子方程式:
您最近一年使用:0次
2024-02-24更新
|
703次组卷
|
4卷引用:广东省2024届高三下学期2月份大联考 化学试题
广东省2024届高三下学期2月份大联考 化学试题广东省高州市2024届高三2月份大联考化学试题广东省揭阳华侨高级中学2023-2024学年高三下学期第二次阶段(期中)考试化学试题(已下线)大题04 化学反应原理综合题(逐空突破)-【大题精做】冲刺2024年高考化学大题突破+限时集训(新高考专用)
6 . 已知 的吸光度(A)与溶液中的
的吸光度(A)与溶液中的 成正比,其标准曲线如图所示。常温时,测得
成正比,其标准曲线如图所示。常温时,测得 饱和溶液
饱和溶液 的吸光度A=0.217,下列说法不正确的是
的吸光度A=0.217,下列说法不正确的是

 的吸光度(A)与溶液中的
的吸光度(A)与溶液中的 成正比,其标准曲线如图所示。常温时,测得
成正比,其标准曲线如图所示。常温时,测得 饱和溶液
饱和溶液 的吸光度A=0.217,下列说法不正确的是
的吸光度A=0.217,下列说法不正确的是
A.向 悬浊液中加入少量水, 悬浊液中加入少量水, 不变 不变 |
B. 饱和溶液中 饱和溶液中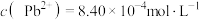 |
C. 的溶度积常数 的溶度积常数 的数量级为 的数量级为 |
D.测得40℃时 饱和溶液 饱和溶液 的吸光度A=0.343,说明 的吸光度A=0.343,说明 的溶解为吸热过程 的溶解为吸热过程 |
您最近一年使用:0次
名校
7 . 为了除去 酸性溶液中的
酸性溶液中的 ,可在加热并搅拌的条件下加入一种试剂,过滤后,再向滤液中加入适量盐酸,这种试剂是
,可在加热并搅拌的条件下加入一种试剂,过滤后,再向滤液中加入适量盐酸,这种试剂是
 酸性溶液中的
酸性溶液中的 ,可在加热并搅拌的条件下加入一种试剂,过滤后,再向滤液中加入适量盐酸,这种试剂是
,可在加热并搅拌的条件下加入一种试剂,过滤后,再向滤液中加入适量盐酸,这种试剂是A. | B. | C. | D. |
您最近一年使用:0次
8 . 已知Ksp(AgCl)=1.56×10-10、Ksp(AgBr)=7.7×10-13、Ksp(Ag2CrO4)=9×10-11,某溶液中含有Cl-、Br-和CrO ,浓度均为0.010mol/L,向该溶液中逐滴加入0.010mol/L的AgNO3溶液时,三种阴离子产生沉淀的先后顺序为
,浓度均为0.010mol/L,向该溶液中逐滴加入0.010mol/L的AgNO3溶液时,三种阴离子产生沉淀的先后顺序为
 ,浓度均为0.010mol/L,向该溶液中逐滴加入0.010mol/L的AgNO3溶液时,三种阴离子产生沉淀的先后顺序为
,浓度均为0.010mol/L,向该溶液中逐滴加入0.010mol/L的AgNO3溶液时,三种阴离子产生沉淀的先后顺序为A. Cl-、Br-、CrO | B.Br-、Cl-、CrO | C.CrO42-、Br-、Cl- | D.Br-、CrO 、Cl- 、Cl- |
您最近一年使用:0次
23-24高二上·广东深圳·期末
名校
9 . 常温下,下列有关电解质溶液的说法正确的是
| A.相同浓度的HCOONa和NaF溶液,前者的pH较大,则Ka(HCOOH)>Ka(HF) |
B.已知FeS溶于稀硫酸,而CuS不溶于稀硫酸,则 |
| C.相同浓度的CH3COOH和CH3COONa溶液等体积混合后pH约为4.7,则溶液中c(CH3COO-)>c(Na+)>c(H+)>c(OH-) |
| D.在1mol/LNa2S溶液中,c(S2-)+c(HS-)+c(H2S)=2c(Na+) |
您最近一年使用:0次
名校
10 . 沉淀溶解平衡对于定量分离沉淀时如何选择沉淀剂具有指导作用。洗涤 沉淀时,为减少沉淀损失,最恰当的洗涤剂是
沉淀时,为减少沉淀损失,最恰当的洗涤剂是
 沉淀时,为减少沉淀损失,最恰当的洗涤剂是
沉淀时,为减少沉淀损失,最恰当的洗涤剂是| A.蒸馏水 | B.饱和 溶液 溶液 | C.盐酸 | D.饱和NaCl溶液 |
您最近一年使用:0次



