1 .  是有机合成的重要催化剂,并可用于颜料、防腐等工业。工业上由废铜料(含
是有机合成的重要催化剂,并可用于颜料、防腐等工业。工业上由废铜料(含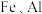 及其化合物、
及其化合物、 等杂质),生产
等杂质),生产 的工艺流程如下:
的工艺流程如下: )时的
)时的 如下表:
如下表:
② 溶液用水稀释后可生成
溶液用水稀释后可生成 沉淀。
沉淀。
(1)“酸浸”时提高浸取率的措施有___________ (写出两条)。
(2)滤渣I的主要成分是___________ (填化学式)。
(3)操作 为调节溶液的
为调节溶液的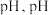 的最佳范围是
的最佳范围是___________ ,加入的物质X可以是___________ ( (填字母标号)。
A. B.
B.  C.
C.  D.
D.  溶液
溶液
(4)往滤液 中加入食盐并通入
中加入食盐并通入 可生成
可生成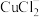 ,反应I的离子方程式为
,反应I的离子方程式为___________ ;在反应I中加入食盐并加热的目的是___________ 。
(5)实验室可以使用铜电极电解饱和食盐水得到 ,阳极的电极反应式为
,阳极的电极反应式为___________ 。
 是有机合成的重要催化剂,并可用于颜料、防腐等工业。工业上由废铜料(含
是有机合成的重要催化剂,并可用于颜料、防腐等工业。工业上由废铜料(含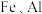 及其化合物、
及其化合物、 等杂质),生产
等杂质),生产 的工艺流程如下:
的工艺流程如下:
 )时的
)时的 如下表:
如下表:| 物质 |  |  |  |
开始沉淀时的 | 1.6 | 3.2 | 5.2 |
完全沉淀时的 | 3.1 | 4.7 | 6.7 |
 溶液用水稀释后可生成
溶液用水稀释后可生成 沉淀。
沉淀。(1)“酸浸”时提高浸取率的措施有
(2)滤渣I的主要成分是
(3)操作
 为调节溶液的
为调节溶液的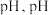 的最佳范围是
的最佳范围是A.
 B.
B.  C.
C.  D.
D.  溶液
溶液(4)往滤液
 中加入食盐并通入
中加入食盐并通入 可生成
可生成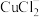 ,反应I的离子方程式为
,反应I的离子方程式为(5)实验室可以使用铜电极电解饱和食盐水得到
 ,阳极的电极反应式为
,阳极的电极反应式为
您最近一年使用:0次
2 . 常温下,CdCO3和Cd(OH)2的沉淀溶解平衡曲线如图所示。下列说法不正确的是

| A.曲线Ⅱ代表的是CdCO3的沉淀溶解平衡曲线 |
| B.X点对应的CdCO3分散系中,CdCO3沉淀速率大于溶解速率 |
| C.向Y点溶液中加入Cd(NO3)2,可使Y点移动至X点 |
| D.常温下,Cd(OH)2、CdCO3,饱和溶液中,前者c(Cd2+)更大 |
您最近一年使用:0次
3 . 常温下,PdCO3和Pd(OH)2的沉淀溶解平衡曲线如图所示。下列说法正确的是
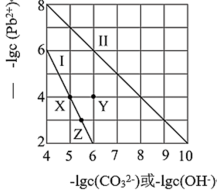
| A.向Z点对应溶液中加入适量的NaOH溶液,有可能得到X点对应溶液 |
| B.Y点对应的PdCO3分散系中,v(溶解)>v(沉淀),固体仍在溶解 |
C.PbCO3(s)+2OH-(aq) Pb(OH)2(s)+ Pb(OH)2(s)+ K=0.01 K=0.01 |
| D.由两者的Ksp可知,Pd(OH)2的溶解度更小 |
您最近一年使用:0次
名校
解题方法
4 . 碳酸锌在工业上用途广泛。利用某种浸锌渣(主要含有 )制备
)制备 的一种流程如下:
的一种流程如下: ;
;
②室温下,部分离子浓度的对数 与
与 的关系如下图所示(其中
的关系如下图所示(其中 和
和 分别代表含铝、含硅和含锌微粒):
分别代表含铝、含硅和含锌微粒):
(1)“焙烧”时,金属硫化物均转化为氧化物,生成的气体 中主要成分是
中主要成分是______ (填化学式)。
(2)“碱浸”后,浸出液中含有金属元素的离子主要是 和
和______ (填离子符号);欲使浸出液中的含锌微粒完全沉淀,应调节 的范围是
的范围是______ 。
(3)浸渣回收银的过程中有配合物 生成,在碱性条件下用
生成,在碱性条件下用 还原该配合物,还原产物为银单质,同时放出N2,该反应中氧化剂与还原剂的物质的量之比为
还原该配合物,还原产物为银单质,同时放出N2,该反应中氧化剂与还原剂的物质的量之比为______ 。
(4)“除杂”时滤渣的主要成分是______ (填化学式)。
(5)“沉锌”时发生反应的离子方程式为______ ;此过程不宜用碳酸钠代替碳酸氢铵,原因是______ 。
 )制备
)制备 的一种流程如下:
的一种流程如下: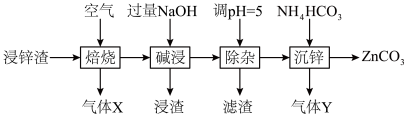
 ;
;②室温下,部分离子浓度的对数
 与
与 的关系如下图所示(其中
的关系如下图所示(其中 和
和 分别代表含铝、含硅和含锌微粒):
分别代表含铝、含硅和含锌微粒):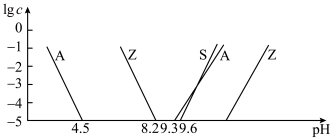
(1)“焙烧”时,金属硫化物均转化为氧化物,生成的气体
 中主要成分是
中主要成分是(2)“碱浸”后,浸出液中含有金属元素的离子主要是
 和
和 的范围是
的范围是(3)浸渣回收银的过程中有配合物
 生成,在碱性条件下用
生成,在碱性条件下用 还原该配合物,还原产物为银单质,同时放出N2,该反应中氧化剂与还原剂的物质的量之比为
还原该配合物,还原产物为银单质,同时放出N2,该反应中氧化剂与还原剂的物质的量之比为(4)“除杂”时滤渣的主要成分是
(5)“沉锌”时发生反应的离子方程式为
您最近一年使用:0次
2024-04-21更新
|
215次组卷
|
2卷引用:2024届四川省射洪中学校高三下学期二模理综试题-高中化学
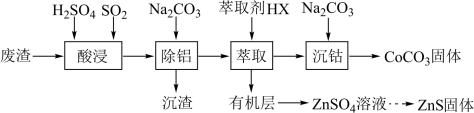
5 . CoCO3可用作选矿剂、催化剂及涂料的颜料。以含钴废渣(主要成分为CoO、Co2O3,还含有Al2O3、ZnO等杂质)为原料制备CoCO3的一种工艺流程如下:
(1)“酸浸”时需控制温度在40℃左右,原因是___________ 。
(2)“除铝”时发生反应的离子方程式为___________ 。
(3)上述“萃取”过程可表示为 。
。
①下列说法不正确的是___________ 。
A.可将废渣粉碎以提高酸浸效率
B.“除铝”时,应加入过量的Na2CO3溶液
C.可选择CCl4作为萃取剂
D.往萃取后的有机层中加水可获得ZnSO4溶液
②若萃取操作是在实验室完成,请选择合适的编号,按正确的操作顺序(有的操作可重复使用),完成萃取实验(假设只放气一次)。___________
倒入溶液和萃取剂→___________→___________→___________→___________→f→___________→___________→使下层液体慢慢流出→c→上层液体从上口倒出
a.打开分液漏斗上口玻璃塞;b.塞上分液漏斗上口玻璃塞;c.关闭分液漏斗旋塞;
d打开分液漏斗旋塞;e.倒转分液漏斗振摇;
f.将分液漏斗放在铁圈上静置;g.手持分液漏斗静置。
(4)“沉钴”时,溶液滴加过快会导致产品不纯,请解释可能原因___________ 。
(5)该工艺的副产物ZnS可参与H2S与CO2生成COS的反应,反应前后ZnS的质量不变,该过程中涉及到的化学反应有___________ 。
(6)在空气中煅烧CoCO3生成钴氧化物和CO2,测得充分煅烧后固体质量为2.41g,CO2的体积为0.672L(标准状况),则该钴氧化物的化学式为___________ 。
(1)“酸浸”时需控制温度在40℃左右,原因是
(2)“除铝”时发生反应的离子方程式为
(3)上述“萃取”过程可表示为
 。
。①下列说法不正确的是
A.可将废渣粉碎以提高酸浸效率
B.“除铝”时,应加入过量的Na2CO3溶液
C.可选择CCl4作为萃取剂
D.往萃取后的有机层中加水可获得ZnSO4溶液
②若萃取操作是在实验室完成,请选择合适的编号,按正确的操作顺序(有的操作可重复使用),完成萃取实验(假设只放气一次)。
倒入溶液和萃取剂→___________→___________→___________→___________→f→___________→___________→使下层液体慢慢流出→c→上层液体从上口倒出
a.打开分液漏斗上口玻璃塞;b.塞上分液漏斗上口玻璃塞;c.关闭分液漏斗旋塞;
d打开分液漏斗旋塞;e.倒转分液漏斗振摇;
f.将分液漏斗放在铁圈上静置;g.手持分液漏斗静置。
(4)“沉钴”时,溶液滴加过快会导致产品不纯,请解释可能原因
(5)该工艺的副产物ZnS可参与H2S与CO2生成COS的反应,反应前后ZnS的质量不变,该过程中涉及到的化学反应有
(6)在空气中煅烧CoCO3生成钴氧化物和CO2,测得充分煅烧后固体质量为2.41g,CO2的体积为0.672L(标准状况),则该钴氧化物的化学式为
您最近一年使用:0次
解题方法
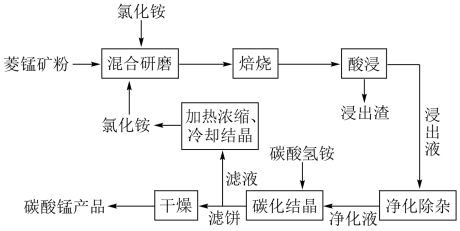
6 . 工业采用氯化铵焙烧菱锰矿制备高纯碳酸锰的流程如图所示: 其余为
其余为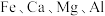 等元素。
等元素。
②部分阳离子沉淀时溶液的 :
:
③“焙烧”过程中主要反应为 。
。
(1)结合图1、2、3,分析“焙烧”过程中最佳的焙烧温度、焙烧时间、 分别为
分别为___________ 、___________ 、___________ 。 ,作用是
,作用是___________ ,再调节溶液 的范围为
的范围为___________ ,将 和
和 变为沉淀而除去,然后加入
变为沉淀而除去,然后加入 将
将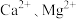 变为氟化物沉淀除去。
变为氟化物沉淀除去。
(3)“碳化结晶”步骤中,加入碳酸氢铵时反应的离子方程式为___________ 。
(4)上述流程中可循环使用的物质是___________ (填化学式)。
(5)现用滴定法测定产品中锰的含量。实验步骤:称取 试样,向其中加入稍过量的磷酸和硝酸,加热使产品中
试样,向其中加入稍过量的磷酸和硝酸,加热使产品中 完全转化为
完全转化为 (其中
(其中 转化为
转化为 );加入稍过量的硫酸铵,发生反应
);加入稍过量的硫酸铵,发生反应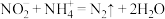 以除去
以除去 ;加入稀硫酸酸化,用
;加入稀硫酸酸化,用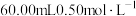 硫酸亚铁铵标准溶液进行滴定,发生的反应为
硫酸亚铁铵标准溶液进行滴定,发生的反应为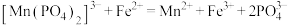 ;用
;用 酸性
酸性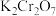 溶液恰好除去过量的
溶液恰好除去过量的 。
。
①酸性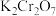 溶液与
溶液与 反应的离子方程式为
反应的离子方程式为___________ 。
②试样中锰的质量分数为___________ 。
 其余为
其余为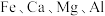 等元素。
等元素。②部分阳离子沉淀时溶液的
 :
:| 离子 |  |  |  |  |  |
开始沉淀的 | 4.1 | 2.2 | 10.6 | 8.1 | 9.1 |
沉淀完全的 | 4.7 | 3.2 | 13.1 | 10.1 | 11.1 |
 。
。(1)结合图1、2、3,分析“焙烧”过程中最佳的焙烧温度、焙烧时间、
 分别为
分别为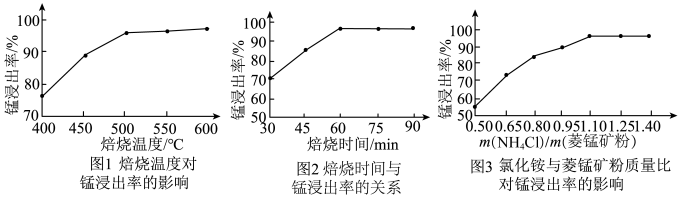
 ,作用是
,作用是 的范围为
的范围为 和
和 变为沉淀而除去,然后加入
变为沉淀而除去,然后加入 将
将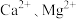 变为氟化物沉淀除去。
变为氟化物沉淀除去。(3)“碳化结晶”步骤中,加入碳酸氢铵时反应的离子方程式为
(4)上述流程中可循环使用的物质是
(5)现用滴定法测定产品中锰的含量。实验步骤:称取
 试样,向其中加入稍过量的磷酸和硝酸,加热使产品中
试样,向其中加入稍过量的磷酸和硝酸,加热使产品中 完全转化为
完全转化为 (其中
(其中 转化为
转化为 );加入稍过量的硫酸铵,发生反应
);加入稍过量的硫酸铵,发生反应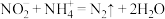 以除去
以除去 ;加入稀硫酸酸化,用
;加入稀硫酸酸化,用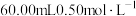 硫酸亚铁铵标准溶液进行滴定,发生的反应为
硫酸亚铁铵标准溶液进行滴定,发生的反应为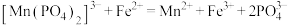 ;用
;用 酸性
酸性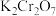 溶液恰好除去过量的
溶液恰好除去过量的 。
。①酸性
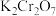 溶液与
溶液与 反应的离子方程式为
反应的离子方程式为②试样中锰的质量分数为
您最近一年使用:0次
2024-04-15更新
|
85次组卷
|
2卷引用:2024届四川省雅安市天全中学高三下学期模拟预测化学试题
7 . 某温度时, 在水溶液中的沉淀溶解平衡曲线如图所示。下列说法正确的是
在水溶液中的沉淀溶解平衡曲线如图所示。下列说法正确的是

 在水溶液中的沉淀溶解平衡曲线如图所示。下列说法正确的是
在水溶液中的沉淀溶解平衡曲线如图所示。下列说法正确的是
A.向 溶液中滴加 溶液中滴加 溶液不一定会生成沉淀 溶液不一定会生成沉淀 |
B.该温度下, 的溶度积常数 的溶度积常数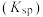 的数量级是 的数量级是 |
| C.可以通过改变温度或加入硫酸银固体使a点移动到b点 |
D.含有大量 的溶液中肯定不存在 的溶液中肯定不存在 |
您最近一年使用:0次
8 . 下列反应的离子方程式错误的是
A.用惰性电极电解氯化镁溶液:2Cl-+2H2O H2↑+Cl2↑+2OH- H2↑+Cl2↑+2OH- |
B.硫酸铵溶液显酸性: +H2O +H2O NH3•H2O+H+ NH3•H2O+H+ |
C.二元弱酸亚磷酸(H3PO3)溶液中滴加足量的NaOH溶液:H3PO3+2OH-=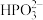 +2H2O +2H2O |
D.硫酸铜溶液遇到难溶的PbS转变为更难溶的CuS:Cu2+(aq)+ (aq)+PbS(s)=CuS(s)+PbSO4(s) (aq)+PbS(s)=CuS(s)+PbSO4(s) |
您最近一年使用:0次
2024-03-10更新
|
32次组卷
|
2卷引用:四川省绵阳中学2023-2024学年高二下学期开学化学试题
名校
解题方法
9 . 纳米铁酸锰(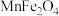 ,具有磁性)在光、电子、催化等领域应用广泛。实验室可采用共沉淀法制备纳米铁酸锰,步骤如下:
,具有磁性)在光、电子、催化等领域应用广泛。实验室可采用共沉淀法制备纳米铁酸锰,步骤如下:
步骤1:按 ,称取
,称取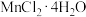 和
和 于烧杯中,加入200mL的蒸馏水,搅拌,形成混合溶液;
于烧杯中,加入200mL的蒸馏水,搅拌,形成混合溶液;
步骤2:配制浓度为 的NaOH溶液,并加热至沸腾;
的NaOH溶液,并加热至沸腾;
步骤3:将步骤1的混合液加热至80℃,剧烈搅拌下于10s内加入沸腾的130mL的NaOH溶液中,然后将该溶液倒入仪器X中回流,于90℃恒温晶化1h;
步骤4:反应结束后,将铁酸锰晶体粒子分离出来,依次用蒸馏水、乙醇洗涤干燥后,即得到黑色具有磁性的铁锰酸。
回答下列问题:
(1)步骤2所配NaOH溶液的物质的量浓度为___________  。配制过程中,下列仪器不需要用到的是
。配制过程中,下列仪器不需要用到的是___________ (填字母)。___________ 。
②回流时的加热方式为___________ 。
③写出形成铁酸锰反应的离子方程式:___________ 。
(3)步骤4分离出铁酸锰的简单方法是___________ ,检验蒸馏水将铁酸锰洗涤干净的操作是___________ ,乙醇洗涤的目的是___________ 。
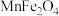 ,具有磁性)在光、电子、催化等领域应用广泛。实验室可采用共沉淀法制备纳米铁酸锰,步骤如下:
,具有磁性)在光、电子、催化等领域应用广泛。实验室可采用共沉淀法制备纳米铁酸锰,步骤如下:步骤1:按
 ,称取
,称取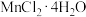 和
和 于烧杯中,加入200mL的蒸馏水,搅拌,形成混合溶液;
于烧杯中,加入200mL的蒸馏水,搅拌,形成混合溶液;步骤2:配制浓度为
 的NaOH溶液,并加热至沸腾;
的NaOH溶液,并加热至沸腾;步骤3:将步骤1的混合液加热至80℃,剧烈搅拌下于10s内加入沸腾的130mL的NaOH溶液中,然后将该溶液倒入仪器X中回流,于90℃恒温晶化1h;
步骤4:反应结束后,将铁酸锰晶体粒子分离出来,依次用蒸馏水、乙醇洗涤干燥后,即得到黑色具有磁性的铁锰酸。
回答下列问题:
(1)步骤2所配NaOH溶液的物质的量浓度为
 。配制过程中,下列仪器不需要用到的是
。配制过程中,下列仪器不需要用到的是

②回流时的加热方式为
③写出形成铁酸锰反应的离子方程式:
(3)步骤4分离出铁酸锰的简单方法是
您最近一年使用:0次
2024-01-22更新
|
110次组卷
|
4卷引用:四川省内江市第三中学2023-2024学年高三1月月考理综试卷-高中化学
10 . 某科研人员以废镍催化剂(主要成分为 ,另含
,另含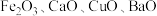 )为原料回收镍,工艺流程如图。
)为原料回收镍,工艺流程如图。 如表。
如表。
回答下列问题:
(1)浸出渣主要成分为___________ 、___________ 。(填化学式)
(2)“除铜”时, 与
与 反应的离子方程式为
反应的离子方程式为___________ 。
(3)“氧化”的目的是将溶液中 氧化为
氧化为 ,写出该反应的离子方程式
,写出该反应的离子方程式___________ 。温度需控制在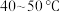 之间,该步骤温度不能太高的原因是
之间,该步骤温度不能太高的原因是___________ 。
(4)“调 ”时,
”时, 的控制范围为
的控制范围为___________ 。
(5)“除钙”后,若溶液中 浓度为
浓度为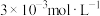 ,则
,则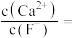
___________ 。[已知常温下, ]
]
(6)用可溶性碳酸盐,可以浸取 固体,在溶液浸取过程发生反应:
固体,在溶液浸取过程发生反应: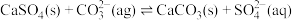 。已知:
。已知: 时,
时,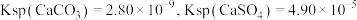 ,则此温度下该反应的平衡常数K为
,则此温度下该反应的平衡常数K为___________ (计算结果保留三位有效数字)。
 ,另含
,另含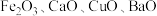 )为原料回收镍,工艺流程如图。
)为原料回收镍,工艺流程如图。
 如表。
如表。| 氢氧化物 |  |  |  |
开始沉淀的 | 1.5 | 6.5 | 7.7 |
沉淀完全的 | 3.7 | 9.7 | 9.2 |
(1)浸出渣主要成分为
(2)“除铜”时,
 与
与 反应的离子方程式为
反应的离子方程式为(3)“氧化”的目的是将溶液中
 氧化为
氧化为 ,写出该反应的离子方程式
,写出该反应的离子方程式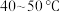 之间,该步骤温度不能太高的原因是
之间,该步骤温度不能太高的原因是(4)“调
 ”时,
”时, 的控制范围为
的控制范围为(5)“除钙”后,若溶液中
 浓度为
浓度为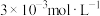 ,则
,则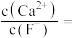
 ]
](6)用可溶性碳酸盐,可以浸取
 固体,在溶液浸取过程发生反应:
固体,在溶液浸取过程发生反应: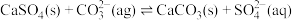 。已知:
。已知: 时,
时,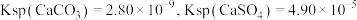 ,则此温度下该反应的平衡常数K为
,则此温度下该反应的平衡常数K为
您最近一年使用:0次
2023-09-16更新
|
868次组卷
|
4卷引用:四川省绵阳中学2023-2024学年高二下学期开学化学试题



