解题方法
1 . 下列实验操作的现象与结论均正确且具有对应关系的是
| 选项 | 实验操作 | 实验现象 | 实验结论 |
| A | 将 通入盛有酸性 通入盛有酸性 溶液的试管中 溶液的试管中 | 溶液紫红色褪去 |  有漂白性 有漂白性 |
| B | 铜片投入稀硫酸中,再加入少量硝酸钾固体 | 铜片始终无明显变化 |  不能与稀硫酸发生置换反应 不能与稀硫酸发生置换反应 |
| C | 取少量待测液于试管中,滴加几滴 溶液 溶液 | 产生白色沉淀 | 待测液中可能含有 |
| D | 向 溶液中加入过量 溶液中加入过量 溶液,再加入 溶液,再加入 溶液 溶液 | 产生黄色沉淀 | 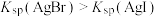 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-08-27更新
|
320次组卷
|
3卷引用:陕西省汉中市2023-2024学年高三上学期第一次联考化学试题
名校
解题方法
2 . 下列实验操作、现象和结论均正确且具有对应关系的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向FeBr2溶液中通入Cl2 | 溶液变黄 | 氧化性:Cl2>Br2 |
| B | 将石蜡油在碎瓷片上强热,产生的气体通入酸性KMnO4溶液中 | 溶液紫色褪色 | 石蜡油分解产物为乙烯 |
| C | 向CaCl2溶液中通入CO2 | 溶液变浑浊 | 生成了CaCO3 |
| D | 在试管装入2mL1mol·L-1MgCl2溶液,先滴加1mL1mol·L-1NaOH溶液,再滴加几滴1mol·L-1CuCl2溶液 | 先生成白色沉淀,后变为蓝色 | Ksp: Cu(OH)2<Mg(OH)2 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
3 . 下列表中实验操作、现象与结论对应关系正确的是
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向含有酚酞的 溶液中加入少量 溶液中加入少量 固体 固体 | 有白色沉淀生成,溶液红色变浅 | 纯碱溶液呈碱性是由 水解引起 水解引起 |
| B | 向盛有2mL NaOH溶液的试管中滴加4~5滴 NaOH溶液的试管中滴加4~5滴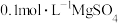 溶液,再向其中滴加 溶液,再向其中滴加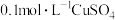 溶液 溶液 | 先生成白色沉淀,后生成蓝色沉淀 | 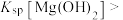  |
| C | 常温下,用玻璃棒蘸取某浓度NaOH溶液滴在湿润的pH试纸中央,与标准比色卡对比 | pH为13 | 该NaOH溶液的浓度为 |
| D | 分别取两支洁净的试管,甲试管中加入10mL 溶液,乙试管中加入5mL 溶液,乙试管中加入5mL 溶液和5mL蒸馏水,然后同时向两支试管中加入10mL 溶液和5mL蒸馏水,然后同时向两支试管中加入10mL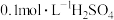 溶液 溶液 | 甲试管出现浑浊的时间更短 | 增大 浓度,可以加快反应速率 浓度,可以加快反应速率 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-01-08更新
|
88次组卷
|
2卷引用:江西省丰城中学2022-2023学年高二下学期入学考试化学试题
名校
解题方法
4 . 化学在环境污染治理中发挥了重要作用。下列治理措施与化学原理无对应关系或有误的是
| 选项 | 治理措施 | 化学原理 |
| A | 向工业废水中添加FeS以除去废水中的Cu2+ | FeS具有还原性 |
| B | 在汽车尾气系统中安装催化转化器以减少尾气污染 | CO 和NO在催化剂作用下发生反应,生成无毒气体 |
| C | 用聚酯塑料替代传统塑料以减少白色污染 | 聚酯具有生物可降解性 |
| D | 向燃煤中添加生石灰以减少酸雨的形成 | CaO具有碱性氧化物的通性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
5 . 表中实验操作、现象与结论对应关系均正确的是
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 等体积pH=2的两种酸HX和HY分别与足量的锌反应 | HX溶液中放出的H2多 | HX的酸性比HY强 |
| B | 用广泛pH试纸测定1mol/LNaHSO3溶液的酸碱性 | 测得pH=3.2 | NaHSO3溶液呈酸性,证明HSO 在水中的电离程度小于水解程度 在水中的电离程度小于水解程度 |
| C | 在KSCN与FeCl3的混合液中再加入KCl固体 | 溶液颜色变浅 | 增大生成物浓度,平衡逆向移动 |
| D | 向浓度均为0.1mol/L的NaCl和NaI的混合溶液中滴加少量0.1mol/L的AgNO3溶液 | 产生黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-03-16更新
|
680次组卷
|
8卷引用:湖南省衡阳县2022-2023学年高二上学期期末考试化学试题
湖南省衡阳县2022-2023学年高二上学期期末考试化学试题江西省宜春市宜丰中学2023-2024学年高二上学期10月月考化学试题辽宁省实验中学、大连八中、大连二十四中、鞍山一中、东北育才学校五校协作体2020-2021学年高二上学期期末化学试题黑龙江省哈尔滨市第六中学2021-2022学年高二上学期期末考试化学试题湖南省永州市宁远县第一中学2022-2023学年高二上学期期中考试化学试题广东省江门市培英高级中学2022-2023学年高二上学期期中考试化学试题江西省临川第二中学2022-2023学年高二上学期第三次月考化学试题广东省梅州市兴宁市沐彬中学2021-2022学年高二下学期期中考试化学试题
名校
解题方法
6 . 铬和钒具有广泛用途。铬钒渣中铬和钒以低价态含氧酸盐形式存在,主要杂质为铁、铝、硅、磷等的化合物,从铬钒渣中分离提取铬和钒的一种流程如下图所示:
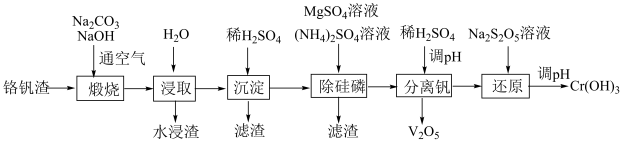
已知:最高价铬酸根在酸性介质中以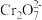 存在,在碱性介质中以
存在,在碱性介质中以 存在。
存在。
回答下列问题:
(1)煅烧过程中,钒和铬被氧化为相应的最高价含氧酸盐,其中含铬化合物主要为___________ 。(填化学式)。
(2)水浸渣中主要有 和
和___________ 。
(3)“除硅磷”步骤中,使硅、磷分别以 和
和 的形式沉淀,该步需要控制溶液的
的形式沉淀,该步需要控制溶液的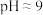 以达到最好的除杂效果,其原因是
以达到最好的除杂效果,其原因是___________ 。
(4)“还原”步骤中加入焦亚硫酸钠( )溶液。
)溶液。
①写出 还原
还原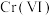 的离子方程式:
的离子方程式:___________ 。
②若用过氧化氢还原 过程中还会生成较稳定的蓝色的过氧化铬(
过程中还会生成较稳定的蓝色的过氧化铬( ,
, 为+6价)。
为+6价)。 分子中存在过氧键,其结构式可表示为
分子中存在过氧键,其结构式可表示为___________ 。
(5)为研究净水剂聚合硫酸铁 组成,某化学兴趣小组取一定量聚合硫酸铁样品与足量盐酸反应,所得溶液平均分为两份。一份溶液中加入足量的
组成,某化学兴趣小组取一定量聚合硫酸铁样品与足量盐酸反应,所得溶液平均分为两份。一份溶液中加入足量的 溶液,得到白色沉淀
溶液,得到白色沉淀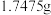 。另一份溶液,先将
。另一份溶液,先将 还原为
还原为 ,再用
,再用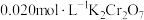 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗 标准溶液
标准溶液 。求
。求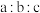 值
值___________ 。(写出计算过程)(已知: 。)
。)

已知:最高价铬酸根在酸性介质中以
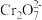 存在,在碱性介质中以
存在,在碱性介质中以 存在。
存在。回答下列问题:
(1)煅烧过程中,钒和铬被氧化为相应的最高价含氧酸盐,其中含铬化合物主要为
(2)水浸渣中主要有
 和
和(3)“除硅磷”步骤中,使硅、磷分别以
 和
和 的形式沉淀,该步需要控制溶液的
的形式沉淀,该步需要控制溶液的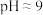 以达到最好的除杂效果,其原因是
以达到最好的除杂效果,其原因是(4)“还原”步骤中加入焦亚硫酸钠(
 )溶液。
)溶液。①写出
 还原
还原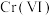 的离子方程式:
的离子方程式:②若用过氧化氢还原
 过程中还会生成较稳定的蓝色的过氧化铬(
过程中还会生成较稳定的蓝色的过氧化铬( ,
, 为+6价)。
为+6价)。 分子中存在过氧键,其结构式可表示为
分子中存在过氧键,其结构式可表示为(5)为研究净水剂聚合硫酸铁
 组成,某化学兴趣小组取一定量聚合硫酸铁样品与足量盐酸反应,所得溶液平均分为两份。一份溶液中加入足量的
组成,某化学兴趣小组取一定量聚合硫酸铁样品与足量盐酸反应,所得溶液平均分为两份。一份溶液中加入足量的 溶液,得到白色沉淀
溶液,得到白色沉淀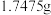 。另一份溶液,先将
。另一份溶液,先将 还原为
还原为 ,再用
,再用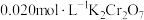 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗 标准溶液
标准溶液 。求
。求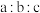 值
值 。)
。)
您最近一年使用:0次
解题方法
7 . 某小组同学探究盐对Fe3+ +3SCN- Fe(SCN)3平衡体系的影响。
Fe(SCN)3平衡体系的影响。
实验I:探究KCl对Fe3+和SCN-平衡体系的影响
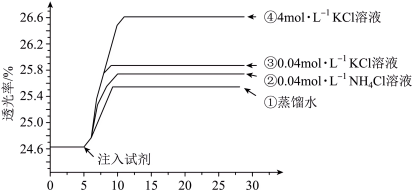
将已用稀盐酸酸化的0.005 mol·L-1 FeCl3溶液和0.01 mol·L-1 KSCN溶液等体积混合,静置至体系平衡,得红色溶液X,分别取3 mL溶液X放入比色皿中,分别滴加0.1 mL的试剂①~④,并测定各溶液的透光率随时间的变化,结果如图所示。
已知:i.Cl-与Fe3+能发生络合反应:Fe3+ +4C1- [FeCl4]-(黄色);
[FeCl4]-(黄色);
ii.Fe3+与NO 不能形成配位化合物;
不能形成配位化合物;
iii.溶液的透光率与溶液颜色深浅有关,颜色越深,透光率越低,忽略[FeCl4]-对透光率的影响。
(1)本实验配制溶液时用到的玻璃仪器除烧杯、量筒、玻璃棒、容量瓶外,还需要___________ ,用稀盐酸酸化FeCl3溶液的目的是___________ 。
(2)注入试剂①后溶液透光率升高,甲同学认为是溶液稀释导致颜色变浅,乙同学认为还可能是稀释的过程中,Fe3+ +3SCN- Fe(SCN)3平衡向
Fe(SCN)3平衡向___________ (填“正”或“逆”)反应方向移动。
(3)注入试剂④后的溶液透光率比注入试剂①后高,结合平衡移动原理分析其原因___________ 。
(4)注入试剂③后的溶液透光率比注入试剂②后高,可能是___________ 导致的(答出一种影响因素即可,不需详细说明理由)。
实验II:探究不同盐对Fe3+和SCN-平衡体系的影响
取2 mL溶液X,分别加入下列试剂进行实验,一段时间后测得各溶液的透光率如下表。
(5)丙同学发现A3>A2>A1,查阅资料认为可能的原因:溶液中的离子会受到周围带有异性电荷离子的屏蔽,使该离子的有效浓度降低,这种影响称为盐效应。推断盐效应较强的金属阳离子为___________ (填离子符号),试分析该离子盐效应对Fe3+和SCN-平衡体系有影响的原因___________ 。
(6)拓展应用:盐效应对多种平衡体系有影响。
分析c(Na2SO4)在0~0.20 mol·L-1范围内,PbSO4溶解度发生变化的原因:___________ 。
(7)FeCl3用途十分广泛,请写出一种其在生活中的用途___________ 。
 Fe(SCN)3平衡体系的影响。
Fe(SCN)3平衡体系的影响。实验I:探究KCl对Fe3+和SCN-平衡体系的影响
将已用稀盐酸酸化的0.005 mol·L-1 FeCl3溶液和0.01 mol·L-1 KSCN溶液等体积混合,静置至体系平衡,得红色溶液X,分别取3 mL溶液X放入比色皿中,分别滴加0.1 mL的试剂①~④,并测定各溶液的透光率随时间的变化,结果如图所示。

已知:i.Cl-与Fe3+能发生络合反应:Fe3+ +4C1-
 [FeCl4]-(黄色);
[FeCl4]-(黄色);ii.Fe3+与NO
 不能形成配位化合物;
不能形成配位化合物;iii.溶液的透光率与溶液颜色深浅有关,颜色越深,透光率越低,忽略[FeCl4]-对透光率的影响。
(1)本实验配制溶液时用到的玻璃仪器除烧杯、量筒、玻璃棒、容量瓶外,还需要
(2)注入试剂①后溶液透光率升高,甲同学认为是溶液稀释导致颜色变浅,乙同学认为还可能是稀释的过程中,Fe3+ +3SCN-
 Fe(SCN)3平衡向
Fe(SCN)3平衡向(3)注入试剂④后的溶液透光率比注入试剂①后高,结合平衡移动原理分析其原因
(4)注入试剂③后的溶液透光率比注入试剂②后高,可能是
实验II:探究不同盐对Fe3+和SCN-平衡体系的影响
取2 mL溶液X,分别加入下列试剂进行实验,一段时间后测得各溶液的透光率如下表。
| 序号 | 加入试剂 | 溶液透光率 |
| 1 | 1 mL蒸馏水 | A1 |
| 2 | 1 mL 3 mol·L-1 KNO3 | A2 |
| 3 | 1 mL 3 mol·L-1 NaNO3 | A3 |
(5)丙同学发现A3>A2>A1,查阅资料认为可能的原因:溶液中的离子会受到周围带有异性电荷离子的屏蔽,使该离子的有效浓度降低,这种影响称为盐效应。推断盐效应较强的金属阳离子为
(6)拓展应用:盐效应对多种平衡体系有影响。
| c(Na2SO4)/(mol·L-1) | 0 | 0.01 | 0.02 | 0.04 | 0.10 | 0.20 |
| PbSO4溶解度/mg | 4.5 | 0.48 | 0.42 | 0.39 | 0.48 | 0.69 |
(7)FeCl3用途十分广泛,请写出一种其在生活中的用途
您最近一年使用:0次
名校
解题方法
8 . 铬和钒具有广泛用途。铬钒渣中铬和钒以低价态含氧酸盐形式存在,主要杂质为铁、铝、硅等的氧化物,从铬钒渣中分离提取铬和钒的一种流程如图所示。下列说法正确的是
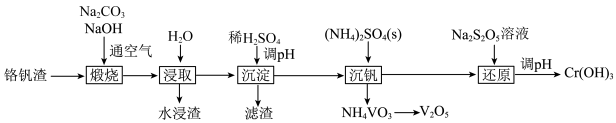
已知:①“煅烧”时铬、铝和硅的氧化物均转化为可溶性钠盐:
② 。
。

已知:①“煅烧”时铬、铝和硅的氧化物均转化为可溶性钠盐:
②
 。
。A.“煅烧”后的含铬化合物是 |
B.“滤渣”中只含有 |
C.“沉钒”时 固体可增大 固体可增大 的浓度,有利于沉淀的生成 的浓度,有利于沉淀的生成 |
D.“还原”工序中氧化剂和还原剂的物质的量之比为 |
您最近一年使用:0次
2023-12-03更新
|
373次组卷
|
2卷引用:山东省菏泽市2023-2024学年高三上学期期中化学试题
名校
9 . 下列物质的用途或事实与盐类的水解无关的是
A.用 溶液处理锅炉水垢中的 溶液处理锅炉水垢中的 |
B.明矾[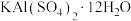 ]用于净水 ]用于净水 |
C.用热饱和 溶液清洗试管壁上附着的植物油 溶液清洗试管壁上附着的植物油 |
D.由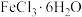 制取无水 制取无水 固体时,需在HCl气流中蒸发 固体时,需在HCl气流中蒸发 |
您最近一年使用:0次
2023-11-29更新
|
312次组卷
|
3卷引用:北京师范大学附属实验中学2023-2024学年高二上学期期中考试化学试题
解题方法
10 . 生活因化学更美好,以下生活用途和化学原理错误的是
选项 | 生活用途 | 化学原理 |
| A | 明矾可用作净水剂和消毒剂 | 铝离子水解生成氢氧化铝胶体 |
| B | 含氟牙膏可以预防龋齿 | 沉淀的转化 |
| C | 电热水器内胆连接镁棒防止腐蚀 | 牺牲阳极法 |
| D | 泡沫灭火器可以灭火 | 盐类的水解 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



