1 . T℃时,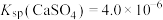 、
、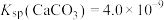 、
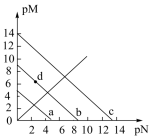
、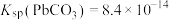 ,三种盐的沉淀溶解平衡曲线如图所示,
,三种盐的沉淀溶解平衡曲线如图所示, (阴离子)、
(阴离子)、 (阳离子)。下列说法错误的是
(阳离子)。下列说法错误的是
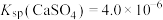 、
、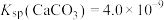 、
、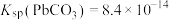 ,三种盐的沉淀溶解平衡曲线如图所示,
,三种盐的沉淀溶解平衡曲线如图所示, (阴离子)、
(阴离子)、 (阳离子)。下列说法错误的是
(阳离子)。下列说法错误的是
A.a线是 沉淀溶解平衡曲线 沉淀溶解平衡曲线 |
B.除去锅炉水垢中 ,可先用碳酸钠溶液处理,使 ,可先用碳酸钠溶液处理,使 转化为 转化为 ,然后用酸除去 ,然后用酸除去 |
C.T℃时,向 水中加入 水中加入 和 和 至二者均饱和,溶液中 至二者均饱和,溶液中 |
D.若d点表示 的饱和溶液加入 的饱和溶液加入 饱和溶液等体积混合则: 饱和溶液等体积混合则: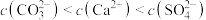 |
您最近一年使用:0次
名校
2 . 下列实验操作、现象与结论均正确的是
| 选项 | 操作 | 现象 | 结论 |
| A | 向盛有2mL0.5mol/L的AgNO3溶液中先滴加2滴0.1mol/L的NaCl溶液,再滴加2滴0.1mol/L的KI溶液 | 先出现白色沉淀,后沉淀变为黄色 | Ksp(AgCl)>Ksp(AgI) |
| B | 向盛有少量Mg(OH)2沉淀的试管中加入适量饱和CH3COONH4溶液,振荡 | 白色沉淀溶解 | NH 结合了Mg(OH)2电离出的OH-,促使了Mg(OH)2的溶解平衡正向移动 结合了Mg(OH)2电离出的OH-,促使了Mg(OH)2的溶解平衡正向移动 |
| C | 用玻璃棒蘸取NaHCO3溶液点在pH试纸上 | 试纸变红 | HCO 的电离程度大于其水解程度 的电离程度大于其水解程度 |
| D | 琼脂溶液中滴加5-6滴酚酞和K3[Fe(CN)6]溶液,倒入培养皿中,将中间裹有锌皮的铁钉放入其中,铁钉两端均外露,观察铁钉两端有无蓝色沉淀生成 | 铁钉两端有蓝色沉淀生成 | 验证牺牲阳极法对铁钉的保护效果 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
3 . 已知常温下, ,
, ,下列叙述中正确的是
,下列叙述中正确的是
 ,
, ,下列叙述中正确的是
,下列叙述中正确的是A.向AgI与AgCl的悬浊液中加入几滴浓NaCl溶液,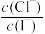 不变 不变 |
B.常温下,AgCl在NaCl溶液中的 比在纯水中的 比在纯水中的 小 小 |
| C.将0.001 mol·L-1的AgNO3溶液滴入KCl和KI的混合溶液中,一定先析出AgI沉淀 |
D.向AgCl饱和溶液中加入NaCl晶体,有AgCl析出且溶液中 |
您最近一年使用:0次
4 . 已知:Ksp(BaSO4)=1.1×10-10,Ksp(CaSO4)=4.9×10-5,若要除去粗盐溶液中的 ,下列说法中,
,下列说法中,不正确 的是
 ,下列说法中,
,下列说法中,| A.沉淀剂的选择要考虑阴离子的种类 |
B.钡盐除 比钙盐更好 比钙盐更好 |
C.为使 沉淀完全,沉淀剂应加至稍过量 沉淀完全,沉淀剂应加至稍过量 |
D.加入足够多沉淀剂后, 浓度可以降至0 浓度可以降至0 |
您最近一年使用:0次
5 . 如图所示进行实验,下列分析错误的是


| A.②中黄色沉淀变成黑色沉淀 |
| B.该实验可以说明溶度积Ksp(AgI)>Ksp(Ag2S) |
| C.反应后的溶液中c(Ag+):①<② |
| D.②中反应为:2AgI(s)+S2−(aq)⇌Ag2S(s)+2I−(aq) |
您最近一年使用:0次
6 . 一定温度下, 和
和 (砖红色)的沉淀溶解平衡曲线如图所示,下列说法正确的是
(砖红色)的沉淀溶解平衡曲线如图所示,下列说法正确的是

 和
和 (砖红色)的沉淀溶解平衡曲线如图所示,下列说法正确的是
(砖红色)的沉淀溶解平衡曲线如图所示,下列说法正确的是
A.曲线M为 的沉淀溶解平衡曲线 的沉淀溶解平衡曲线 |
B.X点条件下可以同时生成 和 和 沉淀 沉淀 |
C.该温度下, 的数量级为 的数量级为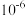 |
D.用 标准溶液滴定 标准溶液滴定 溶液中的 溶液中的 ,可以用 ,可以用 作指示剂 作指示剂 |
您最近一年使用:0次
名校
7 . 某温度下,向10mL0.1mol·L−1Pb(NO3)2溶液中滴加0.1mol·L−1Na2S溶液,溶液中-lgc(Pb2+)与滴加的Na2S溶液体积V的关系如图所示(忽略体积变化)。已知:Ksp(PbS)<Ksp(FeS)。下列判断正确的是


| A.a、b、c三点中Ksp(PbS)从大到小的顺序为:a>b>c |
| B.b点:c(Pb2+)<c(S2−) |
| C.c点:2c(Pb2+)+c(H+)=c(NO3−)+c(OH−) |
| D.其他条件相同时,若将Pb(NO3)2溶液换成同浓度、同体积的Fe(NO3)2溶液,图中-lgc(Pb2+)换成-lgc(Fe2+),则b点会沿虚线向下移动 |
您最近一年使用:0次
2024-01-18更新
|
265次组卷
|
3卷引用:四川省成都市蓉城名校2023-2024学年高二上学期期末联考化学试题
四川省成都市蓉城名校2023-2024学年高二上学期期末联考化学试题江西省宜春市宜丰中学2023-2024学年高三上学期1月月考化学试题(已下线)专题07 水溶液中的离子反应与平衡-【好题汇编】2024年高考化学一模试题分类汇编(新高考七省专用)
名校
解题方法
8 . 下列说法中正确的是
A. 的溶液中: 的溶液中: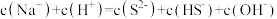 |
B.浓度均为 的① 的① ② ② ③ ③ ④ ④ , , 由小到大的顺序:④<③<①<② 由小到大的顺序:④<③<①<② |
C.向 、 、 的混合饱和溶液中加入少量 的混合饱和溶液中加入少量 ,溶液中 ,溶液中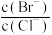 减小 减小 |
D. 溶液中离子浓度大小顺序为 溶液中离子浓度大小顺序为 |
您最近一年使用:0次
2024-01-15更新
|
264次组卷
|
2卷引用:广东省深圳市罗湖高级中学2023-2024学年高二上学期12月阶段性考试化学试题
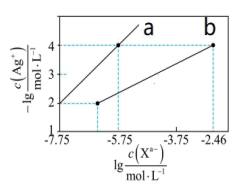
9 . 常温下,用AgNO3溶液分别滴定浓度均为0.0lmol/L的KCl、K2C2O4溶液,所得的沉淀溶解平衡图像如图所示(不考虑 的水解)。下列叙述正确的是
的水解)。下列叙述正确的是
 的水解)。下列叙述正确的是
的水解)。下列叙述正确的是
| A.b表示AgCl的沉淀溶解平衡图像 |
| B.Ksp(Ag2C2O4)的数量级等于10-10 |
C.向c(Cl-)=c( )的混合液中滴入AgNO3溶液时,先生成Ag2C2O4沉淀 )的混合液中滴入AgNO3溶液时,先生成Ag2C2O4沉淀 |
D.Ag2C2O4(s)+2Cl-(l) 2AgCl(s)+ 2AgCl(s)+ (aq)的平衡常数为109.04 (aq)的平衡常数为109.04 |
您最近一年使用:0次
名校
解题方法
10 . 表中实验操作、现象与结论对应关系均正确的
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 取2mL0.lmol/LAgNO3溶液,先后滴加3滴0.lmol/LNaCl溶液和6滴0.lmol/LKI溶液,观察沉淀情况 | 先产生白色沉淀,后产生黄色沉淀 | Ksp(AgCl)大于Ksp(AgI) |
| B | 等体积pH=2的两种酸HX和HY分别与足量的锌反应 | HX溶液中放出的H2多 | HX的酸性比HY弱 |
| C | 在KSCN与FeCl3的混合液中再加入KCl固体 | 溶液颜色变浅 | 增大生成物浓度,平衡逆向移动 |
| D | 用广泛pH试纸测定1mol/LNaHSO3溶液的酸碱性 | 测定pH=3.2 | NaHSO3溶液呈酸性,证明 在水中的电离程度大于水解程度 在水中的电离程度大于水解程度 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



