名校
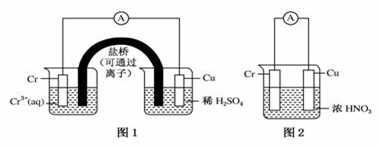
1 . 用如图装置进行实验(A为电流计):
观察到现象:
装置图1:Cu电极上产生大量的无色气泡
装置图2:Cu电极上无气泡产生,而Cr电极上产生大量气泡
则下列说法正确的是

观察到现象:
装置图1:Cu电极上产生大量的无色气泡
装置图2:Cu电极上无气泡产生,而Cr电极上产生大量气泡
则下列说法正确的是
| A.图1是电解池,图2是原电池 |
| B.两个电池中,电子均由Cr电极流向Cu电极 |
| C.图2中Cr电极可能被浓HNO3钝化成惰性电极 |
| D.由实验现象可知金属活动性:Cu>Cr |
您最近一年使用:0次
2018-05-21更新
|
389次组卷
|
4卷引用:河北省唐山一中2017-2018学年高一下学期期中考试化学试题
名校
2 . 回答下列问题
(1)已知完全燃烧ag乙炔(C2H2)气体时生成1molCO2和H2O(l),同时放出热量bkJ,则表示乙炔燃烧热的热化学方程式:_____ 。
(2)某课外科学兴趣小组的同学用如图所示装置研究有关电化学的问题。图中是两个串联的甲烷燃料电池做电源对乙池丙池进行电解实验(各溶液溶质均足量),当闭合该装置的电键时,观察到电流表的指针发生了偏转。

①A电极上发生的电极反应式为:____ 。
②电解过程中丙池中发生的总反应方程式为:____ 。
③当两个燃料电池共消耗甲烷2240mL(标况),乙池中某极上析出Ag的质量为_____ g。
(3)如图所示是一种可实现氢气循环利用的新型电池的放电工作原理。

若以此新型电池为电源,用惰性电极电解制备硼酸[H3BO3或B(OH)3],其工作原理如图所示(阳膜和阴膜分别只允许阳离子和阴离子通过)。

①新型电池放电时,负极电极反应式为:____ 。
②两池工作时,电池的电极M应与电解池的____ (填a或b)极相连接;1、2、3膜为阳膜的是:____ 。
③产品室中发生的离子反应为:____ 。
(1)已知完全燃烧ag乙炔(C2H2)气体时生成1molCO2和H2O(l),同时放出热量bkJ,则表示乙炔燃烧热的热化学方程式:
(2)某课外科学兴趣小组的同学用如图所示装置研究有关电化学的问题。图中是两个串联的甲烷燃料电池做电源对乙池丙池进行电解实验(各溶液溶质均足量),当闭合该装置的电键时,观察到电流表的指针发生了偏转。

①A电极上发生的电极反应式为:
②电解过程中丙池中发生的总反应方程式为:
③当两个燃料电池共消耗甲烷2240mL(标况),乙池中某极上析出Ag的质量为
(3)如图所示是一种可实现氢气循环利用的新型电池的放电工作原理。

若以此新型电池为电源,用惰性电极电解制备硼酸[H3BO3或B(OH)3],其工作原理如图所示(阳膜和阴膜分别只允许阳离子和阴离子通过)。

①新型电池放电时,负极电极反应式为:
②两池工作时,电池的电极M应与电解池的
③产品室中发生的离子反应为:
您最近一年使用:0次
2022-10-08更新
|
475次组卷
|
2卷引用:河北省邢台市六校2022-2023学年高三上学期第一次月考化学试题
名校
解题方法
3 . 己二腈 是工业制造尼龙
是工业制造尼龙 的原料,现代工业常用电有机合成法制备,总反应为
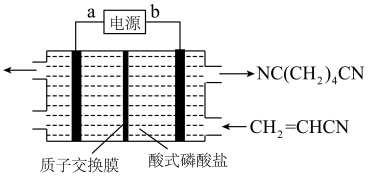
的原料,现代工业常用电有机合成法制备,总反应为 ,装置如图所示。下列说法错误的是
,装置如图所示。下列说法错误的是
 是工业制造尼龙
是工业制造尼龙 的原料,现代工业常用电有机合成法制备,总反应为
的原料,现代工业常用电有机合成法制备,总反应为 ,装置如图所示。下列说法错误的是
,装置如图所示。下列说法错误的是
| A.b为电源的负极 |
B.阳极的电极反应为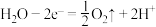 |
C.当电路中转移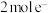 时,阳极室溶液质量减少16 g 时,阳极室溶液质量减少16 g |
D.阴极的电极反应为: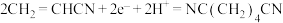 |
您最近一年使用:0次
2023-02-20更新
|
256次组卷
|
3卷引用:河北省石家庄市新乐市第一中学2022-2023学年高二上学期期末考试化学试题
河北省石家庄市新乐市第一中学2022-2023学年高二上学期期末考试化学试题【定心卷】4.2.2 电解原理的应用随堂练习 -人教版2023-2024学年选择性必修1(已下线)专题10 电解池 金属的腐蚀与防护-【好题汇编】备战2023-2024学年高二化学上学期期末真题分类汇编(人教版2019)
名校
解题方法
4 . 利用CH4燃料电池电解制备Ca(H2PO4)2并得到副产物NaOH、H2、Cl2,装置如图所示。下列说法不正确的是


| A.a极的电极反应式为:CH4-8e-+4O2-=CO2+2H2O |
| B.A膜和C均为阳离子交换膜 |
| C.可用铁电极替换Y极室的石墨电极 |
| D.a极上通入2.24L(标准状况)甲烷,X极室Ca2+减少0.8mol |
您最近一年使用:0次
名校
解题方法
5 . 盐酸羟胺(NH3OHCl)是一种常见的还原剂和显像剂,其化学性质类似NH4Cl。工业上主要采用图1所示的方法制备。其电池装置中含Fe的催化电极反应机理如图2所示。不考虑溶液体积变化,下列说法正确的是
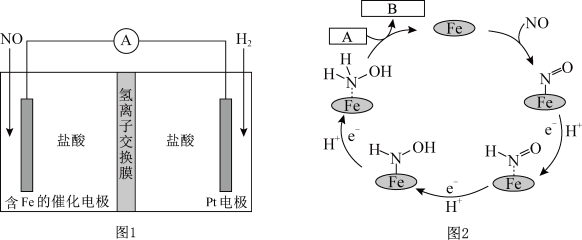

| A.电池工作时,Pt电极是正极 |
| B.图2中,A为H+和e-,B为NH3OH+ |
| C.电池工作时,每消耗2.24LNO(标准状况下),左室溶液质量增加3.3g |
| D.电池工作一段时间后,正、负极区溶液的pH均下降 |
您最近一年使用:0次
2022-04-20更新
|
2127次组卷
|
14卷引用:河北省石家庄市第二中学2022届高三下学期5月模拟考试化学试题
河北省石家庄市第二中学2022届高三下学期5月模拟考试化学试题福建省福州市2022届高中毕业班(3月)第二次质量检测化学试题湖南省大联考雅礼十六校2021-2022学年高三第二次联考化学试题(已下线)秘籍12 原电池原理及应用-备战2022年高考化学抢分秘籍(全国通用)江苏省南京市第十三中学2022届高三下学期适应性考试化学试题江苏省南京市雨花台中学2022-2023学年高二上学期10月月考化学试题湖南省郴州市2023届高三下学期第三次教学质量监测化学试题江苏省镇江中学2022-2023学年高一下学期期中考试化学试题湖南省常德市第一中学2022-2023学年高三下学期5月月考化学试题江苏省常州市第一中学2022-2023学年高一下学期期末测试化学试题福建省漳州第一中学2023届高三下学期毕业班质检考化学试题福建省南平第一中学2023-2024学年高三上学期第二次阶段考化学试题江苏省前黄高级中学2023-2024学年高三上学期期中适应性考试化学试题福建省厦门第一中学2023-2024学年高二上学期10月月考试化学试题
2022·河北·模拟预测
6 . 为实现碳回收,我国科学家设计的用电化学法还原CO2制备草酸的装置如图所示。下列有关该装置的说法中错误的是
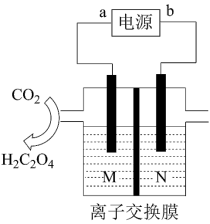

| A.a、b分别为电源的负极、正极 |
B.电解装置左池发生的电极反应为2CO2+2e-=C2O |
| C.为增强溶液导电性,左池中可加入少量Na2C2O4溶液 |
| D.右池电解质溶液为稀硫酸,发生的电极反应为2H2O-4e-=O2↑+4H+ |
您最近一年使用:0次
名校
解题方法
7 . 如图所示是原电池的装置图。请回答:

(1)若C为NaCl溶液,电流表指针发生偏转,B电极材料为Fe且作负极,则A电极上发生的电极反应式为___________ ;反应进行一段时间后,向两电极附近溶液滴加酚酞试剂,___________ (填“A”或“B”)电极周围溶液显红色。
(2)若需将反应:Cu+2Fe3+=Cu2++2Fe2+设计成如图所示的原电池装置,则A(正极)极材料为___________ ,B(负极)极材料为___________ ,溶液C为___________ 。
(3)CO与H2反应还可制备CH3OH,CH3OH可作为燃料使用,用CH3OH和O2组合形成的质子交换膜燃料电池的结构示意图如图:

电池总反应为2CH3OH+3O2=2CO2+4H2O,则d电极是___________ (填“正极”或“负极”),c电极的反应方程式为___________ 。若线路中转移1mol电子,则上述CH3OH燃料电池消耗的O2在标准状况下的体积为___________ L。

(1)若C为NaCl溶液,电流表指针发生偏转,B电极材料为Fe且作负极,则A电极上发生的电极反应式为
(2)若需将反应:Cu+2Fe3+=Cu2++2Fe2+设计成如图所示的原电池装置,则A(正极)极材料为
(3)CO与H2反应还可制备CH3OH,CH3OH可作为燃料使用,用CH3OH和O2组合形成的质子交换膜燃料电池的结构示意图如图:

电池总反应为2CH3OH+3O2=2CO2+4H2O,则d电极是
您最近一年使用:0次
解题方法
8 . CO是一种重要的能源物质。
(1)下列反应原理适合实验室制备CO的是_______ (填选项字母)。
A.C+H2O CO+H2B.2C+O2
CO+H2B.2C+O2 2CO C.HCOOH
2CO C.HCOOH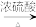 CO+H2O
CO+H2O
(2)用于检测CO含量的某气敏传感器的工作原理如图所示。

①该装置工作时,将_______ 能转化为______ 能。
②工作时,电极 I 作____ 极,电极 II 上的电极反应式为_____________ 。
③向电极 I 缓缓通入10 L 混合气体 ( 其他气体不参加反应)后,测得电路中通过2 mole-,则该混合气体中CO的含量为___ mol/L
(1)下列反应原理适合实验室制备CO的是
A.C+H2O
 CO+H2B.2C+O2
CO+H2B.2C+O2 2CO C.HCOOH
2CO C.HCOOH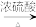 CO+H2O
CO+H2O(2)用于检测CO含量的某气敏传感器的工作原理如图所示。

①该装置工作时,将
②工作时,电极 I 作
③向电极 I 缓缓通入10 L 混合气体 ( 其他气体不参加反应)后,测得电路中通过2 mole-,则该混合气体中CO的含量为
您最近一年使用:0次
名校
9 . (1)科研人员设想用如图所示装置生产硫酸。
①上述生产硫酸的总反应方程式为_____ ,b 是_____ 极,b 电极反应式为______________ ,生产过程中H+向_____ (填 a 或 b)电极区域运动。
②该小组同学反思原电池的原理,其中观点正确的是_____ (填字母)。
A.原电池反应的过程中可能没有电子发生转移
B.原电池装置一定需要2个活泼性不同的金属电极
C.电极一定不能参加反应
D.氧化反应和还原反应可以拆开在两极发生
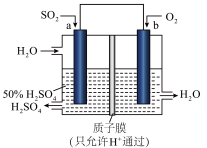
(2)CO与H2反应还可制备CH3OH,CH3OH可作为燃料使用,用CH3OH和O2组合形成的质子交换膜(只允许H+通过)质子交换膜左右两侧的溶液均为1L 2mol·L-1H2SO4溶液。燃料电池的结构示意图如:电池总反应为2CH3OH+3O2=2CO2+4H2O,c电极为_____ (填“正极”或“负极”),c电极反应方程式为___________________________ 。当电池中有1mol e-发生转移时左右两侧溶液的质量之差为______ g (假设反应物耗尽,忽略气体的溶解)。

①上述生产硫酸的总反应方程式为
②该小组同学反思原电池的原理,其中观点正确的是
A.原电池反应的过程中可能没有电子发生转移
B.原电池装置一定需要2个活泼性不同的金属电极
C.电极一定不能参加反应
D.氧化反应和还原反应可以拆开在两极发生

(2)CO与H2反应还可制备CH3OH,CH3OH可作为燃料使用,用CH3OH和O2组合形成的质子交换膜(只允许H+通过)质子交换膜左右两侧的溶液均为1L 2mol·L-1H2SO4溶液。燃料电池的结构示意图如:电池总反应为2CH3OH+3O2=2CO2+4H2O,c电极为
您最近一年使用:0次
2019-05-10更新
|
254次组卷
|
2卷引用:河北安平中学2019-2020学年高二上学期第二次月考化学试题
9-10高一下·江苏扬州·期末
10 . 按下图装置进行实验,并回答下列问题:
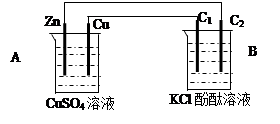
(1)判断装置的名称:A池为___________ ;B池为______________ ;
(2)锌极为________ 极,电极反应式为___________________________________ ;铜极为________ 极,电极反应式为___________________________________ ;石墨棒C1为______ 极,电极反应式为__________________________________ ;石墨棒C2附近发生的实验现象为______________________________________ ;
(3)当C2极析出224mL气体(标准状态)时,锌的质量变化_________ (变大、不变或变小)了________ g,CuSO4溶液的质量_________ (增加、不变或减少)_________ g。
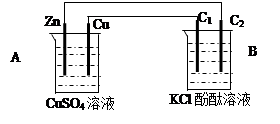
(1)判断装置的名称:A池为
(2)锌极为
(3)当C2极析出224mL气体(标准状态)时,锌的质量变化
您最近一年使用:0次
2014-07-16更新
|
784次组卷
|
11卷引用:2011-2012学年河北省唐山一中高二上学期期中考试化学(理)试卷
(已下线)2011-2012学年河北省唐山一中高二上学期期中考试化学(理)试卷2015-2016学年河北省容城中学高二上学期第一次月考化学试卷(已下线)2010年江苏省江都中学高一第二学期期末考试化学试题(已下线)2011-2012学年福建省厦门一中高二上学期期中考试化学试卷(已下线)2013-2014福建省安溪八中高二下学期期末考试化学试卷云南省临沧市凤庆县第二中学2019-2020学年高三第一学期开学考试化学试题(已下线)考点09 原电池及化学电源——《备战2020年高考精选考点专项突破题集》贵州省惠水县第一高级中学2019-2020学年高三上学期期末考试化学试题宁夏回族自治区中卫市中宁县中宁中学2019-2020学年高二下学期阶段测试化学试题鲁科版(2019)选择性必修1 第1章 化学反应与能量转化 第3节 电能转化为化学能——电解福建省仙游县郊尾中学2020届高三上学期期中考试化学试题



