1 . 氢能备受人们的关注,储氢材料的研究对于氢能的储运和开发具有重要意义。回答下列问题:
Ⅰ.储氢材料氨硼烷 储氢容量高,常温常压下为白色晶体,熔点
储氢容量高,常温常压下为白色晶体,熔点 ,易溶于水。
,易溶于水。
(1) 晶体的晶体类型为
晶体的晶体类型为___________ 晶体。
(2) 易溶于水的主要原因是
易溶于水的主要原因是___________ 。
(3) 中
中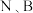 都达到稳定结构,
都达到稳定结构, 分子的结构式为
分子的结构式为___________ (用“ ”表示配位键)。
”表示配位键)。
Ⅱ.铁镁合金是目前已发现的储氢密度最高的储氢材料之一,其晶胞结构如图所示。 原子位于
原子位于 原子构成的
原子构成的___________ 面体空隙中。
(5)铁镁合金的化学式为___________ 。
(6)若该晶胞的边长为 ,阿伏加德罗常数为
,阿伏加德罗常数为 ,则该合金的密度为
,则该合金的密度为___________  (用含
(用含 的表达式表示)。
的表达式表示)。
(7)若该晶体储氢时, 分子在晶胞的体心和棱心位置,则含
分子在晶胞的体心和棱心位置,则含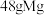 的该储氢合金可储存
的该储氢合金可储存 (标准状况)的体积约为
(标准状况)的体积约为___________ L。
Ⅰ.储氢材料氨硼烷
 储氢容量高,常温常压下为白色晶体,熔点
储氢容量高,常温常压下为白色晶体,熔点 ,易溶于水。
,易溶于水。(1)
 晶体的晶体类型为
晶体的晶体类型为(2)
 易溶于水的主要原因是
易溶于水的主要原因是(3)
 中
中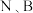 都达到稳定结构,
都达到稳定结构, 分子的结构式为
分子的结构式为 ”表示配位键)。
”表示配位键)。Ⅱ.铁镁合金是目前已发现的储氢密度最高的储氢材料之一,其晶胞结构如图所示。
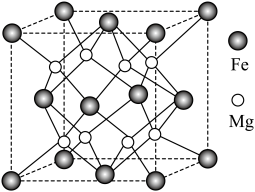
 原子位于
原子位于 原子构成的
原子构成的(5)铁镁合金的化学式为
(6)若该晶胞的边长为
 ,阿伏加德罗常数为
,阿伏加德罗常数为 ,则该合金的密度为
,则该合金的密度为 (用含
(用含 的表达式表示)。
的表达式表示)。(7)若该晶体储氢时,
 分子在晶胞的体心和棱心位置,则含
分子在晶胞的体心和棱心位置,则含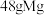 的该储氢合金可储存
的该储氢合金可储存 (标准状况)的体积约为
(标准状况)的体积约为
您最近一年使用:0次
名校
2 . 物质的组成与结构决定了物质的性质与变化。下列说法正确的是
| A.MgO的熔点高于NaCl的熔点 |
| B.金刚石与碳化硅晶体结构相似,金刚石的硬度小于碳化硅 |
| C.CH3CH2CH2COOH的酸性比CH3COOH的酸性强 |
| D.HF晶体沸点高于HCl,是因为HCl共价键键能小于HF |
您最近一年使用:0次
2023-03-18更新
|
682次组卷
|
5卷引用:辽宁省锦州市育明高级中学2022-2023学年高二下学期第一次阶段性考试化学试题
3 . 我国科学家成功合成了一种具有超高能量且室温下稳定的盐(局部结构如图),其中含有两种10电子离子。下列说法错误的是
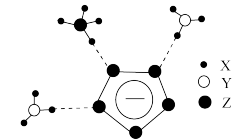

| A.经X射线衍射实验可测得该盐的晶体结构 |
| B.该盐可用于制造炸药 |
| C.两种10电子离子中均含配位键 |
D.图中 离子中Z原子采取 离子中Z原子采取 杂化 杂化 |
您最近一年使用:0次
2022-04-22更新
|
506次组卷
|
4卷引用:辽宁省锦州市2022届高三第一次质量检测化学试题
名校
4 . 铁镁合金是目前已发现的储氢密度较高的储氢材料之一,其晶胞结构如图所示(黑球代表Fe,白球代表Mg)。则下列说法不正确的是
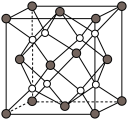

| A.铁镁合金的化学式为Mg2Fe |
| B.晶体中存在的化学键类型为金属键 |
| C.晶胞中Fe和Mg的配位数都是4 |
D.该晶胞的质量是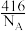 g(NA表示阿伏加德罗常数的值 g(NA表示阿伏加德罗常数的值 |
您最近一年使用:0次
名校
解题方法
5 . Na3OCl是一种良好的离子导体,具有反钙钛矿晶体结构。回答下列问题:
(1)Ca小于Ti的是_______ (填标号)。
A.最外层电子数 B.未成对电子数 C.原子半径 D.第三电离能
(2)由O、Cl元素可组成不同的单质和化合物,其中Cl2O2能破坏臭氧层。
① Cl2O2的沸点比H2O2低,原因是___________________________________ 。
② O3分子中心原子杂化类型为_______ ;O3是极性分子,理由是___________________ 。
(3)Na3OCl可由以下两种方法制得:
方法Ⅰ Na2O + NaCl Na3OCl
Na3OCl
方法II 2Na + 2NaOH + 2NaCl 2Na3OCl + H2↑
2Na3OCl + H2↑
① Na2O的电子式为____________ 。
② 在方法Ⅱ的反应中,形成的化学键有_______ (填标号)。
A.金属键 B.离子键 C.配位键 D.极性键 E.非极性键
(4)Na3OCl晶体属于立方晶系,其晶胞结构如右所示。已知:晶胞参数为a nm,密度为d g·cm-3。

①Na3OCl晶胞中,Cl位于各顶点位置,Na位于_________ 位置,两个Na之间的最短距离为________ nm。
②用a、d表示阿伏加 德罗常数的值NA=__________________ (列计算式)。
(1)Ca小于Ti的是
A.最外层电子数 B.未成对电子数 C.原子半径 D.第三电离能
(2)由O、Cl元素可组成不同的单质和化合物,其中Cl2O2能破坏臭氧层。
① Cl2O2的沸点比H2O2低,原因是
② O3分子中心原子杂化类型为
(3)Na3OCl可由以下两种方法制得:
方法Ⅰ Na2O + NaCl
 Na3OCl
Na3OCl方法II 2Na + 2NaOH + 2NaCl
 2Na3OCl + H2↑
2Na3OCl + H2↑① Na2O的电子式为
② 在方法Ⅱ的反应中,形成的化学键有
A.金属键 B.离子键 C.配位键 D.极性键 E.非极性键
(4)Na3OCl晶体属于立方晶系,其晶胞结构如右所示。已知:晶胞参数为a nm,密度为d g·cm-3。

①Na3OCl晶胞中,Cl位于各顶点位置,Na位于
②用a、d表示阿伏加 德罗常数的值NA=
您最近一年使用:0次
2019-06-11更新
|
598次组卷
|
8卷引用:辽宁省锦州市联合校2020届高三上学期期末考试化学试题
名校
6 . 下列各项比较中前者高于(或大于或强于)后者的是
| A.金属Mg(六方最密堆积)和金属Cu(面心立方最密堆积)的空间利用率 |
| B.BF3和CH4中心原子的价层电子对数 |
| C.Si-O和C-O的键能 |
D.对羟基苯甲醛(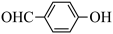 )和邻羟基苯甲醛( )和邻羟基苯甲醛(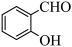 )的沸点 )的沸点 |
您最近一年使用:0次
2019-05-28更新
|
362次组卷
|
4卷引用:辽宁省锦州市黑山县黑山中学2019-2020学年高二6月月考化学试题
名校
7 . 有四种不同堆积方式的金属晶体的晶胞如图所示,下列有关说法正确的是
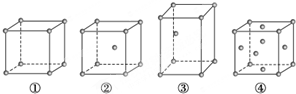

| A.①为简单立方堆积,②为镁型,③为钾型,④为铜型 |
| B.每个晶胞含有的原子数分别为:①1个,②2个,③2个,④4个 |
| C.晶胞中原子的配位数分别为:①6,②8,③8,④12 |
| D.空间利用率的大小关系为:①<②<③<④ |
您最近一年使用:0次
2017-09-21更新
|
1108次组卷
|
12卷引用:辽宁省锦州市凌海市第三高级中学2019-2020学年高二6月月考化学试题
辽宁省锦州市凌海市第三高级中学2019-2020学年高二6月月考化学试题宁夏石嘴山市第三中学2018届高三9月月考化学试题福建省晋江市季延中学2017-2018学年高二上学期期中考试(理)化学试题人教版高中化学选修三:3.3金属晶体(第2课时)同步训练【全国校级联考】湖北省部分重点中学2017-2018学年高二下学期期中考试化学试题(已下线)2019年5月20日 《每日一题》选修3-四种晶胞的空间利用率的计算山西省忻州实验中学2018-2019学年高二下学期期中考试化学试题湖北省宜昌市第二中学2018-2019学年高二上学期期中考试化学试题安徽省安庆市太湖县2019-2020学年高二下学期期中质量调研考试化学试题宁夏青铜峡市高级中学(吴忠中学青铜峡分校)2019-2020学年高二下学期期末考试化学试题山西省潞城第一中学2020-2021学年高二下学期3月月考化学试卷题黑龙江省齐齐哈尔市第八中学校2020-2021学年高二下学期期中考试化学试题



