名校
解题方法
1 . 氮化钛(TiN)为金黄色晶体,由于具有令人满意的仿金效果,越来越多地成为黄金的代替品。TiN晶体的晶胞结构如图所示。下列说法错误的是
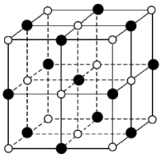

| A.Ti元素位于元素周期表d区,是过渡元素 |
| B.该晶胞中含有4个Ti原子和4个N原子 |
| C.Ti均位于N构成的八面体空隙中 |
| D.Ti的第一电离能大于Mn |
您最近一年使用:0次
2022-04-26更新
|
531次组卷
|
4卷引用:辽宁省阜新市阜新蒙古族自治县高级中学2022届高三下学期模拟考试化学试题
名校
2 . 三价铬离子( )是葡萄糖耐量因子(GTF)的重要组成成分,GTF能够协助胰岛素发挥作用。构成葡萄糖耐量因子和蛋白质的元素有C、H、O、N、S、Cr等。回答下列问题:
)是葡萄糖耐量因子(GTF)的重要组成成分,GTF能够协助胰岛素发挥作用。构成葡萄糖耐量因子和蛋白质的元素有C、H、O、N、S、Cr等。回答下列问题:
(1)Cr的价层电子排布式为_______ 。
(2)O、N、S的原子半径由大到小的顺序为_______ 。
(3) 分子的 VSEPR模型名称为
分子的 VSEPR模型名称为_______
(4)化学式为 的化合物有多种结构,其中一种可表示为
的化合物有多种结构,其中一种可表示为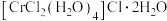 ,该物质的配离子中提供孤电子对的原子为
,该物质的配离子中提供孤电子对的原子为_______ ,配位数为_______ 。
(5)由碳元素形成的某种晶体的晶胞结构如图所示,若阿伏加德罗常数的值为 ,晶体密度为
,晶体密度为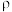
 ,则该晶胞的棱长为
,则该晶胞的棱长为_______ pm。

 )是葡萄糖耐量因子(GTF)的重要组成成分,GTF能够协助胰岛素发挥作用。构成葡萄糖耐量因子和蛋白质的元素有C、H、O、N、S、Cr等。回答下列问题:
)是葡萄糖耐量因子(GTF)的重要组成成分,GTF能够协助胰岛素发挥作用。构成葡萄糖耐量因子和蛋白质的元素有C、H、O、N、S、Cr等。回答下列问题:(1)Cr的价层电子排布式为
(2)O、N、S的原子半径由大到小的顺序为
(3)
 分子的 VSEPR模型名称为
分子的 VSEPR模型名称为(4)化学式为
 的化合物有多种结构,其中一种可表示为
的化合物有多种结构,其中一种可表示为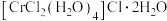 ,该物质的配离子中提供孤电子对的原子为
,该物质的配离子中提供孤电子对的原子为(5)由碳元素形成的某种晶体的晶胞结构如图所示,若阿伏加德罗常数的值为
 ,晶体密度为
,晶体密度为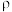
 ,则该晶胞的棱长为
,则该晶胞的棱长为
您最近一年使用:0次
2021-06-15更新
|
136次组卷
|
2卷引用:辽宁省阜新二高2020-2021学年高二下学期期中考试化学试题
解题方法
3 . 钙钛矿(CaTiO3)型化合物是一类可用于生产太阳能电池、传感器、固体电阻器等的功能材料,回答下列问题:
(1)基态Ti原子的核外电子排布式为________ 。
(2)Ti的四卤化物熔点如下表所示,TiF4熔点高于其他三种卤化物,且自TiCl4至TiI4熔点依次升高,原因是________ 。
(3)CaTiO3的晶胞如图(a)所示,其组成元素的电负性大小顺序是________ ;金属离子与氧离子间的作用力为________ ,Ca2+的配位数是________ 。
(4)一种立方钙钛矿结构的金属卤化物光电材料的组成为Pb2+、I-和有机碱离子CH3NH3+,其晶胞如图(b)所示。有机碱CH3NH3+中,N原子的杂化轨道类型是________ ;若晶胞参数为anm,则晶体密度为________ g/cm3(列出计算式)。

(5)用上述金属卤化物光电材料制作的太阳能电池在使用过程中会产生单质铅和碘,降低了器件效率和使用寿命。我国科学家巧妙地在此材料中引入稀土铕(Eu)盐,提升了太阳能电池的效率和使用寿命,其作用原理如图(c)所示,用离子方程式表示该原理________ 、________ 。
(1)基态Ti原子的核外电子排布式为
(2)Ti的四卤化物熔点如下表所示,TiF4熔点高于其他三种卤化物,且自TiCl4至TiI4熔点依次升高,原因是
| 化合物 | TiF4 | TiCl4 | TiBr4 | TiI4 |
| 熔点/℃ | 377 | ﹣24.12 | 38.3 | 155 |
(4)一种立方钙钛矿结构的金属卤化物光电材料的组成为Pb2+、I-和有机碱离子CH3NH3+,其晶胞如图(b)所示。有机碱CH3NH3+中,N原子的杂化轨道类型是

(5)用上述金属卤化物光电材料制作的太阳能电池在使用过程中会产生单质铅和碘,降低了器件效率和使用寿命。我国科学家巧妙地在此材料中引入稀土铕(Eu)盐,提升了太阳能电池的效率和使用寿命,其作用原理如图(c)所示,用离子方程式表示该原理
您最近一年使用:0次
解题方法
4 . 已知A、B、C、D是原子序数依次增大的四种短周期主族元素,A的周期数等于其主族序数,B原子的价电子排布为nsnnpn,D是地壳中含量最多的元素,E是第四周期的p区元素且最外层只有2对成对电子,F元素的基态原子第四能层只有一个电子,其它能层均已充满电子。
(1)基态E原子的价电子排布图________ 。
(2)B、C、D三元素第一电离能由大到小的顺序为________ (用元素符号表示)。
(3)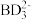 中心原子杂化轨道的类型为
中心原子杂化轨道的类型为________ 杂化;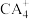 的空间构型为
的空间构型为________ 。
(4)化合物B2A4中含有σ键与π键的个数比为________ 。
(5)比较D、E元素最简单氢化物的沸点高低________ (用化学式表示),理由是________ (用文字表达)。
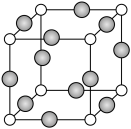
(6)C、F两元素形成的某化合物的晶胞结构如图所示,顶点为C原子,则该化合物的化学式是________ ,C原子的配位数是________ ,若相邻C原子和F原子间的距离为acm,阿伏加 德罗常数为NA,则该晶体的密度为________ g/cm3(用含a、NA的符号表示)。
(1)基态E原子的价电子排布图
(2)B、C、D三元素第一电离能由大到小的顺序为
(3)
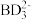 中心原子杂化轨道的类型为
中心原子杂化轨道的类型为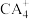 的空间构型为
的空间构型为(4)化合物B2A4中含有σ键与π键的个数比为
(5)比较D、E元素最简单氢化物的沸点高低
(6)C、F两元素形成的某化合物的晶胞结构如图所示,顶点为C原子,则该化合物的化学式是

您最近一年使用:0次



