解题方法
1 . 刀片电池(The blade battery)是比亚迪于2020年3月29日发布的电池产品。正极材料使用了磷酸亚铁锂( ),具有强环境适应性,更安全可靠的特点。磷酸亚铁锂由
),具有强环境适应性,更安全可靠的特点。磷酸亚铁锂由 、
、 (葡萄糖)和
(葡萄糖)和 在高温条件下制备:
在高温条件下制备: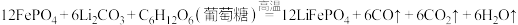 。回答下列问题:
。回答下列问题:
(1)Li位于元素周期表的_____ 区,基态Fe原子的价电子排布式为_________ 。
(2)同周期元素中,第一电离能大于O的原子是_______ 。
(3)有关 叙述正确的是___________。
叙述正确的是___________。
(4) 的空间结构为
的空间结构为______ ,其中P采取____ 杂化方式。
(5)上述反应方程式涉及的物质中最易溶于水的共价化合物是______ ,解释易溶于水的原因_______ 。
 ),具有强环境适应性,更安全可靠的特点。磷酸亚铁锂由
),具有强环境适应性,更安全可靠的特点。磷酸亚铁锂由 、
、 (葡萄糖)和
(葡萄糖)和 在高温条件下制备:
在高温条件下制备: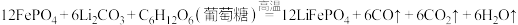 。回答下列问题:
。回答下列问题:(1)Li位于元素周期表的
(2)同周期元素中,第一电离能大于O的原子是
(3)有关
 叙述正确的是___________。
叙述正确的是___________。A.分子中 键和 键和 键个数比为1:1 键个数比为1:1 | B.含有极性键的非极性分子 |
C.分子空间结构与 相同 相同 | D.熔点、沸点高于 |
 的空间结构为
的空间结构为(5)上述反应方程式涉及的物质中最易溶于水的共价化合物是
您最近一年使用:0次
2024-01-13更新
|
224次组卷
|
2卷引用:湖南省益阳博雅高级中学2023-2024学年高二上学期期末考试化学试题
名校
解题方法
2 . 金属镍广泛应用于制造记忆合金、储氢合金以及用作加氢反应的催化剂,是重要的战略物资,但资源匮乏。从某废镍渣(含 、NiO、FeO、
、NiO、FeO、 )中回收金属镍并转化为
)中回收金属镍并转化为 的流程如图所示:
的流程如图所示:
(1)“滤液A”中主要溶质的化学式为________ 。
(2)“焙烧”后金属元素以硫酸盐的形式存在,写出NiO与 反应的化学方程式:
反应的化学方程式:_______ 。
(3)使用95℃热水“溶解”后过滤,所得“滤渣”的主要成分的化学式是______ 。
(4)①“萃取”时发生反应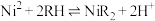 (RH为萃取剂),一定条件下,萃取平衡时,
(RH为萃取剂),一定条件下,萃取平衡时, ,则
,则 的苯取率为
的苯取率为_______ 。
②反萃取获得 ,溶液的实验操作是
,溶液的实验操作是______ 。
(5) 在碱性溶液中用NaClO氧化,可制得碱性镍镉电池电极材料
在碱性溶液中用NaClO氧化,可制得碱性镍镉电池电极材料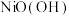 ,该反应的离子方程式为
,该反应的离子方程式为_________ 。
(6)镍能形成多种不同的化合物。图a是镍的一种配合物结构,图b是镍的一种氧化物的结构,下列说法不正确的是_________(填字母)。
 、NiO、FeO、
、NiO、FeO、 )中回收金属镍并转化为
)中回收金属镍并转化为 的流程如图所示:
的流程如图所示:
(1)“滤液A”中主要溶质的化学式为
(2)“焙烧”后金属元素以硫酸盐的形式存在,写出NiO与
 反应的化学方程式:
反应的化学方程式:(3)使用95℃热水“溶解”后过滤,所得“滤渣”的主要成分的化学式是
(4)①“萃取”时发生反应
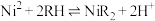 (RH为萃取剂),一定条件下,萃取平衡时,
(RH为萃取剂),一定条件下,萃取平衡时, ,则
,则 的苯取率为
的苯取率为②反萃取获得
 ,溶液的实验操作是
,溶液的实验操作是(5)
 在碱性溶液中用NaClO氧化,可制得碱性镍镉电池电极材料
在碱性溶液中用NaClO氧化,可制得碱性镍镉电池电极材料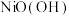 ,该反应的离子方程式为
,该反应的离子方程式为(6)镍能形成多种不同的化合物。图a是镍的一种配合物结构,图b是镍的一种氧化物的结构,下列说法不正确的是_________(填字母)。
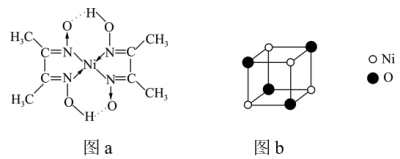
A.图a中,电负性 |
| B.图a分子中存在的化学键有共价键、配位键、氢键 |
| C.图b是氧化镍(NiO)的一个晶胞 |
D.氧化镍中 、 、 的配位数都是6 的配位数都是6 |
您最近一年使用:0次
2024-01-05更新
|
256次组卷
|
5卷引用:湖南省长沙市长郡中学2024届高三上学期期末适应性考试化学试题
名校
解题方法
3 . 硼、镁及其化合物在工农业生产中应用广泛。已知:硼镁矿主要成分为 ,硼砂的化学式为
,硼砂的化学式为 。利用硼镁矿制取金属镁及粗硼的工艺流程如下。请回答下列有关问题:
。利用硼镁矿制取金属镁及粗硼的工艺流程如下。请回答下列有关问题:

已知: 在20℃、40℃、60℃、100℃时溶解度依次为
在20℃、40℃、60℃、100℃时溶解度依次为 、
、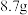 、
、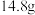 、
、 。
。
(1)B原子的电子排布式为________ 。
(2)硼砂溶于热水后,常用 调pH至2~3,紧接着再采用“热过滤”、冷却结晶获得硼酸晶体。“热过滤”的目的是
调pH至2~3,紧接着再采用“热过滤”、冷却结晶获得硼酸晶体。“热过滤”的目的是________________________________________________ 。
(3)X为 晶体加热脱水的产物,其与Mg反应制取粗硼的化学方程式为
晶体加热脱水的产物,其与Mg反应制取粗硼的化学方程式为______________________ 。
(4) 需要在
需要在 氛围中加热制
氛围中加热制 ,其目的是
,其目的是__________ 。
(5)已知硼酸( )是一种片层状结构的白色晶体,层内的
)是一种片层状结构的白色晶体,层内的 分子通过氢键(如图,用虚线表示)相连。硼酸在冷水中溶解度很小,但在热水中较大,原因是
分子通过氢键(如图,用虚线表示)相连。硼酸在冷水中溶解度很小,但在热水中较大,原因是_______ 。

已知硼酸在水中电离产生 的过程为
的过程为 。下列有关硼酸及其相关化合物的说法正确的是
。下列有关硼酸及其相关化合物的说法正确的是________ (填标号)。
A.硼酸的电离过程中有配位键形成 B.硼酸为三元酸
C.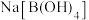 的水溶液呈碱性 D.硼酸和
的水溶液呈碱性 D.硼酸和 中
中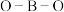 的键角相同
的键角相同
(6)制得的粗硼在一定条件下生成 ,
, 加热分解可以得到纯净的单质硼。现将
加热分解可以得到纯净的单质硼。现将 粗硼制成的
粗硼制成的 完全分解,生成的
完全分解,生成的 用
用
 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液
溶液 。该粗硼样品的纯度为
。该粗硼样品的纯度为________ (提示: )
)
 ,硼砂的化学式为
,硼砂的化学式为 。利用硼镁矿制取金属镁及粗硼的工艺流程如下。请回答下列有关问题:
。利用硼镁矿制取金属镁及粗硼的工艺流程如下。请回答下列有关问题:
已知:
 在20℃、40℃、60℃、100℃时溶解度依次为
在20℃、40℃、60℃、100℃时溶解度依次为 、
、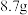 、
、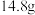 、
、 。
。(1)B原子的电子排布式为
(2)硼砂溶于热水后,常用
 调pH至2~3,紧接着再采用“热过滤”、冷却结晶获得硼酸晶体。“热过滤”的目的是
调pH至2~3,紧接着再采用“热过滤”、冷却结晶获得硼酸晶体。“热过滤”的目的是(3)X为
 晶体加热脱水的产物,其与Mg反应制取粗硼的化学方程式为
晶体加热脱水的产物,其与Mg反应制取粗硼的化学方程式为(4)
 需要在
需要在 氛围中加热制
氛围中加热制 ,其目的是
,其目的是(5)已知硼酸(
 )是一种片层状结构的白色晶体,层内的
)是一种片层状结构的白色晶体,层内的 分子通过氢键(如图,用虚线表示)相连。硼酸在冷水中溶解度很小,但在热水中较大,原因是
分子通过氢键(如图,用虚线表示)相连。硼酸在冷水中溶解度很小,但在热水中较大,原因是
已知硼酸在水中电离产生
 的过程为
的过程为 。下列有关硼酸及其相关化合物的说法正确的是
。下列有关硼酸及其相关化合物的说法正确的是A.硼酸的电离过程中有配位键形成 B.硼酸为三元酸
C.
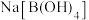 的水溶液呈碱性 D.硼酸和
的水溶液呈碱性 D.硼酸和 中
中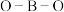 的键角相同
的键角相同(6)制得的粗硼在一定条件下生成
 ,
, 加热分解可以得到纯净的单质硼。现将
加热分解可以得到纯净的单质硼。现将 粗硼制成的
粗硼制成的 完全分解,生成的
完全分解,生成的 用
用
 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液
溶液 。该粗硼样品的纯度为
。该粗硼样品的纯度为 )
)
您最近一年使用:0次
解题方法
4 . C、Si均为第ⅣA族元素,回答下列问题。
(1)若将基态硅原子最高能级的电子排布图表示为 ,则它违背了
,则它违背了___________ 这一电子排布规律。
(2)以SiO2为基本原料制备粗硅的原理为 ,则C、O、Si第一电离能由大到小的顺序为
,则C、O、Si第一电离能由大到小的顺序为___________ 。
(3)CO2和SiO2两种物质中,C、Si原子的杂化类型分别为___________ ;CO2的熔点远低于SiO2的原因是___________ 。
(4) 的键角为
的键角为___________ ;写出一种与 互为等电子体的分子
互为等电子体的分子___________ 。
(5)硅的含氧化合物都以硅氧四面体( )作为基本结构单元,如图甲所示,可简化为图乙。硅氧四面体通过共用氧原子可形成各种不同的硅酸根离子,如图丙和图丁,则丙的化学式为
)作为基本结构单元,如图甲所示,可简化为图乙。硅氧四面体通过共用氧原子可形成各种不同的硅酸根离子,如图丙和图丁,则丙的化学式为___________ 。在无限长链的硅酸根离子中硅原子与氧原子个数比为___________ 。

(1)若将基态硅原子最高能级的电子排布图表示为
 ,则它违背了
,则它违背了(2)以SiO2为基本原料制备粗硅的原理为
 ,则C、O、Si第一电离能由大到小的顺序为
,则C、O、Si第一电离能由大到小的顺序为(3)CO2和SiO2两种物质中,C、Si原子的杂化类型分别为
(4)
 的键角为
的键角为 互为等电子体的分子
互为等电子体的分子(5)硅的含氧化合物都以硅氧四面体(
 )作为基本结构单元,如图甲所示,可简化为图乙。硅氧四面体通过共用氧原子可形成各种不同的硅酸根离子,如图丙和图丁,则丙的化学式为
)作为基本结构单元,如图甲所示,可简化为图乙。硅氧四面体通过共用氧原子可形成各种不同的硅酸根离子,如图丙和图丁,则丙的化学式为
您最近一年使用:0次
2023-01-10更新
|
252次组卷
|
2卷引用:湖南省怀化市2022-2023学年高三下学期期末考试化学试题
名校
5 . 某化合物的结构示意图如图,下列关于该化合物的叙述中不正确的是
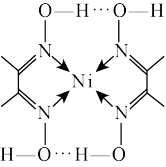

| A.该化合物含有的元素有五种 |
| B.该化合物属配合物,中心离子的配位数是4,配体是氮元素 |
C. 该化合物中 该化合物中 键数目为 键数目为 |
| D.该化合物中含有极性键、非极性键、配位键和氢键 |
您最近一年使用:0次
2022-10-09更新
|
570次组卷
|
7卷引用:湖南省攸县第一中学2022-2023学年高二上学期期末考试化学试题
湖南省攸县第一中学2022-2023学年高二上学期期末考试化学试题河南省焦作市博爱县第一中学2022-2023学年高二下学期6月期末考试化学试题浙江省部分校2022-2023学年高三上学期开学摸底考试化学试题宁夏石嘴山市平罗中学2022-2023学年高二上学期期中考试(重点班)化学试题(已下线)2023年1月浙江省普通高校招生选考变式题(选择题11-16)(已下线)浙江省温州市普通高中2023届高三下学期第二次适应性考试化学试题变式题(选择题11-16)宁夏石嘴山市平罗中学2022-2023学年高二上学期11月期中化学试题
解题方法
6 . 锂电池正极材料NCA,极大地改善了锂电池的性能(注明:NCA指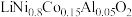 )。请回答下列问题:
)。请回答下列问题:
(1)基态铝原子的价层电子排布式为_______ 。基态钴原子核外有_______ 种能量不同的电子。
(2)钠、镁、铝的第一电离能由大到小排序为_______ (填元素符号)。
(3)氧化锂(Li2O)的熔点为1567℃,氧化镁(MgO)的熔点为2853℃。Li+、Mg2+的离子半径依次为0.076nm、0.072nm。它们的熔点差异除离子半径因素外,还与_______ 有关。
(4)螯合物又称内络合物。 、
、 都能与乙二胺(
都能与乙二胺(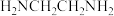 )形成螯合物,其配位原子是
)形成螯合物,其配位原子是_______ (填元素符号)。
(5) 是有机合成的常用还原剂。
是有机合成的常用还原剂。 的空间结构是
的空间结构是_______ 。
(6)NiO晶胞与NaCl晶胞相似,如下图所示:
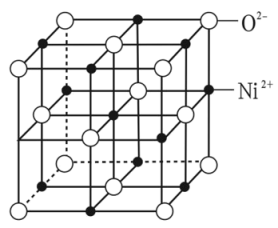
①连接面心上6个 构成
构成_______ (填标号)。
A.正四边形 B.正四面体 C.正八面体 D.立方体
②在NiO晶胞中,每个氧离子周围与它最近且相等距离的氧离子有_______ 个;每个镍离子周围与它最近且相等距离的氧离子有_______ 个。
③已知NiO晶胞边长为a cm,NA为阿伏加德罗常数的值,则NiO晶体的密度为_______  (只列出计算式)。(NiO的摩尔质量用M(g·mol-1)表示)
(只列出计算式)。(NiO的摩尔质量用M(g·mol-1)表示)
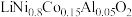 )。请回答下列问题:
)。请回答下列问题:(1)基态铝原子的价层电子排布式为
(2)钠、镁、铝的第一电离能由大到小排序为
(3)氧化锂(Li2O)的熔点为1567℃,氧化镁(MgO)的熔点为2853℃。Li+、Mg2+的离子半径依次为0.076nm、0.072nm。它们的熔点差异除离子半径因素外,还与
(4)螯合物又称内络合物。
 、
、 都能与乙二胺(
都能与乙二胺(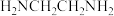 )形成螯合物,其配位原子是
)形成螯合物,其配位原子是(5)
 是有机合成的常用还原剂。
是有机合成的常用还原剂。 的空间结构是
的空间结构是(6)NiO晶胞与NaCl晶胞相似,如下图所示:

①连接面心上6个
 构成
构成A.正四边形 B.正四面体 C.正八面体 D.立方体
②在NiO晶胞中,每个氧离子周围与它最近且相等距离的氧离子有
③已知NiO晶胞边长为a cm,NA为阿伏加德罗常数的值,则NiO晶体的密度为
 (只列出计算式)。(NiO的摩尔质量用M(g·mol-1)表示)
(只列出计算式)。(NiO的摩尔质量用M(g·mol-1)表示)
您最近一年使用:0次
名校
解题方法
7 . 火星岩石冲含有大量氧化物,如 、
、 ,
, 、
、 、
、 、
、 、
、 等。回答下列问题:
等。回答下列问题:
(1)下表的氧化物中偏向共价晶体的过渡晶体是___________ ;(填化学式)。
(2)基态铁元素的原子最高能级电子云轮廓为___________ 形。
(3) 与
与 溶液反应生成的
溶液反应生成的 离子中
离子中 的杂化类型是
的杂化类型是___________ ; 和O构成的空间构型是
和O构成的空间构型是___________ 。
(4)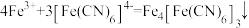 (普鲁士蓝),该反应可检验溶液中
(普鲁士蓝),该反应可检验溶液中 ,如图是普鲁士蓝
,如图是普鲁士蓝 晶胞的结构,与
晶胞的结构,与 形成配位键的是
形成配位键的是___________ (填 或
或 );
); 离子中
离子中 键与
键与 键的个数比是
键的个数比是___________ ;晶胞中与一个 距离相等的N有
距离相等的N有___________ 个。

 、
、 ,
, 、
、 、
、 、
、 、
、 等。回答下列问题:
等。回答下列问题:(1)下表的氧化物中偏向共价晶体的过渡晶体是
| 氧化物 |  |  |  |  |
| 离子键的百分数 | 62% | 50% | 41% | 33% |
(2)基态铁元素的原子最高能级电子云轮廓为
(3)
 与
与 溶液反应生成的
溶液反应生成的 离子中
离子中 的杂化类型是
的杂化类型是 和O构成的空间构型是
和O构成的空间构型是(4)
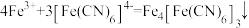 (普鲁士蓝),该反应可检验溶液中
(普鲁士蓝),该反应可检验溶液中 ,如图是普鲁士蓝
,如图是普鲁士蓝 晶胞的结构,与
晶胞的结构,与 形成配位键的是
形成配位键的是 或
或 );
); 离子中
离子中 键与
键与 键的个数比是
键的个数比是 距离相等的N有
距离相等的N有
您最近一年使用:0次
2022-05-01更新
|
325次组卷
|
2卷引用:湖南省株洲市第二中学2021-2022学年高二下学期期末考试化学试题
名校
解题方法
8 . 一种对中枢神经有抑制作用的药物结构如图。其中W、X、Y、Z原子序数依次增大,X、Y、Z位于第二周期,Y的气态氢化物的水溶性显碱性。
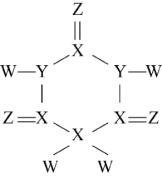
下列判断不正确的是

下列判断不正确的是
| A.第一电离能:X<Z<Y |
| B.XZ2晶体属于共价晶体 |
| C.W与Z可按原子个数比2:1和1:1形成两种化合物 |
| D.该药物在碱性溶液中加热,可水解产生Y的气态氢化物 |
您最近一年使用:0次
2022-04-09更新
|
1645次组卷
|
12卷引用:湖南省株洲市九方中学2021-2022学年高二下学期期末考试化学试题
湖南省株洲市九方中学2021-2022学年高二下学期期末考试化学试题河南省禹州市高级中学菁华校区2023-2024学年高三上学期期末考试理综试题-高中化学北京市东城区2022届高三一模化学试题(已下线)专项08 物质结构 元素周期律-备战2022年高考化学阶段性新题精选专项特训(全国卷)(4月期)(已下线)化学-2022年高考押题预测卷03(山东卷)(已下线)化学-2022年高考考前押题密卷(江苏卷)湖北省鄂东南三校2022届高三下学期5月联考化学试题北京市第一七一中学2022届高三下学期三模化学试题北京首都师范大学附属中学2023届高三上学期10月份月考化学试题北京市第二中学2022-2023学年高三上学期12月考化学试题天津市新华中学2022-2023学年高三第一次模拟考试化学试题北京市中关村中学2023-2024学年高三下学期3月月考化学试题
名校
9 . 碳原子构成的单质具有多种同素异形体,也对应着有多种不同晶体类型。请根据以下信息,回答下列问题。
(1)下图为金刚石的晶胞:

①沿晶胞对角面取得截图(如图c方式截图),所得截图如图d所示,请在图d中白圈处找出未画出的碳原子,请在图中白圈处找出未画出的碳原子,并在相应位置上按图示碳原子涂黑_______ 。
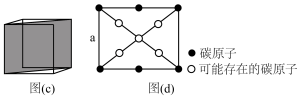
②已知在金刚石晶体中,每个碳原子周围的任意两根碳碳键被2个六元碳环所共有,请计算:金刚石晶体中每个碳原子被_______ 个六元碳环所共有,每个C—C被_______ 个六元碳环所共用。
③若再将任何两个成键的碳原子连线的中心处插入一个氧原子,就构成了某种特殊“碳氧化物”的晶胞。下列说法正确的是_______ (填标号)。
a.该“碳氧化物”晶体中每个碳原子周围的氧原子数是2
b.一个晶胞中含有8个“碳氧化物”分子
c.该“碳氧化物”的化学式为CO2
d.这种晶体是共价晶体
(2)①下图为石墨和石墨烯的结构示意图。石墨烯是从石墨材料中剥离出来,由碳原子组成的只有一层原子厚度的二维晶体。下列关于石墨与石墨烯的说法正确的是_______ 。

A.从石墨中剥离石墨烯需要破坏化学键
B.石墨中的碳原子采取sp2杂化
C.石墨属于混合型晶体,层与层之间存在分子间作用力
D.层内碳原子间存在共价键
E.石墨烯中平均每个六元碳环含有3个碳原子
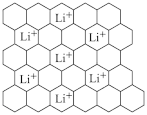
②石墨可用作锂离子电池的负极材料,Li+嵌入石墨的两层间,导致石墨的层堆积方式发生改变,形成化学式为LixC6的嵌入化合物,某石墨嵌入化合物的平面结构如图所示,则x=_______ ;若每个六元环都对应一个Li+,则化学式为_______ 。
(1)下图为金刚石的晶胞:

①沿晶胞对角面取得截图(如图c方式截图),所得截图如图d所示,请在图d中白圈处找出未画出的碳原子,请在图中白圈处找出未画出的碳原子,并在相应位置上按图示碳原子涂黑

②已知在金刚石晶体中,每个碳原子周围的任意两根碳碳键被2个六元碳环所共有,请计算:金刚石晶体中每个碳原子被
③若再将任何两个成键的碳原子连线的中心处插入一个氧原子,就构成了某种特殊“碳氧化物”的晶胞。下列说法正确的是
a.该“碳氧化物”晶体中每个碳原子周围的氧原子数是2
b.一个晶胞中含有8个“碳氧化物”分子
c.该“碳氧化物”的化学式为CO2
d.这种晶体是共价晶体
(2)①下图为石墨和石墨烯的结构示意图。石墨烯是从石墨材料中剥离出来,由碳原子组成的只有一层原子厚度的二维晶体。下列关于石墨与石墨烯的说法正确的是

A.从石墨中剥离石墨烯需要破坏化学键
B.石墨中的碳原子采取sp2杂化
C.石墨属于混合型晶体,层与层之间存在分子间作用力
D.层内碳原子间存在共价键
E.石墨烯中平均每个六元碳环含有3个碳原子
②石墨可用作锂离子电池的负极材料,Li+嵌入石墨的两层间,导致石墨的层堆积方式发生改变,形成化学式为LixC6的嵌入化合物,某石墨嵌入化合物的平面结构如图所示,则x=

您最近一年使用:0次
名校
10 . 我国科学家研究的第五代甲醇生产技术被誉为“液态阳光”,该技术中水经过太阳能光解制得氢气,再利用二氧化碳催化加氢合成甲醇。回答下列问题:
(1)太阳能光解时使用的太阳能电池板的主要成分为单晶硅,硅在周期表中的位置为____ 。
(2)硫化氢分子和水分子结构相似,但冰中水分子周围紧邻的分子数(4个)远小于硫化氢的(12个),原因是____ 。
(3)二氧化碳是重要的碳源,1molCO2分子中存在____ 个π键,碳在成键时,能将一个2s电子激发进入2p能级而参与成键,写出该激发态原子的核外电子排布式:_____ 。基态氧原子有____ 种不同形状的电子云。
(4)磷化硼纳米颗粒可以作为CO2合成甲醇时的非金属电催化剂,磷化硼硬度极大,在数千摄氏度高温时也较稳定,其立方晶胞结构如图所示。回答下列问题:

①晶胞中含有的P原子与B原子的个数比为____ ,晶体中与P原子距离最近且相等的P原子数为____ 。
②已知阿伏加德罗常数的值为NA,磷化硼的晶胞参数为apm,磷化硼晶体的密度ρ=___ g·cm-3。
(1)太阳能光解时使用的太阳能电池板的主要成分为单晶硅,硅在周期表中的位置为
(2)硫化氢分子和水分子结构相似,但冰中水分子周围紧邻的分子数(4个)远小于硫化氢的(12个),原因是
(3)二氧化碳是重要的碳源,1molCO2分子中存在
(4)磷化硼纳米颗粒可以作为CO2合成甲醇时的非金属电催化剂,磷化硼硬度极大,在数千摄氏度高温时也较稳定,其立方晶胞结构如图所示。回答下列问题:

①晶胞中含有的P原子与B原子的个数比为
②已知阿伏加德罗常数的值为NA,磷化硼的晶胞参数为apm,磷化硼晶体的密度ρ=
您最近一年使用:0次
2022-02-22更新
|
183次组卷
|
4卷引用:湖南省攸县第一中学2022-2023学年高二上学期期末考试化学试题



