名校
1 . 一种由镧( )、钴(
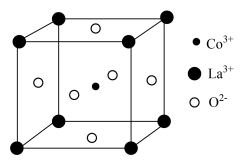
)、钴( )和氧(O)组成的三元氧化物催化剂材料,在环境保护、工业催化和光催化等领域有着广泛的应用。其晶胞结构如图所示,该立方晶胞参数为
)和氧(O)组成的三元氧化物催化剂材料,在环境保护、工业催化和光催化等领域有着广泛的应用。其晶胞结构如图所示,该立方晶胞参数为 。阿伏加德罗常数的值为
。阿伏加德罗常数的值为 。下列说法错误的是
。下列说法错误的是
 )、钴(
)、钴( )和氧(O)组成的三元氧化物催化剂材料,在环境保护、工业催化和光催化等领域有着广泛的应用。其晶胞结构如图所示,该立方晶胞参数为
)和氧(O)组成的三元氧化物催化剂材料,在环境保护、工业催化和光催化等领域有着广泛的应用。其晶胞结构如图所示,该立方晶胞参数为 。阿伏加德罗常数的值为
。阿伏加德罗常数的值为 。下列说法错误的是
。下列说法错误的是
A.晶体最简化学式为 |
B.晶体中与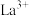 最近且距离相等的 最近且距离相等的 有6个 有6个 |
C.晶体的密度为 |
| D.晶体中相邻微粒间存在离子键 |
您最近一年使用:0次
2 . Mn是元素周期表中第25号元素,它的氧化物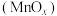 可用于催化醇的氧化氰化,反应如下:
可用于催化醇的氧化氰化,反应如下:
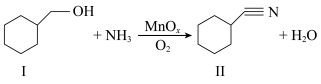
回答下列问题:
(1)组成物质Ⅰ的元素中,电负性最大是_____ (填元素符号)。
(2)物质Ⅱ中C原子的杂化轨道类型有_____ ; 该分子中含有
该分子中含有 键
键_____ mol。
(3) 的VSEPR模型为
的VSEPR模型为_____ ;已知 ,但该反应不及Na与
,但该反应不及Na与 的反应剧烈,从共价键的角度分析,可能的原因是
的反应剧烈,从共价键的角度分析,可能的原因是_____ 。
(4)Mn元素在周期表中的位置是_____ ;基态Mn原子的核外电子有_____ 种空间运动状态。
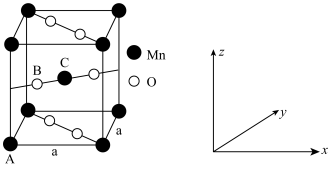
(5)某种 晶体的晶胞如下图所示,该晶体中Mn元素的化合价为
晶体的晶胞如下图所示,该晶体中Mn元素的化合价为_____ 。已知该晶胞底面是边长为 的正方形,以晶胞参数为单位长度建立坐标系,A、B、C处的原子坐标参数分别为
的正方形,以晶胞参数为单位长度建立坐标系,A、B、C处的原子坐标参数分别为 、
、 、
、 ,则Mn与O形成化学键的键长为
,则Mn与O形成化学键的键长为_____ cm(用含a、m、n的代数式表示)。
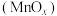 可用于催化醇的氧化氰化,反应如下:
可用于催化醇的氧化氰化,反应如下:
回答下列问题:
(1)组成物质Ⅰ的元素中,电负性最大是
(2)物质Ⅱ中C原子的杂化轨道类型有
 该分子中含有
该分子中含有 键
键(3)
 的VSEPR模型为
的VSEPR模型为 ,但该反应不及Na与
,但该反应不及Na与 的反应剧烈,从共价键的角度分析,可能的原因是
的反应剧烈,从共价键的角度分析,可能的原因是(4)Mn元素在周期表中的位置是
(5)某种
 晶体的晶胞如下图所示,该晶体中Mn元素的化合价为
晶体的晶胞如下图所示,该晶体中Mn元素的化合价为 的正方形,以晶胞参数为单位长度建立坐标系,A、B、C处的原子坐标参数分别为
的正方形,以晶胞参数为单位长度建立坐标系,A、B、C处的原子坐标参数分别为 、
、 、
、 ,则Mn与O形成化学键的键长为
,则Mn与O形成化学键的键长为
您最近一年使用:0次
名校
解题方法
3 . 下列关于各晶体模型示意图的分析正确的是
| 名称 |  的晶胞 的晶胞 |  的晶胞 的晶胞 | 晶体碘的晶胞 | 石墨晶体的结构 |
| 模型 示意图 | 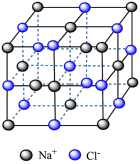 |  |  | 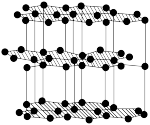 |
| 分析 | 1个 晶胞内含有6个 晶胞内含有6个 和6个 和6个 | B.Si原子的配位数为2 | C. 在晶胞中的排列有2种取向 在晶胞中的排列有2种取向 | D.石墨层与层间的主要作用力是共价键 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-08-15更新
|
417次组卷
|
3卷引用:广西桂林市2022-2023学年高二下学期期末考试化学试题
名校
解题方法
4 . 乙二胺四乙酸铁钠可用于感光材料冲洗药品及漂白剂,化学式为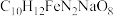 ;工业上可用EDTA与
;工业上可用EDTA与 、NaOH溶液发生反应进行制备,合成路线如下:
、NaOH溶液发生反应进行制备,合成路线如下:
(1)基态氯原子的价层电子排布图为___________ 。
(2)下列氮原子能量最高的是___________(填标号)。
(3)EDTA的组成元素中C、N、O的第一电离能由大到小顺序为___________ (填元素符号)。碳原子的杂化轨道类型为___________ 。
(4)NH3中N—H键的键角小于CH4中C—H键的键角,其原因为___________ 。
(5)某种Fe、N组成的磁性化合物的结构如图1所示,N随机排列在Fe构成的正八面体的空隙中。该磁性化合物的化学式为___________ 。___________ 区(填“s”“p”“d”或“ds”)。铁的某种晶胞沿面对角线的位置切下之后可以得到如图2所示的截面。假设铁的原子半径为a nm,则该铁晶体的密度为___________  (列出计算式,设
(列出计算式,设 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
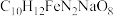 ;工业上可用EDTA与
;工业上可用EDTA与 、NaOH溶液发生反应进行制备,合成路线如下:
、NaOH溶液发生反应进行制备,合成路线如下: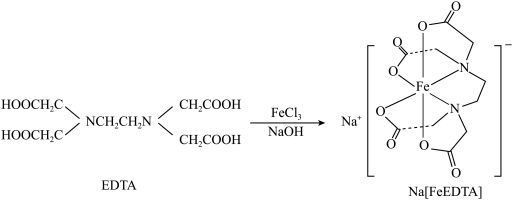
(1)基态氯原子的价层电子排布图为
(2)下列氮原子能量最高的是___________(填标号)。
A.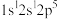 | B. | C. | D.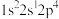 |
(4)NH3中N—H键的键角小于CH4中C—H键的键角,其原因为
(5)某种Fe、N组成的磁性化合物的结构如图1所示,N随机排列在Fe构成的正八面体的空隙中。该磁性化合物的化学式为
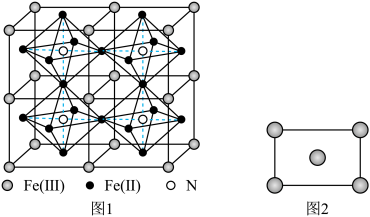
 (列出计算式,设
(列出计算式,设 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
您最近一年使用:0次
2023-04-23更新
|
865次组卷
|
8卷引用:广西壮族自治区南宁市第二中学2023届高三下学期收网考理科综合化学试题
广西壮族自治区南宁市第二中学2023届高三下学期收网考理科综合化学试题2023届广西钦州市灵山县那隆中学高三下学期5月考前冲刺保温卷理综试卷-高中化学福建省百校联盟2023届高三第三次模拟考试化学试题福建省百校联盟2023届高三下学期第三次模拟考试化学试题(已下线)押题密卷 02-【热题狂飙】2023年高考化学样卷(全国卷专用)(已下线)专题16 物质结构与性质综合题-2023年高考化学真题题源解密(全国通用)北京市第二中学2022-2023学年高二下学期期末考试化学试题北京市首都师范大学附属中学2023-2024学年高三下学期3月月考化学试题
5 . 黑火药的爆炸反应原理为2KNO3+3C+S K2S+N2↑+3CO2↑。请回答下列问题:
K2S+N2↑+3CO2↑。请回答下列问题:
(1)基态O原子的核外电子排布式为___________ ;基态18O原子核外有___________ 种空间运动状态的电子。
(2)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用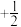 表示,与之相反的用
表示,与之相反的用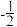 表示称为电子的自旋磁量子数。对于基态的N原子,其价电子自旋磁量子数的代数和为
表示称为电子的自旋磁量子数。对于基态的N原子,其价电子自旋磁量子数的代数和为___________ 。
(3)K位于周期表的___________ 区;基态钾离子的电子占据的最高能层符号是___________ 。
(4)K+与S2-具有相同的电子构型,r(K+)小于r(S2-),原因是___________ 。
(5)下列曲线表示氧族元素性质随核电荷数的变化趋势,正确的是___________ 。
a.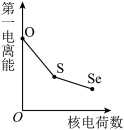 b.
b.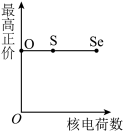 c.
c. d.
d.
(6)元素的基态原子得到一个电子形成气态负一价离子时所放出的能量称为第一电子亲和能(E1)。MgO的Born-Haber循环如图所示。

由图可知,Mg原子的第二电离能为___________ kJ/mol;O=O键的键能为___________ kJ/mol;氧原子的第一电子亲和能为___________ kJ/mol。
 K2S+N2↑+3CO2↑。请回答下列问题:
K2S+N2↑+3CO2↑。请回答下列问题:(1)基态O原子的核外电子排布式为
(2)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用
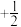 表示,与之相反的用
表示,与之相反的用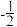 表示称为电子的自旋磁量子数。对于基态的N原子,其价电子自旋磁量子数的代数和为
表示称为电子的自旋磁量子数。对于基态的N原子,其价电子自旋磁量子数的代数和为(3)K位于周期表的
(4)K+与S2-具有相同的电子构型,r(K+)小于r(S2-),原因是
(5)下列曲线表示氧族元素性质随核电荷数的变化趋势,正确的是
a.
 b.
b. c.
c. d.
d.
(6)元素的基态原子得到一个电子形成气态负一价离子时所放出的能量称为第一电子亲和能(E1)。MgO的Born-Haber循环如图所示。

由图可知,Mg原子的第二电离能为
您最近一年使用:0次
2023-03-10更新
|
392次组卷
|
2卷引用:广西南宁市2022-2023学年高二上学期期末教学质量调研化学试题
名校
解题方法
6 . 实验室里经常可以看到蓝色的硅胶干燥剂,变色的主要原因是含有氯化钴。CoCl2为蓝色结晶性粉末,当暴露在潮湿的空气中时会很快变为粉红色的[Co(H2O)6]Cl2,若在约110℃烘箱里放置1小时,又恢复到半透明的蓝色。下列说法不正确的是
| A.Co元素位于元素周期表中第四周期第Ⅷ族 |
| B.配离子[Co(H2O)6]2+ 中H2O分子的中心原子杂化方式为 sp3 杂化 |
| C.1 mol[Co(H2O)6]Cl2与足量的AgNO3 溶液反应时,可得到2 mol AgCl |
| D.该蓝色的硅胶干燥剂,变色反应(蓝粉之间的转化)是可逆反应 |
您最近一年使用:0次
2022-05-30更新
|
338次组卷
|
3卷引用:广西玉林市博白县中学2022-2023学年高二下学期期中段考化学试题
解题方法
7 . 锂离子电池常用的电极材料是LiCoO2和石墨。
(1)画出基态Co2+离子的价电子排布图__________________ 。
(2)Co2+与CN—结合形成配合物[(Co(CN)6]4-,其中与Co2+结合的C原子的杂化方式是_____ 。
(3)NH3分子与Co2+结合成配合物[Co(NH3)6]2+,与游离的氨分子相比,其键角∠HNH____ (填“较大”,“较小”或“相同”),解释原因________________ 。
(4)Li2O的熔点为1570℃,CoO的熔点为1935℃,解释后者熔点更高的主要原因是_____ 。
(5)石墨的晶胞为六方晶胞,部分晶胞参数如下图所示。若石墨的密度为d g·cm-3,以NA代表阿伏加 德罗常数的数值,则石墨中的C-C键长为________ pm,晶胞中A、B两原子间距为________ pm。

(1)画出基态Co2+离子的价电子排布图
(2)Co2+与CN—结合形成配合物[(Co(CN)6]4-,其中与Co2+结合的C原子的杂化方式是
(3)NH3分子与Co2+结合成配合物[Co(NH3)6]2+,与游离的氨分子相比,其键角∠HNH
(4)Li2O的熔点为1570℃,CoO的熔点为1935℃,解释后者熔点更高的主要原因是
(5)石墨的晶胞为六方晶胞,部分晶胞参数如下图所示。若石墨的密度为d g·cm-3,以NA代表阿伏加 德罗常数的数值,则石墨中的C-C键长为

您最近一年使用:0次
2020-02-21更新
|
409次组卷
|
4卷引用:广西钦州市第四中学2022-2023学年高二下学期2月考试化学试题
广西钦州市第四中学2022-2023学年高二下学期2月考试化学试题(已下线)期末模拟预测卷02(范围:选择性必修2+选择性必修3)-2022-2023学年高二化学下学期期中期末考点大串讲(人教版2019)大教育全国名校联盟2020届高三上学期第一次质量检测理科综合化学试题(已下线)考点14 物质结构与性质(选考)-2020年高考化学命题预测与模拟试题分类精编



