名校
解题方法
1 . 氮化钛是一种导电材料,也是一种催化剂。氮化钛晶胞如图所示,A的原子坐标为 ,C的原子坐标为
,C的原子坐标为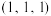 。已知:它的晶胞参数为
。已知:它的晶胞参数为 ,氮原子半径为
,氮原子半径为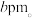 下列叙述错误的是
下列叙述错误的是
 ,C的原子坐标为
,C的原子坐标为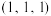 。已知:它的晶胞参数为
。已知:它的晶胞参数为 ,氮原子半径为
,氮原子半径为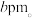 下列叙述错误的是
下列叙述错误的是
| A.基态钛原子有2个未成对电子 | B.B的原子坐标为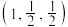 |
C.钛原子半径为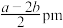 | D.氮原子的配位数为12 |
您最近一年使用:0次
名校
2 . 卤素单质及其化合物在工农业生产中有着广泛的应用。回答下列问题:
(1)类卤素 对应的酸有两种,硫氰酸(
对应的酸有两种,硫氰酸( )和异硫氰酸(
)和异硫氰酸( ):
):
①硫氰酸和异硫氰酸分子中 键和
键和 键个数之比
键个数之比___________ (填“相等”或“不相等”)。
②异硫氰酸中N的杂化轨道类型是___________ 。
③硫氰酸的电子式为___________ 。
(2) 的VSEPR模型是
的VSEPR模型是___________ , 的中心原子的价层电子对数是
的中心原子的价层电子对数是___________ 。
(3)键角:
___________ (填“>”“<”或“=”) ,判断的理由为
,判断的理由为___________ 。
(4)酸性:三氟乙酸( )
)___________ (填“>”或“<”) ,判断的理由为
,判断的理由为___________ 。
(5) 与水反应的化学方程式为
与水反应的化学方程式为___________ (该反应为非氧化还原反应)。
(1)类卤素
 对应的酸有两种,硫氰酸(
对应的酸有两种,硫氰酸( )和异硫氰酸(
)和异硫氰酸( ):
):①硫氰酸和异硫氰酸分子中
 键和
键和 键个数之比
键个数之比②异硫氰酸中N的杂化轨道类型是
③硫氰酸的电子式为
(2)
 的VSEPR模型是
的VSEPR模型是 的中心原子的价层电子对数是
的中心原子的价层电子对数是(3)键角:

 ,判断的理由为
,判断的理由为(4)酸性:三氟乙酸(
 )
) ,判断的理由为
,判断的理由为(5)
 与水反应的化学方程式为
与水反应的化学方程式为
您最近一年使用:0次
2024-04-26更新
|
196次组卷
|
2卷引用:广西壮族自治区桂林市联考2023-2024学年高二下学期3月月考化学试题
名校
解题方法
3 . 在科研和工农业生产中,硼、碳、氮、氧、磷、硫、铜等元素形成的单质及其化合物有着广泛的应用。请按要求回答下列问题:
(1)向盛有CuSO4溶液的试管中滴加少量氨水,现象是_______ ,离子反应方程式为_______ ;继续滴加氨水至过量得到深蓝色溶液;再加入乙醇后,析出深蓝色的晶体[Cu(NH3)4]SO4·H2O,其中配合物[Cu(NH3)4]SO4的配体为_______ (填化学式),中心离子为_______ 。
(2)锂-磷酸氧铜电池正极的活性物质是Cu4O(PO4)2,其中 中P原子的杂化方式为
中P原子的杂化方式为______ 。
(3)磷化硼是一种耐磨涂料,它可用作金属的表面保护层。磷化硼晶体晶胞如图所示:
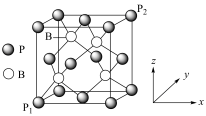
①磷原子的配位数(与磷原子距离最近且相等的硼原子数)为_______ 。
②已知图中原子坐标:P1为(0,0,0),P2为(1,1,1),则图中B的原子坐标是_______ 。
(1)向盛有CuSO4溶液的试管中滴加少量氨水,现象是
(2)锂-磷酸氧铜电池正极的活性物质是Cu4O(PO4)2,其中
 中P原子的杂化方式为
中P原子的杂化方式为(3)磷化硼是一种耐磨涂料,它可用作金属的表面保护层。磷化硼晶体晶胞如图所示:

①磷原子的配位数(与磷原子距离最近且相等的硼原子数)为
②已知图中原子坐标:P1为(0,0,0),P2为(1,1,1),则图中B的原子坐标是
您最近一年使用:0次
名校
4 . 某晶体立方晶胞如图所示。已知图中微粒1的分数坐标是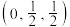 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 。下列说法正确的是
。下列说法正确的是
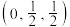 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 。下列说法正确的是
。下列说法正确的是
A. 周围距离最近且相等的 周围距离最近且相等的 个数是6 个数是6 |
B.微粒2的分数坐标是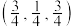 |
| C.已知银与铜位于同一族,银元素位于元素周期表的d区 |
D.若晶胞边长为a pm,则晶体密度为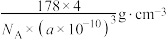 |
您最近一年使用:0次
2024-02-25更新
|
1264次组卷
|
6卷引用:广西柳州高中、南宁三中名校联盟2023-2024学年高三一轮复习诊断联考化学试题
广西柳州高中、南宁三中名校联盟2023-2024学年高三一轮复习诊断联考化学试题(已下线)专题04 物质结构与性质 元素推断-【好题汇编】2024年高考化学一模试题分类汇编(全国通用)(已下线)选择题11-14安徽省蚌埠第二中学2023-2024学年高二下学期3月月考化学试题江西省南昌市2024届高三下学期第三次模拟测试化学试题湖南省株洲市第一中学2021届高三下学期第二次模拟检测化学试题
名校
解题方法
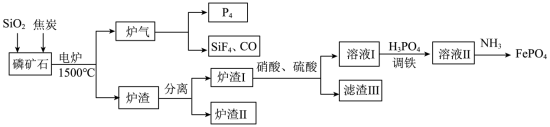
5 . “刀片电池”通过结构创新,大大提升了磷酸铁锂电池的能量密度。以下是以磷矿石(主要成分Ca5(PO4)3F,还有Fe2O3、CaCO3等杂质)为原料生产白磷(P4)同时制得刀片电池正极材料FePO4的工艺流程:
②Fe3+在pH为2.0时开始沉淀,pH为4.0时沉淀完全。
回答下列问题:
(1)白磷(P4)不溶于水但易溶于二硫化碳,说明P4是___________ (填“极性分子”或“非极性分子”)。
(2)炉渣Ⅰ主要含有铁单质及铁的磷化物,写出其中FeP溶于硝酸和硫酸的混合溶液并放出NO气体的离子方程式:___________ 。
(3)炉渣Ⅱ的主要成分是___________ 。
(4)“调铁”后须向“溶液Ⅱ”中通入氨气调节溶液的pH,将pH值控制在2.0的原因是___________ 。若此条件下Fe3+恰好完全转化为FePO4沉淀(当溶液中某离子浓度≤1×10−5mol/L时,可视为该离子沉淀完全),过滤,现往滤液中加入2mol/L的MgCl2溶液(设溶液体积增加1倍),此时溶液中___________ Mg3(PO4)2沉淀生成(填“有”或“无”或“无法确定”)【已知FePO4、Mg3(PO4)2的Ksp分别为1.3×10−22、1.0×10−24】
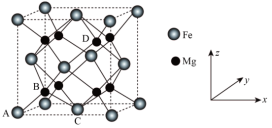
(5)储氢技术是目前化学家研究的热点之一;铁与镁形成的某种合金可用于储氢领域,其晶胞如图所示: ,
, ,
, ),C为(
),C为( ,
, ,0),则D点的坐标参数为
,0),则D点的坐标参数为___________ 。此晶胞中Fe的配位数是___________ 。
②Fe3+在pH为2.0时开始沉淀,pH为4.0时沉淀完全。
回答下列问题:
(1)白磷(P4)不溶于水但易溶于二硫化碳,说明P4是
(2)炉渣Ⅰ主要含有铁单质及铁的磷化物,写出其中FeP溶于硝酸和硫酸的混合溶液并放出NO气体的离子方程式:
(3)炉渣Ⅱ的主要成分是
(4)“调铁”后须向“溶液Ⅱ”中通入氨气调节溶液的pH,将pH值控制在2.0的原因是
(5)储氢技术是目前化学家研究的热点之一;铁与镁形成的某种合金可用于储氢领域,其晶胞如图所示:
 ,
, ,
, ),C为(
),C为( ,
, ,0),则D点的坐标参数为
,0),则D点的坐标参数为
您最近一年使用:0次
2024-02-03更新
|
732次组卷
|
3卷引用:2024届广西2024年“贵百河”高三下学期4月新高考模拟二模化学试题
23-24高三上·广西南宁·阶段练习
名校
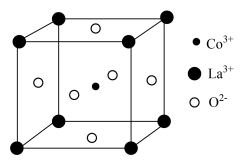
6 . 一种由镧( )、钴(
)、钴( )和氧(O)组成的三元氧化物催化剂材料,在环境保护、工业催化和光催化等领域有着广泛的应用。其晶胞结构如图所示,该立方晶胞参数为
)和氧(O)组成的三元氧化物催化剂材料,在环境保护、工业催化和光催化等领域有着广泛的应用。其晶胞结构如图所示,该立方晶胞参数为 。阿伏加德罗常数的值为
。阿伏加德罗常数的值为 。下列说法错误的是
。下列说法错误的是
 )、钴(
)、钴( )和氧(O)组成的三元氧化物催化剂材料,在环境保护、工业催化和光催化等领域有着广泛的应用。其晶胞结构如图所示,该立方晶胞参数为
)和氧(O)组成的三元氧化物催化剂材料,在环境保护、工业催化和光催化等领域有着广泛的应用。其晶胞结构如图所示,该立方晶胞参数为 。阿伏加德罗常数的值为
。阿伏加德罗常数的值为 。下列说法错误的是
。下列说法错误的是
A.晶体最简化学式为 |
B.晶体中与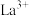 最近且距离相等的 最近且距离相等的 有6个 有6个 |
C.晶体的密度为 |
| D.晶体中相邻微粒间存在离子键 |
您最近一年使用:0次
名校
解题方法
7 . 下列关于各晶体模型示意图的分析正确的是
| 名称 |  的晶胞 的晶胞 |  的晶胞 的晶胞 | 晶体碘的晶胞 | 石墨晶体的结构 |
| 模型 示意图 | 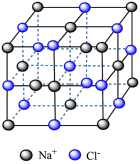 |  |  | 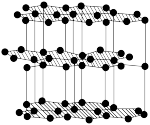 |
| 分析 | 1个 晶胞内含有6个 晶胞内含有6个 和6个 和6个 | B.Si原子的配位数为2 | C. 在晶胞中的排列有2种取向 在晶胞中的排列有2种取向 | D.石墨层与层间的主要作用力是共价键 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-08-15更新
|
407次组卷
|
3卷引用:广西大学附属中学2023-2024学年高二下学期4月月考化学试题
名校
8 . 2020年8月19日发布的《新型冠状病毒肺炎诊疗方案(试行第八版)》中指出,氯喹类药物可用于治疗新冠肺炎,其中羟基氯喹结构如图所示。
(1)羟基氯喹分子中含氧官能团的名称为_____ 。
(2)羟基氯喹分子中基态Cl原子核外电子有_____ 种空间运动状态。
(3)羟基氯喹分子中C、N、O三种元素的电负性由小到大的顺序为_____ (用元素符号表示),第一电离能由小到大的顺序为_____ (用元素符号表示)。
(4)N原子的VSEPR模型为_____ 。
(5)请在答题卡中,用*标出羟基氯喹分子中的手性碳原子_____ 。
(6)下列现代分析手段中,可用于检测羟基氯的晶体结构是_____ 。

(1)羟基氯喹分子中含氧官能团的名称为
(2)羟基氯喹分子中基态Cl原子核外电子有
(3)羟基氯喹分子中C、N、O三种元素的电负性由小到大的顺序为
(4)N原子的VSEPR模型为
(5)请在答题卡中,用*标出羟基氯喹分子中的手性碳原子
(6)下列现代分析手段中,可用于检测羟基氯的晶体结构是
| A.X射线衍射 | B.原子光谱 | C.元素分析 | D.红外光谱 |
您最近一年使用:0次
2023-04-24更新
|
652次组卷
|
3卷引用:广西大学附属中学2023-2024学年高二下学期4月月考化学试题
2022·浙江·模拟预测
解题方法
9 . 下列有关物质的结构与性质说法错误的是
A.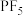 和 和 均为三角双锥结构的分子晶体,所以两者的沸点: 均为三角双锥结构的分子晶体,所以两者的沸点: |
B.工业盐酸中,因含有 而呈亮黄色 而呈亮黄色 |
C.氟的电负性大于氯,所以三氟乙酸的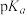 比三氯乙酸大 比三氯乙酸大 |
D.干冰中 的配位数大于冰中水分子的配位数,这与水分子间形成氢键有关 的配位数大于冰中水分子的配位数,这与水分子间形成氢键有关 |
您最近一年使用:0次
10 . 下列各项叙述中,正确的是
| A.H2O、H2S、H2Se由于分子间作用力依次增大,所以熔、沸点依次升高 |
| B.邻羟基苯甲醛的沸点比对羟基苯甲醛的沸点高 |
| C.配合物Fe(CO)n内中心原子价电子数与配体提供电子总数之和为18时,n=5 |
| D.由第ⅠA族和第ⅥA族元素形成的原子个数比为1:1、电子总数为38的化合物,是含有极性共价键的离子化合物 |
您最近一年使用:0次
2021-05-13更新
|
141次组卷
|
3卷引用:广西“贵百河”2023-2024学年高二下学期五月新高考月考测试化学试题



