2023高三·全国·专题练习
1 . FeS2晶胞为立方体,边长为 ,如图所示。
,如图所示。
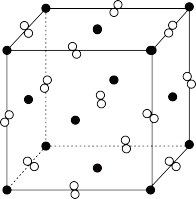
(1)①与Fe2+紧邻的阴离子个数为___________ 。
②晶胞的密度为
___________  。
。
(2)以FeS2为燃料,配合FeSO4·H2O可以制备铁粉精(FexOy)和H2SO4。结合图示解释可充分实现能源和资源有效利用的原因为___________ 。

 ,如图所示。
,如图所示。
(1)①与Fe2+紧邻的阴离子个数为
②晶胞的密度为

 。
。
(2)以FeS2为燃料,配合FeSO4·H2O可以制备铁粉精(FexOy)和H2SO4。结合图示解释可充分实现能源和资源有效利用的原因为

您最近一年使用:0次
2023高三·全国·专题练习
2 . 回答下列问题:
(1)将白色CuSO4粉末溶解于水中,溶液呈蓝色,是因为生成了一种呈蓝色的配位数是4的配离子,请写出生成此配离子的离子方程式:________ ,蓝色溶液中的阳离子内存在的全部化学键类型有_______ 。1mol该阳离子中含σ键个数为_______ 。
(2)CuSO4•5H2O(胆矾)中含有水合铜离子而呈蓝色,写出胆矾晶体中水合铜离子的结构简式(必须将配位键表示出来):________ 。
(3)向CuSO4溶液中滴加氨水会生成蓝色沉淀,再滴加氨水到沉淀刚好全部溶解可得到深蓝色溶液,继续向其中加入极性较小的乙醇可以析出深蓝色的[Cu(NH3)4]SO4•H2O晶体。下列说法不正确的是_______ (填字母)。
a.[Cu(NH3)4]SO4的组成元素中电负性最大的是N元素
b.CuSO4晶体及[Cu(NH3)4]SO4•H2O中S原子的杂化方式均为sp3
c.[Cu(NH3)4]SO4所含有的化学键有离子键、共价键和配位键
d.NH3分子内的H-N-H键角大于H2O分子内的H-O-H键角
e.SO 的空间结构为正四面体形
的空间结构为正四面体形
f.[Cu(NH3)4]2+中,N原子是配位原子
g.NH3分子中氮原子的杂化轨道类型为sp2
(1)将白色CuSO4粉末溶解于水中,溶液呈蓝色,是因为生成了一种呈蓝色的配位数是4的配离子,请写出生成此配离子的离子方程式:
(2)CuSO4•5H2O(胆矾)中含有水合铜离子而呈蓝色,写出胆矾晶体中水合铜离子的结构简式(必须将配位键表示出来):
(3)向CuSO4溶液中滴加氨水会生成蓝色沉淀,再滴加氨水到沉淀刚好全部溶解可得到深蓝色溶液,继续向其中加入极性较小的乙醇可以析出深蓝色的[Cu(NH3)4]SO4•H2O晶体。下列说法不正确的是
a.[Cu(NH3)4]SO4的组成元素中电负性最大的是N元素
b.CuSO4晶体及[Cu(NH3)4]SO4•H2O中S原子的杂化方式均为sp3
c.[Cu(NH3)4]SO4所含有的化学键有离子键、共价键和配位键
d.NH3分子内的H-N-H键角大于H2O分子内的H-O-H键角
e.SO
 的空间结构为正四面体形
的空间结构为正四面体形f.[Cu(NH3)4]2+中,N原子是配位原子
g.NH3分子中氮原子的杂化轨道类型为sp2
您最近一年使用:0次
名校
解题方法
3 . ⅤA族元素(N、P、As、Sb、Bi等)在生活中占有重要地位。请回答:
(1)叠氮酸根离子 的空间结构名称为
的空间结构名称为___________ ;中心氮原子的杂化轨道类型是___________ ;叠氮化钠 用于汽车的安全气囊中,当汽车发生剧烈碰撞时,可分解生成Na和
用于汽车的安全气囊中,当汽车发生剧烈碰撞时,可分解生成Na和 ,
, 不稳定而分解的原因是
不稳定而分解的原因是___________ 。
(2)实验室测得分子式为 的化合物有两种不同的熔点和沸点:
的化合物有两种不同的熔点和沸点:
B的结构式为___________ 。
(3)已知P可以与Cl形成多种化合物,如: 、
、 、
、 等,下列说法
等,下列说法不正确 的是___________。
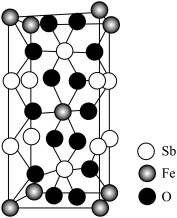
(4)Fe、Sb与O形成的某化合物晶体的晶胞如图。该化合物的化学式为___________ 。
(1)叠氮酸根离子
 的空间结构名称为
的空间结构名称为 用于汽车的安全气囊中,当汽车发生剧烈碰撞时,可分解生成Na和
用于汽车的安全气囊中,当汽车发生剧烈碰撞时,可分解生成Na和 ,
, 不稳定而分解的原因是
不稳定而分解的原因是(2)实验室测得分子式为
 的化合物有两种不同的熔点和沸点:
的化合物有两种不同的熔点和沸点:| 熔点/℃ | 沸点/℃ | |
| A |  | 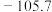 |
| B |  | 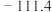 |
(3)已知P可以与Cl形成多种化合物,如:
 、
、 、
、 等,下列说法
等,下列说法A.微粒半径: |
| B.同周期中第一电离能小于P的元素有4种 |
C.根据电负性差异, 的水解产物为 的水解产物为 和 和 |
D.已知 以 以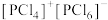 的形式存在,熔融时不导电,可推测熔融时 的形式存在,熔融时不导电,可推测熔融时 可能转化为 可能转化为 |

您最近一年使用:0次
2023-08-08更新
|
557次组卷
|
3卷引用:浙江省杭州市强基联盟2023届高三下学期2月统测化学试题
名校
解题方法
4 . 我国力争在2030年前实现“碳达峰”。2060年前实现“碳中和”的目标,因此二氧化碳的固定及转化成了重要的研究课题。
Ⅰ.在 催化作用下
催化作用下 和
和 反应生成甲醇:
反应生成甲醇: ;
;
Ⅱ.新型 水介质电池放电时,温室气体
水介质电池放电时,温室气体 被转化为储能物质
被转化为储能物质 。
。
请回答下列问题:
(1)基态Cu原子的外围电子排布式为___________ ,基态O原子核外有___________ 种不同运动状态的电子。
(2)Ⅰ中涉及的 、
、 、
、 、
、 ,属于非极性分子的是
,属于非极性分子的是___________ (填化学式)。
(3) 分子中碳原子的杂化轨道类型为
分子中碳原子的杂化轨道类型为___________ ,分子中含有的 键和
键和 键数目之比为
键数目之比为___________ 。
(4) 反应中,
反应中, 的立体构型为
的立体构型为___________ , 的沸点高于
的沸点高于 的原因是
的原因是___________ 。
(5)氧化锌(ZnO),俗称锌白,是一种常用的化学添加剂,广泛地应用于塑料、硅酸盐制品、合成橡胶等产品的制作中。一种ZnO的立方晶胞如图所示。
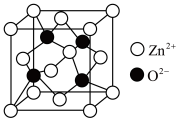
① 周围距离最近且等距的
周围距离最近且等距的 数目为
数目为___________ 。
②设晶胞边长为anm, 为阿伏加德罗常数的值,该晶体的密度为
为阿伏加德罗常数的值,该晶体的密度为___________  。
。
Ⅰ.在
 催化作用下
催化作用下 和
和 反应生成甲醇:
反应生成甲醇: ;
;Ⅱ.新型
 水介质电池放电时,温室气体
水介质电池放电时,温室气体 被转化为储能物质
被转化为储能物质 。
。请回答下列问题:
(1)基态Cu原子的外围电子排布式为
(2)Ⅰ中涉及的
 、
、 、
、 、
、 ,属于非极性分子的是
,属于非极性分子的是(3)
 分子中碳原子的杂化轨道类型为
分子中碳原子的杂化轨道类型为 键和
键和 键数目之比为
键数目之比为(4)
 反应中,
反应中, 的立体构型为
的立体构型为 的沸点高于
的沸点高于 的原因是
的原因是(5)氧化锌(ZnO),俗称锌白,是一种常用的化学添加剂,广泛地应用于塑料、硅酸盐制品、合成橡胶等产品的制作中。一种ZnO的立方晶胞如图所示。

①
 周围距离最近且等距的
周围距离最近且等距的 数目为
数目为②设晶胞边长为anm,
 为阿伏加德罗常数的值,该晶体的密度为
为阿伏加德罗常数的值,该晶体的密度为 。
。
您最近一年使用:0次
2023-07-30更新
|
929次组卷
|
4卷引用:江西省吉安市宁冈中学2023-2024学年高三上学期开学考试化学试题
解题方法
5 . 填空。
(1)N、Al、Si、Zn四种元素中,有一种元素的电离能数据如下,则该元素是___________ (填写元素符号)。
(2)请解释 的热稳定性高于
的热稳定性高于 的原因
的原因___________ 。
(3)基态氮原子核外电子的空间运动状态有___________ 种, 的键角约为107°,推测
的键角约为107°,推测 的键角
的键角___________ 107°(填“>,<或=”)。
(4)基态硅原子价层电子轨道表示式为___________ ; 与N-甲基咪唑(分子式为:
与N-甲基咪唑(分子式为: ,结构为
,结构为 )反应可以得到一种功能性螯合物。则:C、N、H三种非金属元素的电负性由大到小的顺序是
)反应可以得到一种功能性螯合物。则:C、N、H三种非金属元素的电负性由大到小的顺序是___________ ,1个N-甲基咪唑分子中含有___________ 个 键。
键。
(5)已知周期表中存在对角相似规则,如Be与Al在周期表中处于对角线位置则化学性质相似,Be的氧化物、氢氧化物也有两性,写出Be的氢氧化物与氢氧化钠反应的化学方程式___________ 。
(1)N、Al、Si、Zn四种元素中,有一种元素的电离能数据如下,则该元素是
| 电离能 |  |  |  |  | …… |
 | 578 | 1817 | 2745 | 11575 | …… |
 的热稳定性高于
的热稳定性高于 的原因
的原因(3)基态氮原子核外电子的空间运动状态有
 的键角约为107°,推测
的键角约为107°,推测 的键角
的键角(4)基态硅原子价层电子轨道表示式为
 与N-甲基咪唑(分子式为:
与N-甲基咪唑(分子式为: ,结构为
,结构为 )反应可以得到一种功能性螯合物。则:C、N、H三种非金属元素的电负性由大到小的顺序是
)反应可以得到一种功能性螯合物。则:C、N、H三种非金属元素的电负性由大到小的顺序是 键。
键。(5)已知周期表中存在对角相似规则,如Be与Al在周期表中处于对角线位置则化学性质相似,Be的氧化物、氢氧化物也有两性,写出Be的氢氧化物与氢氧化钠反应的化学方程式
您最近一年使用:0次
2023-03-28更新
|
693次组卷
|
3卷引用:山东省济宁市微山县第二中学2023-2024学年高三上学期第三次月考化学试题
名校
6 . 方钴矿化合物是典型的热电材料,在环境污染和能源危机日益严重的今天,进行新型热电材料的研究具有很强的现实意义。
(1)Brian Sales等研究了一类新型热电材料,叫作填隙方钴矿锑化物,在钴和锑形成的晶体空隙中填充入稀土原子La(如图所示),该化合物的化学式为_______ 。

(2)Co和Fe的逐级电离能数据如表,Fe的 大于Co的原因是
大于Co的原因是_______ 。
(3)已知 的熔点73℃,沸点223.5℃,
的熔点73℃,沸点223.5℃, 的熔点是735℃,沸点是1049℃。两者的熔沸点差异较大的原因是
的熔点是735℃,沸点是1049℃。两者的熔沸点差异较大的原因是_______ 。预测 的空间构型为
的空间构型为_______ 。
(4)为更好地理解超酸的强酸性,实验小组查阅相关资料了解得:混合超强酸 显强酸性的原因是氟化氢提供
显强酸性的原因是氟化氢提供 和离子
和离子 ,氟离子通过强配位键与
,氟离子通过强配位键与 生成稳定结构的四氟化硼阴离子,于是
生成稳定结构的四氟化硼阴离子,于是 就成为了“自由质子”,从而导致整合体系具有非常强的酸性。以此类推,魔酸(
就成为了“自由质子”,从而导致整合体系具有非常强的酸性。以此类推,魔酸( )是最早发现的超强酸,其中Sb采取
)是最早发现的超强酸,其中Sb采取_______ 杂化方式,S采取_______ 杂化方式。
(1)Brian Sales等研究了一类新型热电材料,叫作填隙方钴矿锑化物,在钴和锑形成的晶体空隙中填充入稀土原子La(如图所示),该化合物的化学式为

(2)Co和Fe的逐级电离能数据如表,Fe的
 大于Co的原因是
大于Co的原因是| 元素 |  |  |  |  | 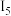 | …… |
| Fe | 462.5 | 1561.9 | 2957 | 5290 | 7240 | |
 | 760.4 | 1648 | 3232 | 4950 | 7670 |
 的熔点73℃,沸点223.5℃,
的熔点73℃,沸点223.5℃, 的熔点是735℃,沸点是1049℃。两者的熔沸点差异较大的原因是
的熔点是735℃,沸点是1049℃。两者的熔沸点差异较大的原因是 的空间构型为
的空间构型为(4)为更好地理解超酸的强酸性,实验小组查阅相关资料了解得:混合超强酸
 显强酸性的原因是氟化氢提供
显强酸性的原因是氟化氢提供 和离子
和离子 ,氟离子通过强配位键与
,氟离子通过强配位键与 生成稳定结构的四氟化硼阴离子,于是
生成稳定结构的四氟化硼阴离子,于是 就成为了“自由质子”,从而导致整合体系具有非常强的酸性。以此类推,魔酸(
就成为了“自由质子”,从而导致整合体系具有非常强的酸性。以此类推,魔酸( )是最早发现的超强酸,其中Sb采取
)是最早发现的超强酸,其中Sb采取
您最近一年使用:0次
2022-11-10更新
|
164次组卷
|
2卷引用:山东省菏泽市2022-2023学年高三上学期期中联考化学(A卷)试题
名校
解题方法
7 . C和Si元素在化学中占有极其重要的地位。
(1)写出Si的基态原子核外最外层电子排布式_______ ,C、O、Si三种元素的电负性由大到小的顺序为_______ 。
(2)干冰是分子晶体,其密度比冰大的原因是_______ 。SiC晶体的结构与晶体硅的相似,其中C原子的杂化方式为_______ 。
(3)氧化物XO的电子总数与SiC的相等,则X为_______ (填元素符号),XO是优良的耐高温材料,其熔点比CaO高的原因是_______ 。
(4)向盛有硫酸铜水溶液的试管中加氨水,先形成蓝色沉淀,继续加入氨水沉淀溶解,得到深蓝色透明溶液。在这个过程中先生成蓝色沉淀,后沉淀溶解的原因是:_______ 。
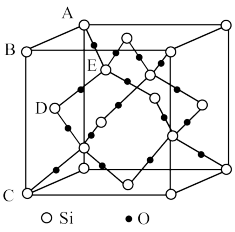
(5)下图表示的是SiO2的晶胞结构(白圈代表硅原子,黑点代表氧原子),判断在30g二氧化硅晶体中含_______ 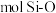 键。如果该立方体的边长为
键。如果该立方体的边长为 ,用
,用 表示阿伏加德罗常数,则SiO2晶体的密度表达式为
表示阿伏加德罗常数,则SiO2晶体的密度表达式为_______  。
。
(1)写出Si的基态原子核外最外层电子排布式
(2)干冰是分子晶体,其密度比冰大的原因是
(3)氧化物XO的电子总数与SiC的相等,则X为
(4)向盛有硫酸铜水溶液的试管中加氨水,先形成蓝色沉淀,继续加入氨水沉淀溶解,得到深蓝色透明溶液。在这个过程中先生成蓝色沉淀,后沉淀溶解的原因是:
(5)下图表示的是SiO2的晶胞结构(白圈代表硅原子,黑点代表氧原子),判断在30g二氧化硅晶体中含
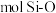 键。如果该立方体的边长为
键。如果该立方体的边长为 ,用
,用 表示阿伏加德罗常数,则SiO2晶体的密度表达式为
表示阿伏加德罗常数,则SiO2晶体的密度表达式为 。
。
您最近一年使用:0次
2022-10-30更新
|
1740次组卷
|
3卷引用:宁夏银川市第六中学2022-2023学年高三上学期第二次月考化学试题
解题方法
8 . 锗的团簇化合物
含锗化合物A的分子式可以表示为 ,R为三异丙基硅基。该化合物中存在两种锗锗键,键长分别为
,R为三异丙基硅基。该化合物中存在两种锗锗键,键长分别为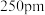 和
和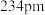 。A的合成方法如下:控制
。A的合成方法如下:控制 与
与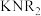 按
按 计量反应生成B,B被金属钾还原得到A。在B转化为A的过程中,可能经过中间产物C,C中含两个锗原子;C与B按
计量反应生成B,B被金属钾还原得到A。在B转化为A的过程中,可能经过中间产物C,C中含两个锗原子;C与B按 计量反应得到环状化合物D,D与C在金属钾还原下反应得到A。若B与吡啶按
计量反应得到环状化合物D,D与C在金属钾还原下反应得到A。若B与吡啶按 计量反应则得到E,E难以与金属钾进一步反应生成A。化合物
计量反应则得到E,E难以与金属钾进一步反应生成A。化合物 中锗原子均满足8电子。
中锗原子均满足8电子。
(1)画出 的结构图。要求:如有锗锗键,须示出化学键是单键、双键还是三键;须示出A中团簇的立体结构。用R表示三异丙基硅基。A:
的结构图。要求:如有锗锗键,须示出化学键是单键、双键还是三键;须示出A中团簇的立体结构。用R表示三异丙基硅基。A:______ ;B:______ ;C:______ ;D:______ ;E:______ ;
(2)简述E难以进一步反应转化为A的原因。______
含锗化合物A的分子式可以表示为
 ,R为三异丙基硅基。该化合物中存在两种锗锗键,键长分别为
,R为三异丙基硅基。该化合物中存在两种锗锗键,键长分别为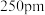 和
和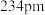 。A的合成方法如下:控制
。A的合成方法如下:控制 与
与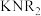 按
按 计量反应生成B,B被金属钾还原得到A。在B转化为A的过程中,可能经过中间产物C,C中含两个锗原子;C与B按
计量反应生成B,B被金属钾还原得到A。在B转化为A的过程中,可能经过中间产物C,C中含两个锗原子;C与B按 计量反应得到环状化合物D,D与C在金属钾还原下反应得到A。若B与吡啶按
计量反应得到环状化合物D,D与C在金属钾还原下反应得到A。若B与吡啶按 计量反应则得到E,E难以与金属钾进一步反应生成A。化合物
计量反应则得到E,E难以与金属钾进一步反应生成A。化合物 中锗原子均满足8电子。
中锗原子均满足8电子。(1)画出
 的结构图。要求:如有锗锗键,须示出化学键是单键、双键还是三键;须示出A中团簇的立体结构。用R表示三异丙基硅基。A:
的结构图。要求:如有锗锗键,须示出化学键是单键、双键还是三键;须示出A中团簇的立体结构。用R表示三异丙基硅基。A:(2)简述E难以进一步反应转化为A的原因。
您最近一年使用:0次
解题方法
9 . “嫦娥五号”首次实现了我国地外天体采样返回,它的成功发射标志着我国航天技术向前迈出了一大步,其制造材料中包含了Cu、Ti、Cr、Ni、Si、N、O等多种元素。回答下列问题:
(1)基态 的价电子排布式为
的价电子排布式为_______ , 溶于氨水的化学方程式为
溶于氨水的化学方程式为_______ 。
(2)Cu催化烯烃硝化反应过程中会产生 。
。 、
、 中氨原子的杂化方式分别为
中氨原子的杂化方式分别为_______ ,键角:
_______ (填“<”或“>”) 。
。
(3)三价铬离子能形成多种配位化合物。 中,提供电子对形成配位键的元素是
中,提供电子对形成配位键的元素是_______ ,中心离子的配位数为_______ 。
(1)基态
 的价电子排布式为
的价电子排布式为 溶于氨水的化学方程式为
溶于氨水的化学方程式为(2)Cu催化烯烃硝化反应过程中会产生
 。
。 、
、 中氨原子的杂化方式分别为
中氨原子的杂化方式分别为
 。
。(3)三价铬离子能形成多种配位化合物。
 中,提供电子对形成配位键的元素是
中,提供电子对形成配位键的元素是
您最近一年使用:0次
解题方法
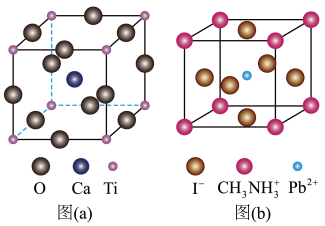
10 . 一种立方钙钛矿结构的金属卤化物光电材料的组成为 、
、 和有机碱离子
和有机碱离子 ,其晶胞如图(b)所示。其中
,其晶胞如图(b)所示。其中 与图(a)中
与图(a)中_______ 的空间位置相同,有机碱 中,N原子的杂化轨道类型是
中,N原子的杂化轨道类型是_______ ;若晶胞参数为anm,则晶体密度为_______  (列出计算式,设
(列出计算式,设 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
 、
、 和有机碱离子
和有机碱离子 ,其晶胞如图(b)所示。其中
,其晶胞如图(b)所示。其中 与图(a)中
与图(a)中 中,N原子的杂化轨道类型是
中,N原子的杂化轨道类型是 (列出计算式,设
(列出计算式,设 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
您最近一年使用:0次



