名校
解题方法
1 . 元素周期表与元素周期律在学习、研究和生产实践中有很重要的作用。下表列出了a~g7种元素在周期表中的位置。
(1)a的元素符号是_______ 。
(2)b、c的最高价氧化物对应的水化物(氢氧化物)中,碱性较弱的是_______ 。
(3)非金属性e强于g,用原子结构解释原因:_______ ,得电子能力e大于g。
(4)下列对f及其化合物的推断中,正确的是_______ (填序号)。
①f的最高化合价为+6价
②f的氢化物的稳定性弱于d的氢化物的稳定性
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
| 2 | a | |||||||
| 3 | b | c | d | e | ||||
| 4 | f | g |
(2)b、c的最高价氧化物对应的水化物(氢氧化物)中,碱性较弱的是
(3)非金属性e强于g,用原子结构解释原因:
(4)下列对f及其化合物的推断中,正确的是
①f的最高化合价为+6价
②f的氢化物的稳定性弱于d的氢化物的稳定性
您最近一年使用:0次
解题方法
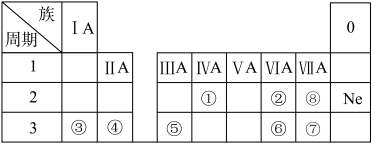
2 . 下表是元素周期表的一部分,除标出的元素外,表中的每个编号代表一种元素,请根据要求回答问题:
①___________ ;⑤___________ ;⑦___________ ;⑧___________ 。
(2)②和③元素所组成的化合物中可做供氧剂的是___________ (写化学式)。
(3)⑥元素的原子结构示意图为___________ 。②元素的原子结构示意图为___________ 。
(4)①元素的氧化物中是酸性氧化物的是___________ (写化学式)。
①
(2)②和③元素所组成的化合物中可做供氧剂的是
(3)⑥元素的原子结构示意图为
(4)①元素的氧化物中是酸性氧化物的是
您最近一年使用:0次
解题方法
3 . 下表为长式元素周期表的主要部分。①~⑬代表13种元素,⑭表示元素周期表中某一区域。
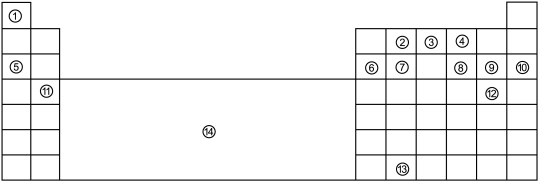
请回答:
(1)①、②、④的原子半径从大到小排列的顺序是______ 。(填化学式)
(2)①与③组成的含10个电子的阳离子的化学式是______ 。
(3)有些族的元素有特别的名称,⑨所在主族的元素叫做______ 元素。
(4)⑩的元素符号是______ 。
(5)⑪的元素名称是______ 。
(6)⑫的原子结构示意图是______ 。
(7)⑬在元素周期表中的位置是______ 。
(8)下列说法不正确 的是______ 。
A. ②的原子所含原子数即
②的原子所含原子数即 任何粒子的粒子数
任何粒子的粒子数
B.⑥、⑦的氧化物均能与⑤的最高价氧化物对应水化物反应
C.⑧的某种氧化物进入大气会形成酸雨
D.⑨的某种氧化物可用于自来水消毒
E.⑭所示区域内的元素常见于农药中
(9)⑥的单质与 溶液反应的化学方程式是
溶液反应的化学方程式是______ 。

请回答:
(1)①、②、④的原子半径从大到小排列的顺序是
(2)①与③组成的含10个电子的阳离子的化学式是
(3)有些族的元素有特别的名称,⑨所在主族的元素叫做
(4)⑩的元素符号是
(5)⑪的元素名称是
(6)⑫的原子结构示意图是
(7)⑬在元素周期表中的位置是
(8)下列说法
A.
 ②的原子所含原子数即
②的原子所含原子数即 任何粒子的粒子数
任何粒子的粒子数B.⑥、⑦的氧化物均能与⑤的最高价氧化物对应水化物反应
C.⑧的某种氧化物进入大气会形成酸雨
D.⑨的某种氧化物可用于自来水消毒
E.⑭所示区域内的元素常见于农药中
(9)⑥的单质与
 溶液反应的化学方程式是
溶液反应的化学方程式是
您最近一年使用:0次
解题方法
4 . 下表是元素周期表的一部分,请针对表中所列标号为①~⑩的元素回答以下问题。
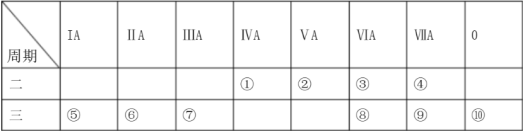
(1)非金属性最强的元素是___________ (填元素符号,下同),最外层电子数是次外层电子数2倍的元素是___________ ,这种元素的一种同位素可用于测定文物年代,这种同位素的符号是___________ 。
(2)与⑥同主族的下一周期的元素是___________ (填元素符号),它在元素周期表中的位置是___________ ,请写出它的原子结构示意图___________ 。
(3)请写出⑦的单质与碱液反应的离子方程式___________ 。

(1)非金属性最强的元素是
(2)与⑥同主族的下一周期的元素是
(3)请写出⑦的单质与碱液反应的离子方程式
您最近一年使用:0次
2024-04-03更新
|
85次组卷
|
2卷引用:四川省雅安市名山区第三中学2023-2024学年高一12月月考化学试题
5 . 金属铜被广泛应用于电气、电子等领域。因原料和工艺不同,铜的冶炼主要有火法冶炼与湿法冶炼两种技术路线。
(1)铜元素位于元素周期表的
(2)基态Cu原子的核外电子排布式_______ 。
(1)铜元素位于元素周期表的
| A.s区 | B.p区 | C.ds区 | D.f区 |
您最近一年使用:0次
名校
6 . 1869年俄国化学家门捷列夫制出第一张元素周期表,到现在形成的周期表经过了众多化学家的艰辛努力。元素周期表体现了元素位构性的关系,揭示了元素间的内在联系,下图是元素周期表的一部分,回答下列问题:
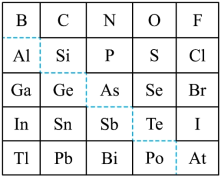
(1)元素Ga在元素周期表中的位置为:______ ;
(2)Sn的最高正价为______ ,C1的最高价氧化物对应水化物的化学式为______ ;
(3)根据元素周期律,推断
①表中元素形成的氢化物中热稳定性最高的是______ (写化学式),其电子式为______ 。
②H3AsO4、H2SeO4的酸性强弱为:H3AsO4______ H2SeO4(填“>”、<”、“=”或“无法比较”);
③氢化物的还原性:H2O______ H2S(填“>”、“<”、“=”或“无法比较”)。
④原子半径比较:N______ Si(填“>”、“<”、“=”或“无法比较”)。

(1)元素Ga在元素周期表中的位置为:
(2)Sn的最高正价为
(3)根据元素周期律,推断
①表中元素形成的氢化物中热稳定性最高的是
②H3AsO4、H2SeO4的酸性强弱为:H3AsO4
③氢化物的还原性:H2O
④原子半径比较:N
您最近一年使用:0次
名校
7 . 1869年俄国化学家门捷列夫制出第一张元素周期表,到现在形成的元素周期表经过了众多化学家的艰辛努力,历经142年。元素周期表体现了元素位、构。性的关系,揭示了元素间的内在联系。如图是元素周期表的一部分,回答下列问题:
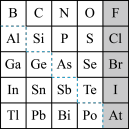
(1) 的结构示意图是
的结构示意图是___________ 。
(2)元素In在元素周期表中的位置是___________ 。
(3)P的最高价氧化物的化学式为___________ ,Al元素的最高价氧化物对应的水化物与S元素的最高价氧化物对应的水化物发生反应的离子方程式是___________ 。
(4) 的中子数与电子数的差值是
的中子数与电子数的差值是___________ ;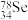 和
和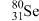 的物理性质
的物理性质___________ (填“相同”或“不同”),化学性质___________ (填“相同”或“不同”)。
(5)根据元素周期律及事实推断:
①在溶液中下列反应能发生的是___________ 。
A.
B.
C.
②氢化物的还原性:
___________  (填“>”或“<”)。
(填“>”或“<”)。

(1)
 的结构示意图是
的结构示意图是(2)元素In在元素周期表中的位置是
(3)P的最高价氧化物的化学式为
(4)
 的中子数与电子数的差值是
的中子数与电子数的差值是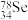 和
和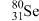 的物理性质
的物理性质(5)根据元素周期律及事实推断:
①在溶液中下列反应能发生的是
A.

B.

C.

②氢化物的还原性:

 (填“>”或“<”)。
(填“>”或“<”)。
您最近一年使用:0次
8 . 核外电子排布与元素周期表的分区
按电子排布式中最后填入电子的_______ 可将元素周期表分为s、p、d、f4个区,而IB、IIB族这2个纵行的元素的核外电子可理解为先填满了_______ 能级而后再填充_______ 能级而得名ds区。5个区的位置关系如下图所示:
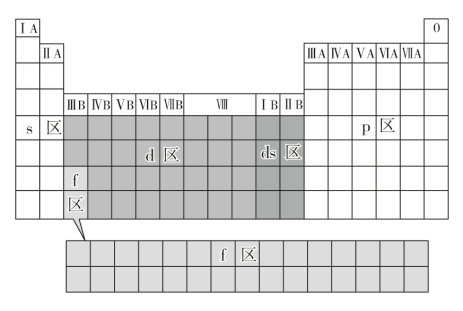
按电子排布式中最后填入电子的

您最近一年使用:0次
名校
解题方法
9 . 如图为元素周期表的一部分,请根据元素①~⑧在表中的位置,回答下列问题:

(1)请写出元素⑦在元素周期表中的位置___________ 。在上述元素的最高价氧化物对应的水化物中,酸性最强的是___________ (用化学式表示)。
(2)由元素①、④、⑤形成的化合物的电子式为___________ ,该物质属于___________ (填“离子”或“共价”)化合物。
(3)③、④、⑤、⑥的简单离子半径由大到小的顺序是___________ (用离子符号表示)。
(4)在发生地震后,地震灾区需要大量的“84消毒液”来消毒杀菌。84消毒液(主要成分为NaClO)和洁厕灵(主要成分为盐酸)混合使用会产生一种有毒气体,写出两者混合时发生反应的离子方程式:___________ 。
(5)由表中元素形成的常见无机化合物A、B、C、X有以下转化关系:
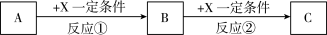
若A、B、C含同一金属元素,X为电解质溶液,可电离出 ,所有反应都在溶液中进行。B的化学式为
,所有反应都在溶液中进行。B的化学式为___________ ,X的化学式为___________ 。

(1)请写出元素⑦在元素周期表中的位置
(2)由元素①、④、⑤形成的化合物的电子式为
(3)③、④、⑤、⑥的简单离子半径由大到小的顺序是
(4)在发生地震后,地震灾区需要大量的“84消毒液”来消毒杀菌。84消毒液(主要成分为NaClO)和洁厕灵(主要成分为盐酸)混合使用会产生一种有毒气体,写出两者混合时发生反应的离子方程式:
(5)由表中元素形成的常见无机化合物A、B、C、X有以下转化关系:

若A、B、C含同一金属元素,X为电解质溶液,可电离出
 ,所有反应都在溶液中进行。B的化学式为
,所有反应都在溶液中进行。B的化学式为
您最近一年使用:0次
解题方法
10 . 回答下列问题。
(1)下表是元素周期表的一部分,将 Na、Mg、Al 三种元素填入相应位置。___________
(2)Na、Mg、Al这三种元素中,原子半径由大到小的顺序是___________ 。
(3)由于金属离子的氧化性强弱存在差异,使得它们被还原为单质的难易程度不同,因此金属冶炼的方法不同,活泼金属常用电解法冶炼。下列金属需要使用电解法冶炼的是___________。
(1)下表是元素周期表的一部分,将 Na、Mg、Al 三种元素填入相应位置。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 一 | ||||||||
| 二 | ||||||||
| 三 | ||||||||
(2)Na、Mg、Al这三种元素中,原子半径由大到小的顺序是
(3)由于金属离子的氧化性强弱存在差异,使得它们被还原为单质的难易程度不同,因此金属冶炼的方法不同,活泼金属常用电解法冶炼。下列金属需要使用电解法冶炼的是___________。
| A.Na | B.Fe | C.Cu | D.Au |
您最近一年使用:0次



