解题方法
1 . 人体必需的一些元素在周期表中的分布情况如下:
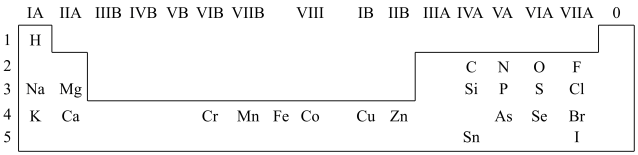
(1)请在上图中画出金属与非金属的分界线______ 。
(2)Na与O形成的原子个数比为1:1的化合物所含的化学键类型为______ 。
(3)锡(Sn)与C为同一主族元素,Sn原子比C原子多三个电子层,则Sn的原子序数为______ 。
(4)X射线衍射法可以测定某些分子的结构,下列分子结构模型中正确是______ (填字母)。
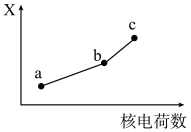
(5)前四周期同族元素的某种性质X随核电荷数的变化趋势如图所示,则下列说法正确的是______(填字母)。
(6)某小组为探究 、
、 、
、 的氧化性强弱,设计实验如下:
的氧化性强弱,设计实验如下:
资料:稀溴水呈黄色;浓溴水呈红棕色;碘水呈棕黄色。
实验②观察到的现象是______ ,甲同学根据此现象得出结论:氧化性 。乙同学认为实验②不能充分证明氧化性
。乙同学认为实验②不能充分证明氧化性 ,其理由是
,其理由是______ 。试从原子结构的角度解释卤素单质的氧化性递变规律:同一主族元素从上到下,______ ,因此,元素的非金属性逐渐减弱,对应的单质的氧化性逐渐减弱。

(1)请在上图中画出金属与非金属的分界线
(2)Na与O形成的原子个数比为1:1的化合物所含的化学键类型为
(3)锡(Sn)与C为同一主族元素,Sn原子比C原子多三个电子层,则Sn的原子序数为
(4)X射线衍射法可以测定某些分子的结构,下列分子结构模型中正确是
| A | B | C | D |
| HCl | H₂O | CO₂ | CH₄ |
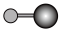 | 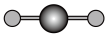 | 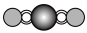 | 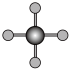 |
| 直线形 | 直线形 | 直线形 | 平面正方形 |
(5)前四周期同族元素的某种性质X随核电荷数的变化趋势如图所示,则下列说法正确的是______(填字母)。

| A.若a、b、c表示碱金属元素,则X表示对应单质的密度 |
| B.若a、b、c表示卤族元素,则X表示对应简单离子的还原性 |
| C.若a、b、c表示第ⅥA族元素,则X表示对应氢化物的稳定性 |
| D.若a、b、c表示第ⅡA族元素,则X表示最高价氧化物对应水化物的碱性 |
(6)某小组为探究
 、
、 、
、 的氧化性强弱,设计实验如下:
的氧化性强弱,设计实验如下:资料:稀溴水呈黄色;浓溴水呈红棕色;碘水呈棕黄色。
| 序号 | 实验① | 实验② |
| 实验操作 |  |  |
| 现象 | 溶液变为黄色 |
 。乙同学认为实验②不能充分证明氧化性
。乙同学认为实验②不能充分证明氧化性 ,其理由是
,其理由是
您最近一年使用:0次
名校
解题方法
2 . 为纪念元素周期表诞生150周年,IUPAC等向世界介绍了118位优秀青年化学家,并形成一张“青年化学家元素周期表”。中国学者雷晓光、姜雪峰、刘庄分别成为“ ,
, 、
、 ”元素的代言人。回答下列问题:
”元素的代言人。回答下列问题:
(1)根据汞的原子结构示意图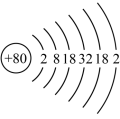 判断,汞在第
判断,汞在第___________ 周期。工业上冶炼金属汞的方法为___________ 。
(2)硒(Se)与硫位于同一主族,均是生命必需元素。下列推断不正确的是___________ 。
A.硒元素的最低负化合价为 价
价
B.还原性: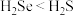
C.二氧化硒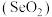 具有还原性
具有还原性
(3)氮是自然界各种生物体生命活动不可缺少的重要元素,磷(P)、砷(As)也是氮族元素。
①砷有多种同位素原子,其中稳定的核素是 ,它的中子数为
,它的中子数为___________ 。
②已知 与
与 的性质相似,则对
的性质相似,则对 性质的推测正确的是
性质的推测正确的是___________ 。
A.含有离子键和共价键
B.能与 溶液反应
溶液反应
C.加热充分分解时与 分解产物的种类完全一样
分解产物的种类完全一样
③下列关于第ⅤA族元素及其化合物的说法正确的是___________ 。
A.热稳定性:
B.As的氧化物的水化物是强碱
C.简单离子半径随原子序数递增而增大
(4)砷酸 可用于制造杀虫剂、药物等。
可用于制造杀虫剂、药物等。 溶于稀硝酸中可得砷酸,此反应的化学方程式为
溶于稀硝酸中可得砷酸,此反应的化学方程式为___________ 。
 ,
, 、
、 ”元素的代言人。回答下列问题:
”元素的代言人。回答下列问题:(1)根据汞的原子结构示意图
 判断,汞在第
判断,汞在第(2)硒(Se)与硫位于同一主族,均是生命必需元素。下列推断不正确的是
A.硒元素的最低负化合价为
 价
价B.还原性:
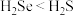
C.二氧化硒
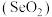 具有还原性
具有还原性(3)氮是自然界各种生物体生命活动不可缺少的重要元素,磷(P)、砷(As)也是氮族元素。
①砷有多种同位素原子,其中稳定的核素是
 ,它的中子数为
,它的中子数为②已知
 与
与 的性质相似,则对
的性质相似,则对 性质的推测正确的是
性质的推测正确的是A.含有离子键和共价键
B.能与
 溶液反应
溶液反应C.加热充分分解时与
 分解产物的种类完全一样
分解产物的种类完全一样③下列关于第ⅤA族元素及其化合物的说法正确的是
A.热稳定性:

B.As的氧化物的水化物是强碱
C.简单离子半径随原子序数递增而增大
(4)砷酸
 可用于制造杀虫剂、药物等。
可用于制造杀虫剂、药物等。 溶于稀硝酸中可得砷酸,此反应的化学方程式为
溶于稀硝酸中可得砷酸,此反应的化学方程式为
您最近一年使用:0次
2024-02-11更新
|
144次组卷
|
3卷引用:安徽省合肥市一中2023-2024学年高三上学期第二次教学质量检测化学试题
名校
解题方法
3 . 人体必需的一些元素在周期表中的分布情况如下:______ 。 是一种绿色氧化剂,电子式为
是一种绿色氧化剂,电子式为________ 。
(2)钠离子和氯离子可以帮助我们维持机体的电解质平衡。常温下,将 通入水中,可以得到一种具有漂白性的分子,写出它的结构式
通入水中,可以得到一种具有漂白性的分子,写出它的结构式________ 。
(3)硒(Se)具有抗氧化、增强人体抵抗力的功效。Se在元素周期表中的位置是________ ,原子序数为____ 。
(4)铁、铬、锰在人体内含量微乎其微,但对维持内分泌平衡和身体基础代谢有重要作用。向少量酸性 溶液中加入
溶液中加入 溶液,发生反应的离子方程式为
溶液,发生反应的离子方程式为___________ 。
(5)前四周期同族元素的某种性质X随核电荷数的变化趋势如图所示,则下列说法正确的是_______(填字母)。

 是一种绿色氧化剂,电子式为
是一种绿色氧化剂,电子式为(2)钠离子和氯离子可以帮助我们维持机体的电解质平衡。常温下,将
 通入水中,可以得到一种具有漂白性的分子,写出它的结构式
通入水中,可以得到一种具有漂白性的分子,写出它的结构式(3)硒(Se)具有抗氧化、增强人体抵抗力的功效。Se在元素周期表中的位置是
(4)铁、铬、锰在人体内含量微乎其微,但对维持内分泌平衡和身体基础代谢有重要作用。向少量酸性
 溶液中加入
溶液中加入 溶液,发生反应的离子方程式为
溶液,发生反应的离子方程式为(5)前四周期同族元素的某种性质X随核电荷数的变化趋势如图所示,则下列说法正确的是_______(填字母)。
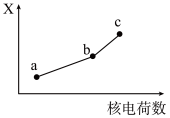
| A.若a、b、c表示氧族元素,则X表示对应氢化物的沸点 |
| B.若a、b、c表示卤族元素,则X表示对应简单离子的还原性 |
| C.若a、b、c表示第ⅠA族元素,则X表示对应离子的氧化性 |
| D.若a、b、c表示第ⅡA族元素,则X表示最高价氧化物对应水化物的碱性 |
您最近一年使用:0次
2024-01-24更新
|
71次组卷
|
2卷引用:山东省邹城市第二中学2023-2024学年高一上学期12月月考化学试题
名校
4 . 下列说法是否正确(正确的打“√”,不正确的打“×”)若不正确请说明理由。
(1)元素周期表中每一横行称为一周期,每一纵列称为一个族。_________ ;
(2)FeCl3与Cu的反应为置换反应。_________ ;
(3)1 mol Na2O溶于水中形成1 L溶液,所得溶液的物质的量浓度为1 mol/L。_________ ;
(4)镧镍合金能大量吸收H2形成金属氢化物,可作储氢材料。_________
(1)元素周期表中每一横行称为一周期,每一纵列称为一个族。
(2)FeCl3与Cu的反应为置换反应。
(3)1 mol Na2O溶于水中形成1 L溶液,所得溶液的物质的量浓度为1 mol/L。
(4)镧镍合金能大量吸收H2形成金属氢化物,可作储氢材料。
您最近一年使用:0次
名校
解题方法
5 . 海洋是资源的宝库,蕴藏着丰富的氯、溴、碘等元素。氯、溴、碘是典型的非金属元素,都能与大多数金属化合生成盐,故统称为卤素;卤素单质都具有氧化性。
(1)氯在元素周期表中的位置___________
(2)氯气是重要的化工产品,工业可以由电解氯化钠溶液得到,同时还生成NaOH和H2.写出该电解过程的离子方程式___________
(3)氰(CN)2、硫氰(SCN)2的化学性质和卤素(X2)很相似,化学上称为拟卤素,它们阴离子的还原性强弱顺序为: 。试写出:在NaBr和KSCN的混合溶液中滴加少量(CN)2,请写出发生反应的离子方程式
。试写出:在NaBr和KSCN的混合溶液中滴加少量(CN)2,请写出发生反应的离子方程式___________ 。
(4)NaNO2因外观和食盐相似,又有咸味,容易使人误食中毒。已知NaNO2能发生如下反应: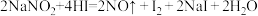
Ⅰ.上述反应的还原剂是___________
Ⅱ.根据上述反应,鉴别某白色固体是NaNO2还是NaCl。可选用的物质有:①水 ②淀粉碘化钾试纸 ③淀粉溶液 ④白酒 ⑤食醋(稀的醋酸溶液),你认为必须选用的物质有___________ (填字母)。
A.③⑤ B.①②⑤ C.①②④
Ⅲ.某厂废液中,含有2%~5%的NaNO2直接排放会造成污染,下列试剂能使NaNO2转化为N2防止污染的是___________ 。(填字母)
A.NaCl B. C.
C. D.浓
D.浓
(1)氯在元素周期表中的位置
(2)氯气是重要的化工产品,工业可以由电解氯化钠溶液得到,同时还生成NaOH和H2.写出该电解过程的离子方程式
(3)氰(CN)2、硫氰(SCN)2的化学性质和卤素(X2)很相似,化学上称为拟卤素,它们阴离子的还原性强弱顺序为:
 。试写出:在NaBr和KSCN的混合溶液中滴加少量(CN)2,请写出发生反应的离子方程式
。试写出:在NaBr和KSCN的混合溶液中滴加少量(CN)2,请写出发生反应的离子方程式(4)NaNO2因外观和食盐相似,又有咸味,容易使人误食中毒。已知NaNO2能发生如下反应:
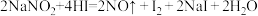
Ⅰ.上述反应的还原剂是
Ⅱ.根据上述反应,鉴别某白色固体是NaNO2还是NaCl。可选用的物质有:①水 ②淀粉碘化钾试纸 ③淀粉溶液 ④白酒 ⑤食醋(稀的醋酸溶液),你认为必须选用的物质有
A.③⑤ B.①②⑤ C.①②④
Ⅲ.某厂废液中,含有2%~5%的NaNO2直接排放会造成污染,下列试剂能使NaNO2转化为N2防止污染的是
A.NaCl B.
 C.
C. D.浓
D.浓
您最近一年使用:0次
名校
解题方法
6 . 若某非金属元素X的最高价氧化物对应的水化物的化学式为HnXOm,则X元素的族序数为______ ,它的最高价氧化物的化学式为______ ,氢化物的化学式为______ 。
您最近一年使用:0次
解题方法
7 . 下表列出了9种元素在元素周期表中的位置示意图。
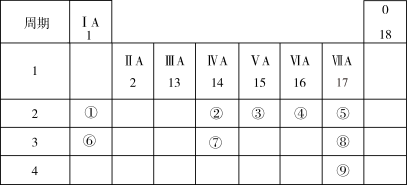
请回答下列问题:
(1)考古工作者利用元素②的一种核素测定一些文物的年代,这种核素的符号是_______________ 。
(2)画出元素⑧形成的简单离子的结构示意图_______________ 。
(3)写出元素④和⑥的单质在加热条件下反应,所得产物的电子式为_______________ 。
(4)⑥元素的最高价氧化物对应的水化物含有的化学键是_______________ 。
(5)②、③、④、⑤四种元素的简单气态氢化物中,稳定性最强的是______________ (填化学式),写出元素⑤的单质与水反应的化学方程式_______________ ,写出一个能证明元素⑧比元素⑨非金属性强的反应事实的离子方程式_______________ 。

请回答下列问题:
(1)考古工作者利用元素②的一种核素测定一些文物的年代,这种核素的符号是
(2)画出元素⑧形成的简单离子的结构示意图
(3)写出元素④和⑥的单质在加热条件下反应,所得产物的电子式为
(4)⑥元素的最高价氧化物对应的水化物含有的化学键是
(5)②、③、④、⑤四种元素的简单气态氢化物中,稳定性最强的是
您最近一年使用:0次
8 . 已知元素周期表中共有18纵行,如图实线表示元素周期表的边界。按电子排布,可把周期表里的元素划分为几个区:s区、p区、d区、ds区等。除ds区外,其他区的名称来自按构造原理最后填入的电子的能级符号。
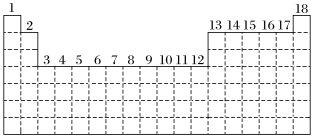
(1)请在图中用实线画出s区、p区、d区、ds区的边界线,并分别用阴影 和
和 表示d区和ds区。
表示d区和ds区。___________
(2)有的同学受这种划分的启发,认为d区内6、7纵行的部分元素可以排在另一区,你认为应排在___________ 区。
(3)随着科学技术的发展,不断有新的元素被发现。若把第七周期排满,则元素周期表共可以排布___________ 种元素。

(1)请在图中用实线画出s区、p区、d区、ds区的边界线,并分别用阴影
 和
和 表示d区和ds区。
表示d区和ds区。(2)有的同学受这种划分的启发,认为d区内6、7纵行的部分元素可以排在另一区,你认为应排在
(3)随着科学技术的发展,不断有新的元素被发现。若把第七周期排满,则元素周期表共可以排布
您最近一年使用:0次
2023高三·全国·专题练习
9 . 1869年,俄国化学家门捷列夫提出了元素周期律,并在此基础上发表了第一张元素周期表。为了纪念元素周期表诞生150年,联合国将2019年定为“国际化学元素周期表年”,并认为元素周期表是“科学共同的语言”。
(1)认识元素周期表的结构:
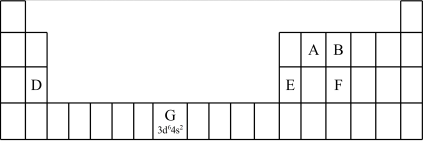
①在元素周期表中,第ⅠB、ⅡB元素属于___________ 区。
②2017年5月9日我国发布了113号Nh、115号Mc、117号Ts、118号Og四种元素,则下列说法正确的是___________ (填字母序号)。
a.113号元素在周期表中的位置是第七周期VB族
b.117号元素Ts位于金属与非金属分界线上,属于准金属,可能是半导体
c.这四种元素都是主族元素
d.最高价氧化物的水化物的碱性:Nh>Mc
(2)认识原子结构与元素周期表的关系:见表中元素G的信息,其中“3d64s2”称为该元素原子的___________ ,该元素M能层上具有___________ 种不同运动状态的电子。
(3)认识元素周期律及其应用:
①第三周期元素的第一电离能:D___________ E(填“>”“<”或“=”)。
②气态氢化物的沸点:B___________ F(填“>”“<”或“=”),理由是___________ 。
(1)认识元素周期表的结构:

①在元素周期表中,第ⅠB、ⅡB元素属于
②2017年5月9日我国发布了113号Nh、115号Mc、117号Ts、118号Og四种元素,则下列说法正确的是
a.113号元素在周期表中的位置是第七周期VB族
b.117号元素Ts位于金属与非金属分界线上,属于准金属,可能是半导体
c.这四种元素都是主族元素
d.最高价氧化物的水化物的碱性:Nh>Mc
(2)认识原子结构与元素周期表的关系:见表中元素G的信息,其中“3d64s2”称为该元素原子的
(3)认识元素周期律及其应用:
①第三周期元素的第一电离能:D
②气态氢化物的沸点:B
您最近一年使用:0次
名校
10 . 现代化学在材料、资源、能源、环境、医药、信息技术等领域均有重大应用。
I.新疆也要建造磁悬浮列车了。在磁悬浮列车制造过程中将使用大量含钇(Y)元素的超导材料。钇(Y)元素在元素周期表中的信息如图所示:
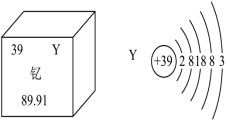
(1)钇原子核内有___________ 个质子,图中89.91表示的是___________ 。
(2)钇元素形成氧化物的化学式是___________ 。
II.电解质是维持人体生理活动的基础之一、请回答下列问题:
①CO2 ②Al ③乙醇 ④Fe(OH)3胶体 ⑤熔融BaSO4 ⑥KOH溶液 ⑦固态
(3)上述物质中属于电解质的是___________ 。(填序号)
(4)属于非电解质的是___________ 。(填序号)
(5)能导电的纯净物是___________ 。(填序号)
(6)写出⑦在水中的电离方程式___________ 。
(7)写出①和⑥的反应方程式___________ 。
(8)请写出实验室中制备Fe(OH)3胶体的化学反应方程式___________ 。
I.新疆也要建造磁悬浮列车了。在磁悬浮列车制造过程中将使用大量含钇(Y)元素的超导材料。钇(Y)元素在元素周期表中的信息如图所示:

(1)钇原子核内有
(2)钇元素形成氧化物的化学式是
II.电解质是维持人体生理活动的基础之一、请回答下列问题:
①CO2 ②Al ③乙醇 ④Fe(OH)3胶体 ⑤熔融BaSO4 ⑥KOH溶液 ⑦固态

(3)上述物质中属于电解质的是
(4)属于非电解质的是
(5)能导电的纯净物是
(6)写出⑦在水中的电离方程式
(7)写出①和⑥的反应方程式
(8)请写出实验室中制备Fe(OH)3胶体的化学反应方程式
您最近一年使用:0次



