名校
1 . 砷(As)是第四周期ⅤA族元素,可以形成As2S3、H3AsO3、H3AsO4等化合物,用途广泛。完成下列填空:
(1)砷原子核外有____ 个电子层,最外层有_____ 个电子。
(2)将砷与ⅤA族所有短周期元素的原子半径,按从小到大的顺序排列_____ (用元素符号表示)
(3)溴位于ⅦA族且与砷同周期,比较溴、砷最高价氧化物对应水化物酸性的强弱:_____ 强于____ (填物质的化学式)
(4)周期表中,铝和砷都在金属和非金属过渡线附近。若向AlCl3溶液中逐滴加入NaOH溶液,先生成沉淀,然后沉淀逐渐消失,请用电离平衡移动的原理解释沉淀会消失的原因______ 。
(1)砷原子核外有
(2)将砷与ⅤA族所有短周期元素的原子半径,按从小到大的顺序排列
(3)溴位于ⅦA族且与砷同周期,比较溴、砷最高价氧化物对应水化物酸性的强弱:
(4)周期表中,铝和砷都在金属和非金属过渡线附近。若向AlCl3溶液中逐滴加入NaOH溶液,先生成沉淀,然后沉淀逐渐消失,请用电离平衡移动的原理解释沉淀会消失的原因
您最近一年使用:0次
2 . 砷(As)是第四周期VA族元素,可以形成As2S3、H3AsO3、H3AsO4等化合物,用途广泛。
完成下列填空:
(1)砷原子核外有__ 个电子层,最外层有__ 个电子,写出砷原子最外层电子的轨道表示式:__ 。
(2)将砷与VA族所有短周期元素的原子半径,按从小到大的顺序排列:__ (用元素符号表示)。
(3)溴位于VIIA族且与砷同周期,比较溴、砷最高价氧化物对应水化物酸性的强弱:__ 强于__ (填物质的化学式)。
(4)周期表中,铝和砷都在金属和非金属过渡线附近,举一例说明铝元素具有非金属性:__ 。
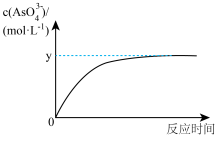
(5)已知:稀Na3AsO3溶液、稀碘水和稀NaOH溶液混合,发生如下反应:AsO33-(aq)+I2(aq)+2OH- AsO43-(aq)+2I-(aq)+H2O(l),溶液中c(AsO43-)与反应时间(t)的关系如图所示。
AsO43-(aq)+2I-(aq)+H2O(l),溶液中c(AsO43-)与反应时间(t)的关系如图所示。
①写出该反应平衡常数的表达式K=___ 。
②不能判断反应达到平衡状态的是___ (选填编号)。
A.溶液的pH不再变化
B.v(I-)=2v(AsO33-)
C.c(AsO33-)/c(I-)不再变化
D.c(I-)=2ymol·L-1
完成下列填空:
(1)砷原子核外有
(2)将砷与VA族所有短周期元素的原子半径,按从小到大的顺序排列:
(3)溴位于VIIA族且与砷同周期,比较溴、砷最高价氧化物对应水化物酸性的强弱:
(4)周期表中,铝和砷都在金属和非金属过渡线附近,举一例说明铝元素具有非金属性:
(5)已知:稀Na3AsO3溶液、稀碘水和稀NaOH溶液混合,发生如下反应:AsO33-(aq)+I2(aq)+2OH-
 AsO43-(aq)+2I-(aq)+H2O(l),溶液中c(AsO43-)与反应时间(t)的关系如图所示。
AsO43-(aq)+2I-(aq)+H2O(l),溶液中c(AsO43-)与反应时间(t)的关系如图所示。
①写出该反应平衡常数的表达式K=
②不能判断反应达到平衡状态的是
A.溶液的pH不再变化
B.v(I-)=2v(AsO33-)
C.c(AsO33-)/c(I-)不再变化
D.c(I-)=2ymol·L-1
您最近一年使用:0次
2019-11-08更新
|
164次组卷
|
3卷引用:上海市杨浦区2017-2018学年度高三第一学期高中等级考模拟调研化学试题
上海市杨浦区2017-2018学年度高三第一学期高中等级考模拟调研化学试题上海市民星中学2019—2020学年高三上学期期中考试化学试题(已下线)专题35 磷、砷及其化合物-2022年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)
3 . 下面是元素周期表的一部分,表中的每个字母表示一种短周期元素,请用对应的化学符号回答下列问题:

(1)D在元素周期表中的位置是____ 。
(2)E元素所形成的气态氢化物的电离方程式____ 。
(3)B、C两元素的单质较活泼的是___ 。(填元素符号)
(4)F是形成化合物最多的一种元素,它有多种单质请写出其中的两种:___ 、___ 。
(5)C是大自然赐予人类的宝物。将少量C单质置于足量氢氧化钠溶液中,可以观察到的现象为__ 。它其中的一个用途是和氧化铁反应制得难熔金属铁,该反应的化学方程式为__ C表现出的性质是___ (氧化性/还原性),反应时可观察到的实验现象有___ (填字母)。
A.产生红棕色烟雾 B.发出耀眼的光芒 C有熔融物生成
(6)C元素的最高价氧化物对应的水化物的化学式为___ ,该物质___ (填“能”或“不能”)溶于氨水,___ (填“能”或“不能”)溶于氢氧化钠溶液,若能写出发生反应的离子方程式___ 。
(7)G元素的非金属性比H元素的非金属性___ (选填“强”、“弱”),能说明这一事实的化学方程式是___ (任写一个)。

(1)D在元素周期表中的位置是
(2)E元素所形成的气态氢化物的电离方程式
(3)B、C两元素的单质较活泼的是
(4)F是形成化合物最多的一种元素,它有多种单质请写出其中的两种:
(5)C是大自然赐予人类的宝物。将少量C单质置于足量氢氧化钠溶液中,可以观察到的现象为
A.产生红棕色烟雾 B.发出耀眼的光芒 C有熔融物生成
(6)C元素的最高价氧化物对应的水化物的化学式为
(7)G元素的非金属性比H元素的非金属性
您最近一年使用:0次
4 . 下表为元素周期表的一部分,请回答有关问题:
(1)元素⑥的原子结构示意图___________ ;写出⑤的氧化物的一种用途__________ 。
(2)表中⑤和⑥气态氢化物的稳定性顺序为______ >______ (填氢化物的化学式);
(3)表中能形成两性氢氧化物的元素是_________ (填元素符号),该元素的单质与③的氢氧化物水溶液反应的离子反应方程式_______________ 。
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
| 第2周期 | ① | ② | ||||||
| 第3周期 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
(1)元素⑥的原子结构示意图
(2)表中⑤和⑥气态氢化物的稳定性顺序为
(3)表中能形成两性氢氧化物的元素是
您最近一年使用:0次
名校
5 . 门捷列夫在研究周期表时预言了包括“类铝”、“类硅”在内的11种元素。
(1)门捷列夫预言的“类硅”,多年后被德国化学家文克勒发现,命名为锗(Ge)。
①已知主族元素锗的最高化合价为+4价,其最高价氧化物的水化物为两性氢氧化物。试比较元素的非金属性Si___ Ge(用“>”或“<”表示)。
②若锗位于Si的下一周期,写出“锗”在周期表中的位置_____ 。根据锗在周期表中处于金属和非金属分界线附近,预测锗单质的一种用途是_______ .
③硅和锗单质分别与 反应时,反应较难进行的是
反应时,反应较难进行的是_______ (填“硅”或“锗”)。
(2)“类铝”在门捷列夫预言4年后,被布瓦博德朗在一种矿石中发现,命名为镓(Ga)。
①由镓的性质推知,镓与铝同主族,且位于铝的下一周期。试写出镓原子的结构示意图____ 。冶炼金属镓通常采用的方法是_____ .
②已知Ga(OH)3难溶于水,为判断Ga(OH)3是否为两性氢氧化物,设计实验时,需要选用的试剂有GaCl3溶液、________ 和________ .
(3)某同学阅读课外资料,看到了下列有关锗、锡、铅三种元素的性质描述:
①锗、锡在空气中不反应,铅在空气中表面形成一层氧化铅;
②锗与盐酸不反应,锡与盐酸反应,铅与盐酸反应但生成PbCl2微溶而使反应终止:
该同学查找三种元素在周期表的位置如图所示:
根据以上信息推测,下列描述正确的是______ (填标号)。
a.锗、锡、铅的+4价的氢氧化物的碱性强弱顺序是:Ge(OH)4<Sn(OH)4<Pb(OH)4
b.锗、锡、铅的金属性依次减弱;
c. 锗、锡、铅的原子半径依次增大。
(1)门捷列夫预言的“类硅”,多年后被德国化学家文克勒发现,命名为锗(Ge)。
①已知主族元素锗的最高化合价为+4价,其最高价氧化物的水化物为两性氢氧化物。试比较元素的非金属性Si
②若锗位于Si的下一周期,写出“锗”在周期表中的位置
③硅和锗单质分别与
 反应时,反应较难进行的是
反应时,反应较难进行的是(2)“类铝”在门捷列夫预言4年后,被布瓦博德朗在一种矿石中发现,命名为镓(Ga)。
①由镓的性质推知,镓与铝同主族,且位于铝的下一周期。试写出镓原子的结构示意图
②已知Ga(OH)3难溶于水,为判断Ga(OH)3是否为两性氢氧化物,设计实验时,需要选用的试剂有GaCl3溶液、
(3)某同学阅读课外资料,看到了下列有关锗、锡、铅三种元素的性质描述:
①锗、锡在空气中不反应,铅在空气中表面形成一层氧化铅;
②锗与盐酸不反应,锡与盐酸反应,铅与盐酸反应但生成PbCl2微溶而使反应终止:
该同学查找三种元素在周期表的位置如图所示:
IV | |
4 | Ge |
5 | Sn |
6 | Pb |
a.锗、锡、铅的+4价的氢氧化物的碱性强弱顺序是:Ge(OH)4<Sn(OH)4<Pb(OH)4
b.锗、锡、铅的金属性依次减弱;
c. 锗、锡、铅的原子半径依次增大。
您最近一年使用:0次
6 . 下表是元素周期表的一部分,针对表中的①~⑨种元素,填写下列空白:
(1)在这些元素中,化学性质最不活泼的是:_____ (填具体化学用语,下同)。
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是______ ,碱性最强的化合物的电子式是:_____ 。
(3)最高价氧化物是两性氧化物的元素是___ ;写出它的氧化物与氢氧化钠反应的离子方程式__ 。
(4)②氢化物与③的单质在一定条件下反应的化学方程式为:______ 。
(5)②可以形成多种氧化物,其中一种是红棕色气体,试用方程式说明该气体不宜采用排水法收集的原因________ 。
(6)用结构式表示元素①与③形成的化合物____ ,该化合物在固体时俗称___ ,属于____ 晶体,指出它的一种用途___ 。
主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ |
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是
(3)最高价氧化物是两性氧化物的元素是
(4)②氢化物与③的单质在一定条件下反应的化学方程式为:
(5)②可以形成多种氧化物,其中一种是红棕色气体,试用方程式说明该气体不宜采用排水法收集的原因
(6)用结构式表示元素①与③形成的化合物
您最近一年使用:0次
名校
7 . 下表为元素周期表的一部分, 表中列出10种元素在周期表中的位置,按要求回答下列各题。
(1)写出下列序号所代表的元素符号③_____ ;⑩______
(2)写出⑥的一种用途_________________ ;常温下可与表中_______ 单质反应(填化学式)
(3)元素④的原子结构示意图为________________________ ;
(4)⑤和⑨形成的化合物的化学式为:_____________ ;向该化合物的水溶液里逐滴滴入苛性钠溶液,现象为__________________________________________________ .
(5)②⑤⑦⑧的原子半径由大到小的顺序是__________________________ (用元素符号表示)
(6)将①⑤同时投入到水中,发生反应的化学方程式有:______________
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ⑧ | ⑩ | ||||||
| 3 | ① | ③ | ⑤ | ⑥ | ⑦ | ⑨ | ||
| 4 | ② | ④ |
(1)写出下列序号所代表的元素符号③
(2)写出⑥的一种用途
(3)元素④的原子结构示意图为
(4)⑤和⑨形成的化合物的化学式为:
(5)②⑤⑦⑧的原子半径由大到小的顺序是
(6)将①⑤同时投入到水中,发生反应的化学方程式有:
您最近一年使用:0次
2019-04-16更新
|
280次组卷
|
2卷引用:福建省永安第十二中学2018-2019学年高一下学期3月月考化学试题
名校
8 . 硒的原子序数为34,是硫的同主族元素,硒的单质及其化合物用途非常广泛。
(1)硒位于周期表第___ ,周期___ 族。Se2Cl2常用作分析试剂,其电子式为_____ 。
(2)硒化铟是一种可应用于未来超算设备的新型半导体材料。已知铟(In)与铝同族且比铝多两个电子层。下列说法正确的是_____ (填字母)。
A.原子半径:In>Se B.In的金属性比Se强
C.In的金属性比Al弱 D.硒化铟的化学式为InSe2
(3)工业上常从电冶铜的阳极泥中提取纳米硒。向浆化的阳极泥中通入氯气,Cu2Se被溶液中的HClO氧化为H2SeO3及CuCl2,反应中HClO与Cu2Se的物质的量之比为___ 。用氨水中和亚硒酸后得到亚硒酸铵,再向( NH4)2SeO3溶液中加入Na2S2O3可得到纳米硒,同时生成亚硫酸盐,(NH4)2SeO3与Na2S2O3反应生成纳米硒的离子方程式为______ 。
(1)硒位于周期表第
(2)硒化铟是一种可应用于未来超算设备的新型半导体材料。已知铟(In)与铝同族且比铝多两个电子层。下列说法正确的是
A.原子半径:In>Se B.In的金属性比Se强
C.In的金属性比Al弱 D.硒化铟的化学式为InSe2
(3)工业上常从电冶铜的阳极泥中提取纳米硒。向浆化的阳极泥中通入氯气,Cu2Se被溶液中的HClO氧化为H2SeO3及CuCl2,反应中HClO与Cu2Se的物质的量之比为
您最近一年使用:0次
2017-10-30更新
|
892次组卷
|
2卷引用:江西省百所名校2018届高三第一次联合考试化学试题
9 . 元素周期表和元素周期律是学习化学的重要工具,可以帮助我们推测元素及其化合物的结构和性质,对工农业生产具有一定的指导意义。下表是元素周期表的部分片段(2、3周期)
(1)9种元素中,原子半径最小的是______ ,化学性质最不活泼的是____ 。
(2)⑥、⑧的最高价氧化物对应的水化物的酸性较强的是_______ 。
(3)④元素形成的多种同素异形体,有广泛的用途。请写出其中任意两种同素异形体的名称:______ 和______ 。
(4)写出③的最高价氧化物对应的水化物分别与①、⑤的最高价氧化物对应的水化物反应的化学方程式_______________ 。
(5)某同学做同周期元素金属性递变规律实验时,设什了如下实验并记录了有关实验现象。
请你根据上表得出实验结论:_________ ;若比较⑥与⑧的单质的活泼性,请写出实验方案___________________ 。
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 2 | ④ | ⑤ | ⑦ | |||||
| 3 | ① | ② | ③ | ⑥ | ⑧ | ⑨ |
(1)9种元素中,原子半径最小的是
(2)⑥、⑧的最高价氧化物对应的水化物的酸性较强的是
(3)④元素形成的多种同素异形体,有广泛的用途。请写出其中任意两种同素异形体的名称:
(4)写出③的最高价氧化物对应的水化物分别与①、⑤的最高价氧化物对应的水化物反应的化学方程式
(5)某同学做同周期元素金属性递变规律实验时,设什了如下实验并记录了有关实验现象。
| 实验步骤 | 实验现象 |
| A、将一小块单质①放入滴有酚酞溶液的冷水中 | 剧烈反应,①浮于水面上,熔成小球,四处游动,发出“嘶嘶”声.随之消失,溶液变成红色 |
| B、将单质②投入冷水中,观察现象,再将水加热 | 开始无现象,加热后有气体产生 |
| C.将单质②投入稀盐酸中 | 迅速产生大量无色气体 |
| D.将单质③投入稀盐酸中 | 反应不十分剧烈,产生无色气体 |
请你根据上表得出实验结论:
您最近一年使用:0次
10 . 铁、铜、铬、镍及其化合物在现代社会中的用途越来越广泛。
(1)铁在元素周期表中的位置是_____________ ,基态铁原子价电子排布式为___________ 。
(2)锂—磷酸氧铜电池正极的的活性物质是Cu4O(PO4)2,PO43-的空间构型是______________ ,P、S元素第一电离能大小关系为_______________ 。
(3)镍可与CO形成配合物Ni(CO)n,CO分子与N2互为等电子体,则中CO分子σ键与π键的个数比为________ ;该配合物的熔点是170℃,则Ni(CO)n 属于 _______ 晶体。
(4)在铬的催化作用下,乙醇可被空气氧化为乙醛(CH3CHO),乙醛分子中碳原子的杂化方式是______ ,乙醇极易溶于水,其主要原因是_______________ 。
(5)立方NiO晶体结构类似于NaCl,则Ni2+的配位数为________ ,其晶胞边长为a cm,列式表示NiO晶体的密度为____ g/cm3(不必计算出结果,阿伏伽德罗常数的值为NA)。
(1)铁在元素周期表中的位置是
(2)锂—磷酸氧铜电池正极的的活性物质是Cu4O(PO4)2,PO43-的空间构型是
(3)镍可与CO形成配合物Ni(CO)n,CO分子与N2互为等电子体,则中CO分子σ键与π键的个数比为
(4)在铬的催化作用下,乙醇可被空气氧化为乙醛(CH3CHO),乙醛分子中碳原子的杂化方式是
(5)立方NiO晶体结构类似于NaCl,则Ni2+的配位数为
您最近一年使用:0次
2017-07-01更新
|
482次组卷
|
2卷引用:四川省广安市2016-2017学年高二下学期期末考试化学试题



