名校
1 . 根据元素周期表中1~18号元素的性质和递变规律,回答下列问题。
(1)原子序数为17的元素符号是___________ ;
(2)二氧化碳中所含两种元素的原子半径大小:C___________ O(填“>”或“<”);
(3)硫和氯均为第三周期元素,则两种元素的气态氢化物的稳定性强弱:
___________ HCl(填“>”或“<”);
(4)氮元素的简单气态氢化物与其最高价氧化物对应的水化物相互反应的离子方程式为___________ 。
(1)原子序数为17的元素符号是
(2)二氧化碳中所含两种元素的原子半径大小:C
(3)硫和氯均为第三周期元素,则两种元素的气态氢化物的稳定性强弱:

(4)氮元素的简单气态氢化物与其最高价氧化物对应的水化物相互反应的离子方程式为
您最近一年使用:0次
名校
2 . 下表显示了元素周期表中的一部分。
请回答下列问题。
(1)硫元素的原子序数是_______ 。
(2)氟元素的原子结构示意图为_______ (填写字母)。
A.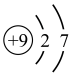 B.
B.
(3)镁元素在元素周期表的第_______ (填“二”或“三”)周期第_______ (填“ⅡA”或“ⅢA”)族。
(4)已知同主族元素从上到下原子半径逐渐增大,原子半径大小:H_______ (填“<”或“>”)Na。
(5)雷雨天闪电时空气中有O3生成,O2转化为O3是_______ (填“物理变化”或“化学变化”)。
(6)SiO2可用于生产光导纤维,SiO2中硅元素的化合价为_______ 。
(7)海水中的重要元素——钠和氯,形成生活中常见调味品的化学式为_______ 。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 第一周期 | 1 H 氢 | 2 He 氦 | ||||||
| 第二周期 | 3 Li 锂 | 4 Be 镀 | 5 B 硼 | 6 C 碳 | 7 N 氮 | 8 O 氧 | 9 F 氟 | 10 Ne 氖 |
| 第三周期1 | 1 Na 钠 | 12 Mg 镁 | 33 Al 铝 | 14 Si 硅 | 15 P 磷 | 16 S 硫 | 17 C 氯 | 18 Ar 氩 |
(1)硫元素的原子序数是
(2)氟元素的原子结构示意图为
A.
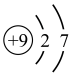 B.
B.
(3)镁元素在元素周期表的第
(4)已知同主族元素从上到下原子半径逐渐增大,原子半径大小:H
(5)雷雨天闪电时空气中有O3生成,O2转化为O3是
(6)SiO2可用于生产光导纤维,SiO2中硅元素的化合价为
(7)海水中的重要元素——钠和氯,形成生活中常见调味品的化学式为
您最近一年使用:0次
2023-05-11更新
|
205次组卷
|
2卷引用:2023年黑龙江省春季普通高中学业合格考试化学试题
解题方法
3 . 亚硫酰氯( )在医药、农药合成领域有广泛的应用。
)在医药、农药合成领域有广泛的应用。
(1) 含有S、O、Cl三种元素,其中位于元素周期表中第二周期的元素是
含有S、O、Cl三种元素,其中位于元素周期表中第二周期的元素是_______ 。
(2)Cl的非金属性强于S的非金属性。
①用原子结构解释:Cl和S位于元素周期表中同一周期,原子核外电子层数相同,核电荷数Cl大于S,原子半径_______ ,得电子能力Cl强于S。
②用实验事实验证:将 通入
通入 溶液中,生成淡黄色沉淀。淡黄色沉淀是
溶液中,生成淡黄色沉淀。淡黄色沉淀是_______ 。
(3)下列关于 的说法正确的是
的说法正确的是_______ (填字母)。
a.属于化合物 b.摩尔质量为119 g·mol
 )在医药、农药合成领域有广泛的应用。
)在医药、农药合成领域有广泛的应用。(1)
 含有S、O、Cl三种元素,其中位于元素周期表中第二周期的元素是
含有S、O、Cl三种元素,其中位于元素周期表中第二周期的元素是(2)Cl的非金属性强于S的非金属性。
①用原子结构解释:Cl和S位于元素周期表中同一周期,原子核外电子层数相同,核电荷数Cl大于S,原子半径
②用实验事实验证:将
 通入
通入 溶液中,生成淡黄色沉淀。淡黄色沉淀是
溶液中,生成淡黄色沉淀。淡黄色沉淀是(3)下列关于
 的说法正确的是
的说法正确的是a.属于化合物 b.摩尔质量为119 g·mol

您最近一年使用:0次
4 . 分子筛是一类具有规整孔道结构的多孔材料,能够选择性吸附空间结构各异和不同尺寸的分子,在化学工业中有着广泛的应用。近年来,我国科学家在分子筛研究领域不断取得新的突破。这些研究中涉及的部分元素在周期表中位置如下:
(1)近期我国科学家制备了一种无缺陷的分子筛膜,可高效分离CH4与CO2两种气体。下列有关分子空间结构的描述正确的是_______
(2)传统的分子筛主要含有O、Na、Al和Si元素,通过调控这 4种元素的比例,可获得不同性能的分子筛产品。这4种元素描述中正确的是_______ 。
(3)通过将分子筛中的元素Na替换为K或Ca,可改变分子筛的孔径大小。这3种元素中说法正确的是_______
(4)N2常用于分子筛的孔结构测试,H、O和N元素可形成多种物质。下列说法正确的是_______
(5)某些分子筛可以选择性吸附Ar。Ar位于元素周期表的_______
| 周期 | 族 | ||||||
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 1 | H | ||||||
| 2 | C | N | O | ||||
| 3 | Na | Al | Si | ||||
| 4 | K | Ca | |||||
| A.CH4是平面结构 | B.CO2是V形结构 |
| C.CH4是正四面体结构 | D.CO2是直线形结构 |
| A.非金属性最强的是O |
| B.核外电子数最少的是 Na |
| C.金属性最强的是Al |
| D.原子半径最大的是Si |
| A.仅Na可与Cl2反应 |
| B.K的单质与水的反应最剧烈 |
| C.Na的氧化物与水的反应均为化合反应 |
| D.Ca的最高价氧化物的水化物碱性最强 |
| A.N2中含有共价三键 |
| B.NO可由NH3催化氧化得到 |
| C.NH3的水溶液呈碱性 |
| D.稀HNO3与Cu反应产生H2 |
| A.第二周期 | B.Ⅷ族 | C.第三周期 | D.0族 |
您最近一年使用:0次
5 . 填写下列空白:
(1)写出表示含有8个质子、10个中子的原子的化学符号:_______ 。
(2)原子符号为 X的元素属于第
X的元素属于第_______ 周期_______ 族。
(3)周期表中位于第8纵列的铁元素属于第_______ 族。
(4)周期表中第三周期最活泼的金属元素是_______ 。
(5)已知某微粒的结构示意图为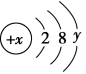 ,试回答下列问题:
,试回答下列问题:
①当x-y=10时,该微粒为_______ (填“原子”“阳离子”或“阴离子”)。
②当y=6时,元素最高价氧化物对应水化物的化学式为_______ 。
(1)写出表示含有8个质子、10个中子的原子的化学符号:
(2)原子符号为
 X的元素属于第
X的元素属于第(3)周期表中位于第8纵列的铁元素属于第
(4)周期表中第三周期最活泼的金属元素是
(5)已知某微粒的结构示意图为
 ,试回答下列问题:
,试回答下列问题:①当x-y=10时,该微粒为
②当y=6时,元素最高价氧化物对应水化物的化学式为
您最近一年使用:0次
2023-02-02更新
|
481次组卷
|
3卷引用:2023年广东省普通高中学业水平合格性考试化学科模拟测试卷(一)
名校
解题方法
6 . 一氯化碘(ICl)是一种卤素互化物,与卤素单质性质相似,可用于制农药等。
(1)Cl在元素周期表中位于第三周期、第_______ 族。
(2)Cl的最高价氧化物对应的水化物为HClO4,其中Cl元素的化合价为_______ 价。
(3)Cl的非金属性强于I的,用原子结构解释原因:Cl和I位于同一主族,最外层电子数相同,_______ ,得电子能力Cl强于I。
(4)下列推断中,正确的是_______ (填字母)。
a.ICl有氧化性
b.热稳定性:HI>HCl
c.I的最高价氧化物对应的水化物为HIO4
(1)Cl在元素周期表中位于第三周期、第
(2)Cl的最高价氧化物对应的水化物为HClO4,其中Cl元素的化合价为
(3)Cl的非金属性强于I的,用原子结构解释原因:Cl和I位于同一主族,最外层电子数相同,
(4)下列推断中,正确的是
a.ICl有氧化性
b.热稳定性:HI>HCl
c.I的最高价氧化物对应的水化物为HIO4
您最近一年使用:0次
2023-01-17更新
|
286次组卷
|
2卷引用:北京市2022-2023学年高二上学期第二次合格考化学试题
7 . 下表列出了①~④四种元素在周期表中的位置.
回答下列问题:
(1)①的元素符号为_____________ 。
(2)②的基态原子电子排布式为__________________________ 。
(3)③和④中原子半径较大的是_____________ (填元素符号)。
(4)如图是③原子中s电子和p电子的电子云轮廓图。s电子的电子云形状为_____________ 形;每个p能级都有_____________ 个相互垂直的电子云。

| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ① | |||||||
| 3 | ② | ③ | ||||||
| 4 | ④ |
回答下列问题:
(1)①的元素符号为
(2)②的基态原子电子排布式为
(3)③和④中原子半径较大的是
(4)如图是③原子中s电子和p电子的电子云轮廓图。s电子的电子云形状为

您最近一年使用:0次
8 . 根据元素周期表中1~20号元素的性质和递变规律,回答下列问题:
(1)原子序数为8的元素符号是_______ ;
(2)硫化氢的化学式是_______ ;
(3)氟(F)和氯(Cl)均为第ⅦA族元素,则两种元素的非金属性强弱是:F_______ Cl(填“>”或“<”);
(4)钾和硫两种元素的最高价氧化物对应的水化物相互反应的离子方程式为_______ 。
(1)原子序数为8的元素符号是
(2)硫化氢的化学式是
(3)氟(F)和氯(Cl)均为第ⅦA族元素,则两种元素的非金属性强弱是:F
(4)钾和硫两种元素的最高价氧化物对应的水化物相互反应的离子方程式为
您最近一年使用:0次
2022-12-16更新
|
393次组卷
|
2卷引用:湖南省部分普通高中2022-2023学年高一上学期学业水平合格性考试化学试题
解题方法
9 . 下表列出了 九种元素在周期表中的位置,根据要求回答下列问题:
九种元素在周期表中的位置,根据要求回答下列问题:

(1)f的名称是_______ ,d的元素符号是_______ ;
(2)a在周期表中的位置是_______ ;
(3)h的原子结构示意图是_______ ;
(4)e、g、i按原子半径由大到小的顺序排列为_______ (填元素符号);
(5)c与h相比非金属性较强的是_______ (填元素符号),h的氢化物与i的氢化物相比,稳定性较弱的是_______ (填化学式);
(6)e的最高价氧化物对应的水化物与g的最高价氧化物对应的水化物,在水溶液中反应的离子方程式为_______ ;
(7)g的单质与氧化铁在高温条件下反应的化学方程式为_______ ;
(8)i的氢化物的电子式为_______ 。
 九种元素在周期表中的位置,根据要求回答下列问题:
九种元素在周期表中的位置,根据要求回答下列问题:
(1)f的名称是
(2)a在周期表中的位置是
(3)h的原子结构示意图是
(4)e、g、i按原子半径由大到小的顺序排列为
(5)c与h相比非金属性较强的是
(6)e的最高价氧化物对应的水化物与g的最高价氧化物对应的水化物,在水溶液中反应的离子方程式为
(7)g的单质与氧化铁在高温条件下反应的化学方程式为
(8)i的氢化物的电子式为
您最近一年使用:0次
解题方法
10 . NaOH被大量用于制皂、造纸和纺织品生产。回答下列问题。
(1)H元素位于元素周期表的第____ 周期第IA族。
(2)Na元素位于第IA族H元素下方,Na的原子半径比H的____ (填“大”或“小”)。
(3)NaOH所含的两种非金属元素中,非金属性较强的是___ (填“H”或“O”)。
(4)Na的最高价氧化物的化学式为____ 。
(1)H元素位于元素周期表的第
(2)Na元素位于第IA族H元素下方,Na的原子半径比H的
(3)NaOH所含的两种非金属元素中,非金属性较强的是
(4)Na的最高价氧化物的化学式为
您最近一年使用:0次



