解题方法
1 . 元素周期表的一部分如图,每一序号代表一种元素。回答下列问题:___________ 。
(2)非金属性:④___________ ⑤(填“ ”“
”“ ”或“
”或“ ”,下同);金属性:⑥
”,下同);金属性:⑥___________ ⑩。④⑤⑦的简单离子半径从小到大的排列顺序是___________ (写离子符号)。
(3)用电子式表示由元素①和⑨组成的化合物的形成过程:___________ 。
(4)原子的电子层数比⑩多1且与⑩同主族的元素为___________ (填元素符号),原子序数为___________ 。
(5)⑥的最高价氧化物对应水化物的溶液与⑦形成的单质反应的离子方程式为___________ 。

(2)非金属性:④
 ”“
”“ ”或“
”或“ ”,下同);金属性:⑥
”,下同);金属性:⑥(3)用电子式表示由元素①和⑨组成的化合物的形成过程:
(4)原子的电子层数比⑩多1且与⑩同主族的元素为
(5)⑥的最高价氧化物对应水化物的溶液与⑦形成的单质反应的离子方程式为
您最近一年使用:0次
解题方法
2 . 下表是元素周期表的一部分,请参照元素①~⑥的位置回答下列问题:
(1)元素①的一种核素中,含有1个质子和1个中子,该核素组成的符号是 _______ 。
(2)⑤的原子结构示意图是_______ 。
(3)上述元素中,原子半径最大的是_______ (写元素符号)。
(4)金属性:③_______ ④(填“>”或“<”)。
(5)34号元素硒(Se)和⑤位于同一主族,是生命必需元素,硒酸(H2SeO4)的酸性比(H2SO4)_______ (填“强”或“弱”)。
| 族 周期 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | |||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ||||
(2)⑤的原子结构示意图是
(3)上述元素中,原子半径最大的是
(4)金属性:③
(5)34号元素硒(Se)和⑤位于同一主族,是生命必需元素,硒酸(H2SeO4)的酸性比(H2SO4)
您最近一年使用:0次
3 . )如表是周期表中的一部分,根据A~I在周期表中的位置,用元素符号或化学式回答下列问题:
(1)表中元素,化学性质最不活泼的是_______ ,只有负价而无正价的元素是_______ 。
(2)最高价氧化物的水化物酸性最强的是_______ ,呈两性的是_______ 。
(3)A分别与E、G、H形成的化合物中,最稳定的是_______ 。
(4)在B、C、E、F中,原子半径最大的是_______ 。
(5)写出C的最高价氧化物与H的氢化物之间反应的离子方程式:_______ 。
(6)写出B与C两种元素的最高价氧化物对应的水化物相互反应的化学方程式:_______ 。
| 族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 1 | A | ||||||||
| 2 | D | E | G | ||||||
| 3 | B | C | J | F | H | I |
(2)最高价氧化物的水化物酸性最强的是
(3)A分别与E、G、H形成的化合物中,最稳定的是
(4)在B、C、E、F中,原子半径最大的是
(5)写出C的最高价氧化物与H的氢化物之间反应的离子方程式:
(6)写出B与C两种元素的最高价氧化物对应的水化物相互反应的化学方程式:
您最近一年使用:0次
4 . 回答下列问题。
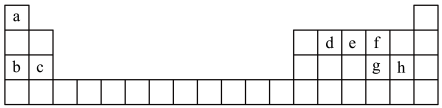
(1)现有a~h8种短周期元素,它们在元素周期表中的位置如图所示。_______ 。
②表中元素原子半径最大的是(元素符号)_______ 。
③g、h的最高价氧化物对应的水化物酸性强的是(化学式)_______ 。
④写出上述元素组成的一种四原子、10电子的共价化合物的电子式_______ 。
⑤下列事实能说明f元素的非金属性比g元素的非金属性强的是_______ (填序号)。
i.f单质与g的氢化物反应,能置换出g的单质
ii.在氧化还原反应中,1molf单质比1molg得电子多
iii.f和g两元素的简单氢化物受热分解,前者的分解温度高
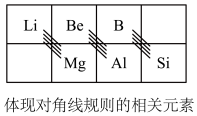
(2)在元素周期表中,某些主族元素与右下方的主族元素(如图)的有些性质是相似的(如锂和镁在过量的氧气中燃烧均生成氧化物,而不是过氧化物),这种相似性被称为对角线规则。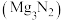 。锂在空气中燃烧,除生成氧化锂外,也会生成微量的
。锂在空气中燃烧,除生成氧化锂外,也会生成微量的_______ (填化学式)。
②铍最高价氧化物对应的水化物为 ,属于两性氢氧化物,可溶于氢氧化钠溶液,生成
,属于两性氢氧化物,可溶于氢氧化钠溶液,生成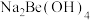 。写出离子反应方程式
。写出离子反应方程式_______ 。
(1)现有a~h8种短周期元素,它们在元素周期表中的位置如图所示。
②表中元素原子半径最大的是(元素符号)
③g、h的最高价氧化物对应的水化物酸性强的是(化学式)
④写出上述元素组成的一种四原子、10电子的共价化合物的电子式
⑤下列事实能说明f元素的非金属性比g元素的非金属性强的是
i.f单质与g的氢化物反应,能置换出g的单质
ii.在氧化还原反应中,1molf单质比1molg得电子多
iii.f和g两元素的简单氢化物受热分解,前者的分解温度高
(2)在元素周期表中,某些主族元素与右下方的主族元素(如图)的有些性质是相似的(如锂和镁在过量的氧气中燃烧均生成氧化物,而不是过氧化物),这种相似性被称为对角线规则。
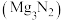 。锂在空气中燃烧,除生成氧化锂外,也会生成微量的
。锂在空气中燃烧,除生成氧化锂外,也会生成微量的②铍最高价氧化物对应的水化物为
 ,属于两性氢氧化物,可溶于氢氧化钠溶液,生成
,属于两性氢氧化物,可溶于氢氧化钠溶液,生成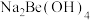 。写出离子反应方程式
。写出离子反应方程式
您最近一年使用:0次
解题方法
5 . 阅读下列科普短文并结合短文内容填空。
材料一:燃料电池是一种用途广泛的化学电源,不仅能量转化率高而且对环境友好。燃料电池在工作时,从负极连续通入 、①
、① 、②
、②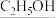 等燃料,从正极连续通入③
等燃料,从正极连续通入③ ,二者在电池内部(含有KOH溶液或④稀硫酸)发生反应生成
,二者在电池内部(含有KOH溶液或④稀硫酸)发生反应生成 、⑤
、⑤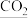 或
或 溶液等,同时产生电能。目前已研制成功Al—空气燃料电池,它可以代替汽油为汽车提供动力,也可用作照明电源。
溶液等,同时产生电能。目前已研制成功Al—空气燃料电池,它可以代替汽油为汽车提供动力,也可用作照明电源。
材料二:目前,我国的电动汽车约有80%应用的电池为磷酸铁锂电池,为了避免环境污染,必须回收废弃电池。通常采用湿法冶金工艺:首先用⑥NaOH溶液浸泡拆解下来的材料,其中⑦Al与⑧ 溶解得到⑨
溶解得到⑨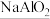 溶液,过滤得到含⑩石墨、
溶液,过滤得到含⑩石墨、 的滤渣,再用稀硝酸浸取滤渣,反应生成NO气体,得到含
的滤渣,再用稀硝酸浸取滤渣,反应生成NO气体,得到含 、
、 和磷酸的浸出液,经过调节pH、过滤、浓缩结晶等操作,可回收
和磷酸的浸出液,经过调节pH、过滤、浓缩结晶等操作,可回收 晶体。
晶体。
(1)燃料电池的氧化剂为 ,
, 和
和 互为
互为___________ (填“同位素”或“同素异形体”);氧元素在元素周期表中的位置为___________ 。
(2)①~⑤(仅指划线部分,下同)中,属于非电解质的是___________ (填序号 ,下同),⑥~⑩中能导电的是___________ 。
(3)⑥与⑧反应的离子方程式为___________ ;其中NaOH的电子式为___________ 。
(4)文中使用稀硫酸的浓度为 ,配制该稀硫酸250mL,需量取98%的浓硫酸(密度为
,配制该稀硫酸250mL,需量取98%的浓硫酸(密度为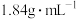 )的体积为
)的体积为___________ mL,配制过程中用到的仪器有:量筒、烧杯、玻璃棒、胶头滴管、___________ 若定容时俯视读数,会导致所配制稀硫酸浓度___________ 。(填“偏高”“偏低”或“无影响”)
(5)材料一:Al—空气燃料电池的反应原理是负极材料Al在电解质溶液中与空气中的 反应生成
反应生成 。该反应中氧化剂和还原剂的物质的量之比为
。该反应中氧化剂和还原剂的物质的量之比为___________ 。
(6)材料二:滤渣 中铁的化合价为
中铁的化合价为___________ ,酸浸时若有标准状况下4.48LNO产生,参加反应的 的物质的量为
的物质的量为___________ mol。
材料一:燃料电池是一种用途广泛的化学电源,不仅能量转化率高而且对环境友好。燃料电池在工作时,从负极连续通入
 、①
、① 、②
、②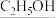 等燃料,从正极连续通入③
等燃料,从正极连续通入③ ,二者在电池内部(含有KOH溶液或④稀硫酸)发生反应生成
,二者在电池内部(含有KOH溶液或④稀硫酸)发生反应生成 、⑤
、⑤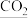 或
或 溶液等,同时产生电能。目前已研制成功Al—空气燃料电池,它可以代替汽油为汽车提供动力,也可用作照明电源。
溶液等,同时产生电能。目前已研制成功Al—空气燃料电池,它可以代替汽油为汽车提供动力,也可用作照明电源。材料二:目前,我国的电动汽车约有80%应用的电池为磷酸铁锂电池,为了避免环境污染,必须回收废弃电池。通常采用湿法冶金工艺:首先用⑥NaOH溶液浸泡拆解下来的材料,其中⑦Al与⑧
 溶解得到⑨
溶解得到⑨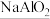 溶液,过滤得到含⑩石墨、
溶液,过滤得到含⑩石墨、 的滤渣,再用稀硝酸浸取滤渣,反应生成NO气体,得到含
的滤渣,再用稀硝酸浸取滤渣,反应生成NO气体,得到含 、
、 和磷酸的浸出液,经过调节pH、过滤、浓缩结晶等操作,可回收
和磷酸的浸出液,经过调节pH、过滤、浓缩结晶等操作,可回收 晶体。
晶体。(1)燃料电池的氧化剂为
 ,
, 和
和 互为
互为(2)①~⑤(仅指划线部分,下同)中,属于非电解质的是
(3)⑥与⑧反应的离子方程式为
(4)文中使用稀硫酸的浓度为
 ,配制该稀硫酸250mL,需量取98%的浓硫酸(密度为
,配制该稀硫酸250mL,需量取98%的浓硫酸(密度为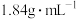 )的体积为
)的体积为(5)材料一:Al—空气燃料电池的反应原理是负极材料Al在电解质溶液中与空气中的
 反应生成
反应生成 。该反应中氧化剂和还原剂的物质的量之比为
。该反应中氧化剂和还原剂的物质的量之比为(6)材料二:滤渣
 中铁的化合价为
中铁的化合价为 的物质的量为
的物质的量为
您最近一年使用:0次
解题方法
6 . 元素周期表与元素周期律在学习、研究和生产实践中有很重要的作用。下表列出了5种元素在周期表中的位置,其中①~④代表4种元素。
(1)③的元素符号是___________ 。
(2)下列能说明①比②失电子能力强的事实是___________ (填字母)。
a.单质①的密度比单质②的密度小
b.单质①比单质②更容易与水反应置换出氢气
c.最高价氧化物对应的水化物的碱性:①强于②
(3)依据元素周期律推测:
Ⅰ. 属于
属于___________ (填“金属”或“非金属”)元素。
Ⅱ. 的最高价氧化物对应的水化物的化学式是
的最高价氧化物对应的水化物的化学式是___________ 。
Ⅲ.气态氢化物的热稳定性:
___________ (填“强于”或“弱于”) 。
。
(4)某元素的原子结构示意图为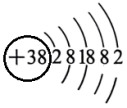 。下列关于该元素的说法正确的是
。下列关于该元素的说法正确的是___________ (填字母)。
a.位于周期表中第五周期第ⅡA族 b.属于非金属元素
c.单质能与水反应 d.其碳酸盐难溶于水
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅦA | 0 | ||
| 3 | ① | ② | ③ | |||||
| 4 | ④ |
(1)③的元素符号是
(2)下列能说明①比②失电子能力强的事实是
a.单质①的密度比单质②的密度小
b.单质①比单质②更容易与水反应置换出氢气
c.最高价氧化物对应的水化物的碱性:①强于②
(3)依据元素周期律推测:
Ⅰ.
 属于
属于Ⅱ.
 的最高价氧化物对应的水化物的化学式是
的最高价氧化物对应的水化物的化学式是Ⅲ.气态氢化物的热稳定性:

 。
。(4)某元素的原子结构示意图为
 。下列关于该元素的说法正确的是
。下列关于该元素的说法正确的是a.位于周期表中第五周期第ⅡA族 b.属于非金属元素
c.单质能与水反应 d.其碳酸盐难溶于水
您最近一年使用:0次
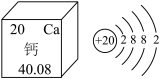
7 . 家中的食品、调味品、洗涤剂和药品等都含有化学物质,以下是胃药和加碘食盐的标签,回答下列问题。
(1)标签中涉及到的元素Al在周期表中的位置是_______ 。
(2)标签中涉及到的元素位于第三周期的有_______ 种,原子半径由大到小的排序是_______ 。
(3)氢氧化铝治疗胃酸过多时,发生反应的化学方程式是_______ 。
(4)食用盐的主要成分为氯化钠,氯化钠含有的化学键是_______ ;碘酸钾在水溶液中的电离方程式是_______ ;碘酸钾和碘化钾在酸性溶液中能发生反应生成使淀粉变蓝的物质,写出该反应的离子方程式并用单线桥法标出电子转移的方向和数目_______ 。
| 铝镁咀嚼片 【药品名】铝镁咀嚼片 【成分】氢氧化镁、氢氧化铝、二甲基硅油 【适应症】胃酸过多引起的胃痛、烧心等胃胀气的治疗 |
| 食用盐 【配料表】精制盐、碘酸钾 【碘含量(以计)】21mgkg-39mgkg 【保质期】36个月 |
(2)标签中涉及到的元素位于第三周期的有
(3)氢氧化铝治疗胃酸过多时,发生反应的化学方程式是
(4)食用盐的主要成分为氯化钠,氯化钠含有的化学键是
您最近一年使用:0次
名校
8 . 金属材料与人类生活息息相关,请回答下列问题。_______ 。
(2)家用台灯通常采用铜质插头,是利用金属铜的_______ 性。
(3)我国是最早采用湿法炼铜的国家,铁与硫酸铜溶液反应的化学方程式是_______ 。
(4)将一定质量的Zn片加入 的混合溶液中,充分反应后过滤,得到滤渣和滤液,则滤渣中一定含有的金属是
的混合溶液中,充分反应后过滤,得到滤渣和滤液,则滤渣中一定含有的金属是_______ ;若滤液显蓝色,则滤液中溶质一定有_______ 。
(2)家用台灯通常采用铜质插头,是利用金属铜的
(3)我国是最早采用湿法炼铜的国家,铁与硫酸铜溶液反应的化学方程式是
(4)将一定质量的Zn片加入
 的混合溶液中,充分反应后过滤,得到滤渣和滤液,则滤渣中一定含有的金属是
的混合溶液中,充分反应后过滤,得到滤渣和滤液,则滤渣中一定含有的金属是
您最近一年使用:0次
解题方法
9 . 下图为元素周期表的一部分。
回答下列问题:
(1)画出C的原子结构示意图________ 。
(2)指出O在元素周期表中的位置是________ 。
(3)工业上制备Na的方法为________ 。
(4)非金属性Cl强于S,用原子结构解释原因:________ ,得电子能力Cl大于S。
(5)硒(Se)与S在同一主族,位于S的正下方,下列推断正确的是________ (填序号)。
①硒元素的最高正化合价为+6价
②热稳定性:H2Se>H2O
③最高价氧化物对应的水化物的酸性:HClO4>H2SeO4
C | O | ||||||
Na | Al | Si | S | Cl |
(1)画出C的原子结构示意图
(2)指出O在元素周期表中的位置是
(3)工业上制备Na的方法为
(4)非金属性Cl强于S,用原子结构解释原因:
(5)硒(Se)与S在同一主族,位于S的正下方,下列推断正确的是
①硒元素的最高正化合价为+6价
②热稳定性:H2Se>H2O
③最高价氧化物对应的水化物的酸性:HClO4>H2SeO4
您最近一年使用:0次
解题方法
10 . 元素周期表在学习、研究和生产实践中有很重要的作用。下表列出了A〜E5种元素在周期表中位置:
(1)A元素的原子结构示意图________ 。
(2)B和C分别形成的最高价氧化物对应的水化物可以发生反应,离子方程式是_______ 。
(3)B、C、D三种元素原子半径最小的是_______ (填元素符号)。
(4)用电子式表示D的氢化物的形成过程:_______ 。
(5)在常温下,A的氢化物与E发生反应的离子方程式是_______ 。
(6)下列事实能判断B和E的金属性强弱的是______ (填字母)。
a.最高价氧化物对应的水化物的碱性强弱
b.常温下单质与水反应置换出氢的难易程度
c.相同温度下,其氢氧化物的溶解度大小
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
2 | A | |||||||
3 | B | C | D | |||||
4 | E |
(1)A元素的原子结构示意图
(2)B和C分别形成的最高价氧化物对应的水化物可以发生反应,离子方程式是
(3)B、C、D三种元素原子半径最小的是
(4)用电子式表示D的氢化物的形成过程:
(5)在常温下,A的氢化物与E发生反应的离子方程式是
(6)下列事实能判断B和E的金属性强弱的是
a.最高价氧化物对应的水化物的碱性强弱
b.常温下单质与水反应置换出氢的难易程度
c.相同温度下,其氢氧化物的溶解度大小
您最近一年使用:0次



