名校
1 . 下列物质含有非极性键的是
| A.HCl | B.H2 | C.NH3 | D.KCl |
您最近一年使用:0次
2024-06-12更新
|
171次组卷
|
2卷引用:2023年7月浙江省普通高中学业水平考试(学考)化学试题
解题方法
2 . 下列物质所形成的晶体中只含有离子键的是
A. | B. | C. | D. |
您最近一年使用:0次
名校
3 . 硅材料在生活中占有重要地位。 (结构如图所示)受热分解可生成
(结构如图所示)受热分解可生成 和
和 。
。 是一种优良的耐高温结构陶瓷。下列有关说法
是一种优良的耐高温结构陶瓷。下列有关说法不正确 的是
 (结构如图所示)受热分解可生成
(结构如图所示)受热分解可生成 和
和 。
。 是一种优良的耐高温结构陶瓷。下列有关说法
是一种优良的耐高温结构陶瓷。下列有关说法
A. 属于分子晶体 属于分子晶体 |
B.键角: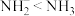 |
C.基态 和N原子的未成对电子数之比为 和N原子的未成对电子数之比为 |
D. 中的 中的 、N原子轨道的杂化类型相同 、N原子轨道的杂化类型相同 |
您最近一年使用:0次
名校
4 . X、Y、Z、M、Q五种短周期元素,原子序数依次增大。Y元素原子的L层电子是K层的2倍,Y元素与Z、M元素相邻,且与M元素同主族;化合物 的电子总数为18个;化合物
的电子总数为18个;化合物 是工业上重要的有机溶剂。下列说法
是工业上重要的有机溶剂。下列说法不正确 的是
 的电子总数为18个;化合物
的电子总数为18个;化合物 是工业上重要的有机溶剂。下列说法
是工业上重要的有机溶剂。下列说法| A.原子半径:Z<Y<M |
| B.最高价氧化物对应水化物的酸性:Z>Y>M |
C. 易溶于水,其水溶液呈碱性 易溶于水,其水溶液呈碱性 |
| D.X、Z和Q三种元素形成的化合物一定是共价化合物 |
您最近一年使用:0次
2024-06-10更新
|
89次组卷
|
2卷引用:浙江省丽水市发展共同体2023-2024学年高一下学期5月期中考试化学试题
名校
解题方法
5 . 卤素可形成许多结构和性质特殊的化合物。回答下列问题:
(1)下列说法正确的是___________。
(2)ClO2中心原子为Cl,Cl2O中心原子为O,二者均为V形结构,但ClO2中存在大π键(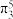 ),ClO2中Cl原子的轨道杂化方式
),ClO2中Cl原子的轨道杂化方式___________ ;O-Cl-O键角___________ Cl-O-Cl键角(填“>”“<”或“=”)。比较ClO2与Cl2O中Cl-O键的键长并说明原因___________ 。
(3)470K时,F2与Cl2反应生成ClF,常温常压下,ClF为无色气体,固态ClF的晶体类型为___________ 。
(4)一定条件下,CuCl2、K和F2反应生成KCl和化合物X。已知X属于四方晶系,晶胞结构如图所示(晶胞参数 ,
,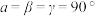 ),其中Cu化合价为+2。上述反应中K和F2的物质的量之比为
),其中Cu化合价为+2。上述反应中K和F2的物质的量之比为___________ 。与Cu原子距离最近的F原子的数目为___________ ,若该化合物的密度为 ,则阿伏加德罗常数的值NA=
,则阿伏加德罗常数的值NA=___________ (用含 、a、c的代数式表示。
、a、c的代数式表示。
(1)下列说法正确的是___________。
A.能量最低的激发态F原子的电子排布图为: |
| B.化学键中离子键成分的百分数:CaF2>LiF>NaF |
| C.HF的沸点比H2O低是因为HF氢键的键能小于H2O |
| D.已知N—F键的极性比N—H的极性强,因此NF3分子的极性比NH3的极性弱 |
(2)ClO2中心原子为Cl,Cl2O中心原子为O,二者均为V形结构,但ClO2中存在大π键(
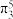 ),ClO2中Cl原子的轨道杂化方式
),ClO2中Cl原子的轨道杂化方式(3)470K时,F2与Cl2反应生成ClF,常温常压下,ClF为无色气体,固态ClF的晶体类型为
(4)一定条件下,CuCl2、K和F2反应生成KCl和化合物X。已知X属于四方晶系,晶胞结构如图所示(晶胞参数
 ,
,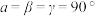 ),其中Cu化合价为+2。上述反应中K和F2的物质的量之比为
),其中Cu化合价为+2。上述反应中K和F2的物质的量之比为 ,则阿伏加德罗常数的值NA=
,则阿伏加德罗常数的值NA= 、a、c的代数式表示。
、a、c的代数式表示。
您最近一年使用:0次
名校
解题方法
6 . 短周期主族元素A、B、C、D的原子序数依次增大,A、B、D分别位于不同周期,且B和D是同主族,B的最外层电子数是内层的3倍,C是同周期原子半径最大的,下列说法正确的是
| A.A与B、D均可形成18电子分子 |
| B.B、C两种元素形成的化合物中只含离子键 |
| C.B的非金属性强于D,故简单气态氢化物的沸点水高于硫化氢 |
D.离子半径大小关系: |
您最近一年使用:0次
名校
7 . 下列物质中含有非极性共价键的是
A. | B. | C.Ar | D. |
您最近一年使用:0次
名校
8 . 下列物质熔化时,不破坏化学键的是
| A.氯化钠 | B.十七烷 | C.金刚石 | D.铜 |
您最近一年使用:0次
2024-05-17更新
|
411次组卷
|
4卷引用:2024届浙江省金华市金华第一中学高三下学期模拟预测化学试题
2024届浙江省金华市金华第一中学高三下学期模拟预测化学试题山东省济南市2024届高三下学期高考针对性训练(5月)化学试题(已下线)专题03 物质结构与性质-【好题汇编】5年(2020-2024)高考1年模拟化学真题分类汇编(山东专用)(已下线)第03讲 分子结构与性质、化学键(练习)-【上好课】2025年高考化学一轮复习讲练测(新教材新高考)
名校
解题方法
9 . 短周期主族元素W、X、Y、Z在元素周期表中的相对位置如图所示。下列说法不正确 的是
| Y | W | |||
| X | Z |
A.简单离子半径: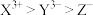 | B.简单氢化物的沸点: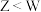 |
C.阴离子的还原性: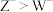 | D. 和 和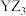 的化学键类型相同 的化学键类型相同 |
您最近一年使用:0次
2024-05-10更新
|
63次组卷
|
2卷引用:浙江省9+1高中联盟2023-2024学年高一下学期4月期中考试化学试题
名校
解题方法
10 . 科学家发现了一种四苯基卟啉络合的铁催化剂(Q),在可见光的照射下可以将 还原为
还原为 。下列有关叙述错误的是
。下列有关叙述错误的是
 还原为
还原为 。下列有关叙述错误的是
。下列有关叙述错误的是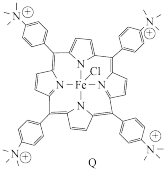
A.Q中N原子都是 杂化 杂化 | B.Fe提供空轨道形成配位键 |
| C.Q所含第二周期元素中,N的电负性最大 | D.1mol Q含36mol  型 型 键 键 |
您最近一年使用:0次
2024-05-06更新
|
336次组卷
|
5卷引用:选择题11-16



